-
25℃时在10 mL 0.1mol·L—1Na2CO3溶液中逐滴加入0.1 mol·L—1HCl溶液20 mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示。下列说法不正确的是
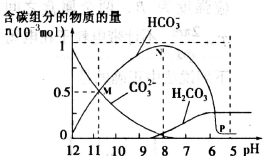
A.HCl溶液滴加一半时,溶液pH>7
B.当溶液的pH=8时,溶液中NaHCO3的物质的量浓度为0.1mol·L—1
C.0.1 mol·L—1Na2CO3溶液中c(Na+)+c(H+)=c(OH—)+2c(CO32—)+c(HCO3—)
D.在M点:c(Na+)>c(CO32—)=c(HCO3—)>c(OH—)>c(H+)
高三化学选择题极难题查看答案及解析
-
某课外兴趣小组进行电解原理的实验探究,做了如下的实验:以铜为电极,按如图所示的装置电解饱和食盐水。
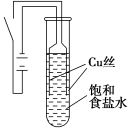
实验现象:接通电源30 s内,阳极附近出现白色浑浊,之后变成橙黄色浑浊,此时测定溶液的pH约为10。一段时间后,试管底部聚集大量红色沉淀,溶液仍为无色。
查阅资料:
物质
氯化铜
氧化亚铜
氢氧化亚铜(不稳定)
氯化亚铜
颜色
固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色
红色
橙黄色
白色
*相同温度下CuCl的溶解度大于CuOH
下列说法错误的是
A.反应结束后最终溶液呈碱性
B.阴极上发生的电极反应为:2H2O + 2e-¯ ═ H2↑+ 2OH-¯
C.电解过程中氯离子移向阳极
D.试管底部红色的固体具有还原性
高三化学选择题极难题查看答案及解析
-
含MgCl2、AlCl3均为n mol的混合溶液,向其中滴NaOH溶液至过量.加入NaOH的物质的量与生成沉淀的物质的量的关系正确的是(离子(或物质)沉淀pH见表)
A.
B.
C.
D.
离子
Mg2+
Al3+
物质
Al(OH)3
开始沉淀pH
8.93
3.56
开始溶解pH
8.04
完全沉淀pH
10.92
4.89
完全溶解pH
12.04
高三化学选择题极难题查看答案及解析
-
在l00mL密度为1.2g/mL稀硝酸中,加入一定量的镁和铜组成的混合物,充分反应后金属完全溶解(假设还原产物只有NO),向反应后溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀质量比原金属质量增加5. lg。则下列叙述不正确是
A.当金属全部溶解时收集到NO气体的体积为2.24L(标准状况)
B.当生成沉淀的量最多时,消耗NaOH溶液体积最小为l00mL
C.原稀硝酸的物质的量浓度一定为4 mol/L
D.参加反应金属总质量( m)为9.6g>m>3. 6g
高三化学选择题极难题查看答案及解析
-
已知重铬酸钾(K2Cr2O7)溶液中存在如下平衡:Cr2O7 2-(橙色)+ H2O
2H++ 2CrO42- (黄色),①向2 mL 0.1 mol·L-1 K2Cr2O7溶液中滴入3滴6 mol·L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色。②向2 mL 0.1 mol·L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O7 2- + 14H++ 6Fe2+
2Cr3+(绿色) + 6Fe3+ + 7H2O。下列分析正确的是
A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡
B.实验②能说明氧化性:Cr2O7 2-> Fe3+
C. CrO42- 和Fe2+在酸性溶液中可以大量共存
D.稀释K2Cr2O7溶液时,溶液中各离子浓度均减小
高三化学选择题极难题查看答案及解析
-
3.87克锌铜合金完全溶解于150mL、密度为1.20g/cm3、质量分数为21%的稀硝酸中,得到NO气体896mL (标准状况),向反应后的溶液中加入适量的1.0mol/LNaOH溶液,恰使溶液中的金属离子全部沉淀。下列说法不正确是( )
A.该稀硝酸中HNO3的物质的量浓度是4.0mol/L
B.加入NaOH溶液的体积是560mL
C.被还原的硝酸的物质的量为0.04mol
D.得到的金属氢氧化物的沉淀为5.81克
高三化学选择题极难题查看答案及解析
-
将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加入 3 mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g。下列叙述不正确的是( )
A. 当生成的沉淀量达到最大时,消耗NaOH 溶液的体积V≥100 mL
B. 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4 mol
C. 参加反应的金属的总质量9.6 g>m>3.6 g
D. 当金属全部溶解时收集到 NO气体的体积一定为2.24 L
高三化学选择题极难题查看答案及解析
-
反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2
下列说法正确的是 ( )
A. 两个反应中均为硫元素被氧化
B. 碘元素在反应①中被还原,在反应②中被氧化
C. 氧化性:MnO2>SO42->IO3->I2
D. 反应①、②中生成等量的I2时转移电子数比为1:5
高三化学选择题极难题查看答案及解析
-
酒石酸是葡萄酒中特有的一种有机酸,葡萄酒的pH主要取决于酒石酸的含量,正常的葡萄酒pH约为2.9~3.8。常温下,酒石酸(用H2T表示)水溶液中三种微粒所占的分数(a)与pH的关系如图所示。下列表述不正确的是
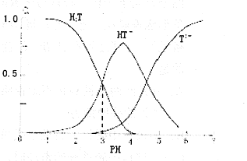
A.葡萄酒中除了存在酒石酸外,还存在酒石酸盐
B.常温下,H2T
H++HT- Ka=10-3
C.当葡萄酒的pH为3.7时,HT一所占分数达到最大,此时葡萄酒中H2T>T2-
D.当HT一和T2-物质的量浓度相等时,溶液中水电离出来的氢离子浓度小于纯水中氢离子的浓度
高三化学选择题极难题查看答案及解析
-
已知反应①:
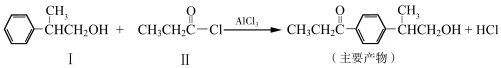
化合物Ⅱ可由化合物Ⅲ合成:
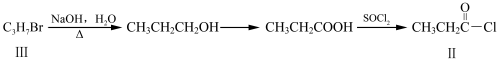
(1)化合物Ⅰ的分子式为 。反应①的反应类型为 。
(2)过量的化合物Ⅰ与HOOCCH2CH2COOH发生酯化反应,反应的化学方程式为 (注明条件)。
(3)化合物Ⅲ的结构简式为 。化合物Ⅲ可与NaOH乙醇溶液共热,反应的化学方程式 。
(4)化合物Ⅰ在一定条件下氧化生成化合物Ⅳ(分子式为C9H10O),化合物Ⅳ的一种同分异构体Ⅴ能发生银镜反应,Ⅴ的核磁共振氢谱除苯环峰外还有三组峰,峰面积之比为为2:2:1,Ⅴ的结构简式为 。
(5)一定条件下,1分子
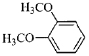 与1分子
与1分子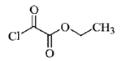 也可以发生类似反应①的反应,有机化合物结构简式为
也可以发生类似反应①的反应,有机化合物结构简式为 高三化学选择题极难题查看答案及解析