-
下列图象是表示铁加入到一定量硝酸中时,铁和硝酸铁之间物质的量(mol)的关系,其中正确的是
A.
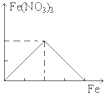 B.
B.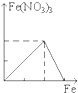 C.
C.D.
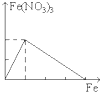
高三化学单选题困难题查看答案及解析
-
某溶液中可能含有OH-、CO32-、A1O2-、SiO32-、SO42-、HCO3-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如下图所示。下列说法正确的是
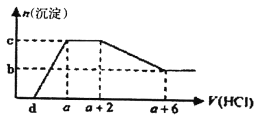
A. 原溶液中可能含有Na2SO4、可能不含有CO32-
B. 原溶液中一定含有的阴离子只有:OH-、A1O2-、CO32-
C. 原溶液中含CO32-与A1O2-的物质的量之比为3:4
D. a-d>3/4
高三化学单选题困难题查看答案及解析
-
我国明崇祯年间《徐光启手迹》记载了《造强水法》 :“绿钒(FeSO4•7H2O)五斤,硝五斤,将矾炒去,约折五分之一,将二味同研细,次用铁作锅,…… 锅下起火,取气冷定,开坛则药化为水……。用水入五金皆成水,惟黄金不化水中,加盐则化。……强水用过无力……”。下列有关解释错误的是
A.“将矾炒去,约折五分之一”后生成FeSO4•4H2O
B.该方法所造“强水”为硝酸
C.“惟黄金不化水中,加盐则化”的原因是加人 NaCl溶液后氧化性增强
D.“强水用过无力”的原因是“强水”用过以后,生成了硝酸盐溶液,其氧化性减弱
高三化学单选题困难题查看答案及解析
-
下列实验过程、实验目的、判定及解释都正确的是
编号
实验目的
实验过程
判定、解释
A
配制0.4000mol·L-1的NaOH溶液
称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,直接转移至250mL容量瓶中定容
正确,4.0g固体NaOH的物质的量为0.1mol,定容到250mL的容量瓶,物质的量浓度恰好为0.4000mol·L-1
B
探究维生素C的还原性
向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化
正确,FeCl3具有氧化性,能与具有还原性的维生素C发生反应,使溶液的颜色由黄色变为浅绿色(Fe2+)
C
制取并纯化
氢气
向稀盐酸中加入锌粒,将生成的气体依次通过NaOH溶液、浓硫酸和KMnO4溶液
正确,产生的气体依次通过NaOH溶液、浓硫酸和KMnO4溶液,除去可能的酸性气体、水蒸气和还原性气体等杂质,得到纯净氢气
D
探究浓度对反应速率的影响
向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL 5%H2O2溶液,观察实验现象
错误,反应的离子方程式为
H2O2+NaHSO3=Na++H++SO42-+H2O
没有明显的实验现象,因此不能用此反应探究浓度对反应速率的影响
A. A B. B C. C D. D
高三化学单选题困难题查看答案及解析
-
聚合硫酸铁[Fe(OH)SO4]n能用作净水剂(絮凝剂),可由绿矾(FeSO4·7H2O)和KClO3在水溶液中反应得到。下列说法不正确的是
A.KClO3作氧化剂,每生成1 mol [Fe(OH)SO4]n消耗6/n mol KClO3
B.生成聚合硫酸铁后,水溶液的pH增大
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
高三化学单选题困难题查看答案及解析
-
常温下将NaOH溶液滴加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
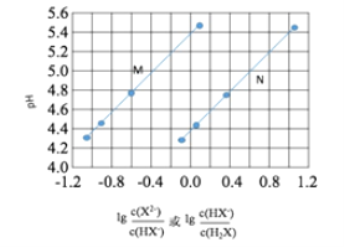
A. Ka2(H2X)的数量级为10–6
B. 曲线N表示pH与
的变化关系
C. NaHX溶液中c(H+)>c(OH-)
D. 当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+)
高三化学单选题困难题查看答案及解析
-
处理超标电镀废水,使其NaCN含量低于0.5 mg/L,即可达到排放标准,反应分两步进行。第一步NaCN与NaClO反应,生成NaOCN和NaCl。第二步NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2。已知HCN是弱酸,易挥发,有剧毒;HCN、HOCN中N元素的化合价相同。下列说法正确的是
A. 处理NaCN超标电镀废水的过程中无元素化合价的改变
B. 第一步反应溶液应调节为酸性,可避免生成有毒物质HCN
C. 第二步发生的反应为2OCN- + 3ClO-
2CO2↑ + CO32− + 3Cl- + N2↑
D. 处理100 m3含NaCN 10.3 mg/L的废水实际至少需要50 mol NaClO
高三化学单选题困难题查看答案及解析
-
向含a mol NaClO的溶液通入b mol SO2充分反应(不考虑二氧化硫与水之间的反应以及次氯酸的分解)。下列说法不正确的是
A.当0<b<a/3时:SO2+H2O+3ClO-=
+2HClO+Cl-
B.当b=a时,SO2+H2O+ClO-==2H++Cl-+
C.当a/3≤b≤a时,反应后溶液中H+的物质的量: 0<n(H+)≤2b mol
D.当0<b<a时,反应后溶液中ClO-、Cl-和
物质的量之比为:(a-b)∶b∶b
高三化学单选题困难题查看答案及解析
-
某同学用KSCN溶液和
溶液探究
的还原性时出现异常现象,实验如下:

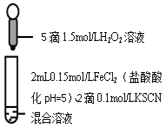

溶液变红,大约10秒左右红色褪去,有气体生成
经检验为
。取褪色后溶液,滴加盐酸和
溶液,产生白色沉淀
溶液变红且不褪色,有气体生成
经检验为
,经检验有丁达尔效应。
溶液变红且不褪色,滴加盐酸和
溶液,无白色沉淀,经检验无丁达尔效应。
下列说法不正确的是
A.对比
,可以判定酸性条件下
可以氧化
B.实验
中发生的氧化还原反应有两种
C.
中红色溶液中含有
胶体
D.
中发生的氧化还原反应为:
高三化学单选题困难题查看答案及解析
-
处理超标电镀废水,使其NaCN含量低于0.5 mg/L,即可达到排放标准,反应分两步进行。第一步NaCN与NaClO反应,生成NaOCN和NaCl。第二步NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2。已知HCN是弱酸,易挥发,有剧毒;HCN、HOCN中N元素的化合价相同。下列说法正确的是
A. 处理NaCN超标电镀废水的过程中无元素化合价的改变
B. 第一步反应溶液应调节为酸性,可避免生成有毒物质HCN
C. 第二步发生的反应为2OCN- + 3ClO-
2CO2↑ + CO32− + 3Cl- + N2↑
D. 处理100 m3含NaCN 10.3 mg/L的废水实际至少需要50 mol NaClO
高三化学单选题困难题查看答案及解析