-
Fe2+基态核外电子排布式为 ____________。
高三化学填空题简单题查看答案及解析
-
Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为__、__(填标号)。
A.
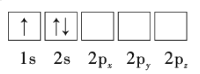
B.
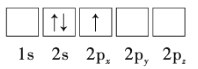
C.
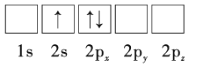
D.
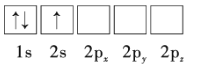
(2)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是___。
高三化学填空题简单题查看答案及解析
-
用符号“>”或“<”表示下列各项关系。
(1)第一电离能:Na __________ Mg,Mg _______ Ca。
(2)电负性:O ________ F,F ________ Cl。
(3)能量高低:ns ________ (n+1)s,ns ________ np。
高三化学填空题简单题查看答案及解析
-
某元素的激发态(不稳定状态)原子的电子排布式为
,则该元素基态原子的电子排布式为 _______ ;其最高价氧化物对应水化物的化学式是 ______ 。
高三化学填空题简单题查看答案及解析
-
以下列出的是一些原子的2p能级和3d能级中电子的排布情况。试判断,违反了泡利不相容原理的是 ___________ (填序号,下同),违反了洪特规则的是 _______ 。
①
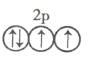 ②
②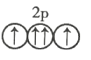 ③
③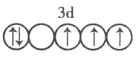 ④
④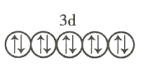 ⑤
⑤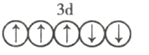
高三化学填空题简单题查看答案及解析
-
汽车尾气中CO、
在一定条件下可发生反应
,一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和
,
的物质的量随时间的变化曲线如图所示:
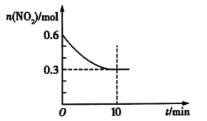
(1)0~10min内该反应的平均反应速率
________
(2)恒温恒容条件下,不能说明该反应已经达到平衡状态的是________(填序号)
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变
高三化学填空题简单题查看答案及解析
-
将一铜棒和碳棒用导线连接后,插入盛有20%NaC1溶液的U形管中。
(1)若该装置不是原电池,请说明原因:________(如果回答此题,则下面的②不用回答)。
(2)若该装置是原电池,请采取适当的措施(电极材料、溶液浓度均不变)来提高电池的放电效率:________。
高三化学填空题简单题查看答案及解析
-
(1)锂空气电池比传统的锂离子电池拥有更强的蓄电能力,是传统锂离子电池容量的10倍,其工作原理示意图如图。
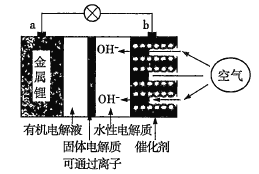
放电时,b电极为电源的__极,电极反应式为__。
(2)汽车尾气中CO、NO2在一定条件下可发生反应4CO(g)+2NO2(g)
4CO2(g)+N2(g),一定温度下,向容积固定的2L的密闭容器中充入一定量的CO和NO2,NO2的物质的量随时间的变化曲线如图所示。
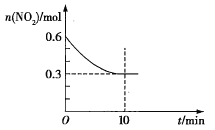
①0~10min内该反应的平均反应速率v(CO)=__。
②恒温恒容条件下,不能说明该反应已经达到平衡状态的是__(填序号)。
A.容器内混合气体颜色不再变化
B.容器内的压强保持不变
C.容器内混合气体密度保持不变
高三化学填空题简单题查看答案及解析
-
(1)下列是中学化学中熟悉的物质:
O2 金刚石 NaBr H2SO4 Na2CO3 Na2S NaHSO4
回答下列问题:
这些物质中,只含共价键的是________;只含离子键的是________;既含离子键又含共价键的是________。
(2)写出下列物质的电子式。
Na2O2:_________________;
NH4H:_______________________;
(3)写出下列物质的结构式。
CO2:____________________
H2O2:_______________________
高三化学填空题简单题查看答案及解析
-
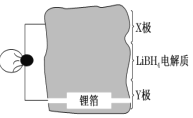
(1)全固态锂离子电池的结构如图所示,放电时电池反应为 2Li+MgH2=Mg+2LiH。放电时,X 极作_________极。充电时,Y 极反应式为___________。
(2)电渗析法处理厨房垃圾发酵液,同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子)。
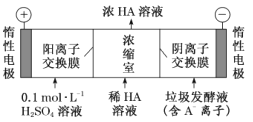
①阳极的电极反应式为 ________________
②简述浓缩室中得到浓乳酸的原理:________________
③电解过程中,采取一定的措施可控制阳极室的 pH 约为 6~8,此时进入浓缩室的OH-可忽略不计。400 mL 10 g∙L −1 乳酸溶液通电一段时间后,浓度上升为 145 g∙L −1 (溶液体积变化忽略不计),阴极上产生的 H2 在标准状况下的体积约为_____________L。(乳酸的摩尔质量为90 g•mol-1)
高三化学填空题简单题查看答案及解析