-
据报道复旦大学修发贤教授课题组成功制备出砷化铌纳米带,并观测到其表面态具有百倍于金属铜薄膜和千倍于石墨烯的导电性。相关研究论文已在线发表于权威科学期刊《自然》。回答下列问题:
(1)铌元素(Nb)为一种金属元素,其基态原子的核外电子排布式为[Kr]4d55s1。下列是Nb的不同微粒的核外电子排布式,其中失去最外层1个电子所需能量最小的是___(填标号)。
a.[Kr]4d35s15p1b.[Kr]4d45s1c.Kr]4d2d.Kr]4d3
(2)砷为第VA族元素,砷可以与某些有机基团形成有机化合物,如(ClCH=CH)2AsCl,其中As原子与2个C原子、1个Cl原子形成的VSEPR模型为____。
(3)英国曼彻斯特大学物理学家安德烈·盖姆和康斯坦丁诺沃肖洛夫用微机械剥离法成功从石墨中分离出石墨烯,因此共同获得2010年诺贝尔物理学奖;而石墨烯具有优异的光学、电学、力学特性在材料学、微纳加工、能源、生物医学和药物传递等方面具有重要的应用前景,被认为是一种未来革命性的材料。
已知“石墨烯”的平面结构如图所示,一定条件下石墨烯与H2发生加成反应生成石墨烷,石墨烷中碳原子杂化类型是___,石墨烯导电的原因是____。

(4)石墨烯也可采用化学方法进行制备如采用六氯苯、六溴苯作为原料可制备石墨烯。下表给出了六氯苯、六溴苯、苯六酸俗名为蜜石酸的熔点和水溶性:
物质
六氯苯
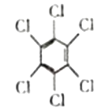
六溴苯
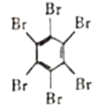
苯六酸
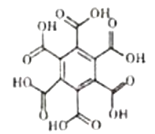
熔点/℃
231
325
287
水溶性
不溶
不溶
易溶
六溴苯的熔点比六氯苯高的原因是____,苯六酸与六溴苯、六氯苯的水溶性存在明显的差异本质原因是___。
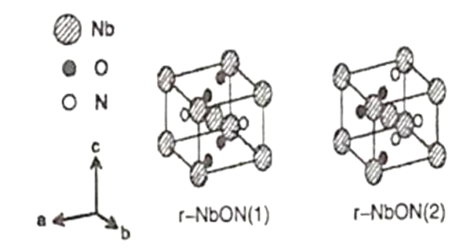
(5)出于以更高效率利用太阳光等目的研制出金红石型铌氧氮化物(NbON),比以往的光学半导体更能够吸收长波长侧的光,作为光学半导体的新材料。该化合物的晶胞有如图所示的两种构型,若晶胞的边长为apm,该晶体的密度为__g·cm-3。(NA是阿伏加德罗常数的值,相关原子量:Nb—93)
高三化学填空题困难题查看答案及解析
-
煤和甲烷既是重要的常用燃料,又是重要的化工原料。根据题意,回答下列问题:
I.煤制天然气过程中,存在多种化学反应,其中在煤气化装置中发生反应①:C(s) + H2O(g)=CO(g) + H2(g) ∆H = +135 kJ • mol-1 ,而在水气变换装置中发生反应②:CO(g)+H2O(g)=CO2(g)+ H2(g) ∆H =-41 kJ • mol-1
(1)煤气化前,需要通入一定量的氧气与碳发生燃烧反应,请利用平衡移动原理说明通入氧气的作用:_____________________
(2)写岀碳和二氧化碳反应生成一氧化碳的热化学方程式_____。
(3)如图表示发生反应①后进入反应②装置的n( H2O)/n(CO)与反应②中CO平衡转化率、温度的变化关系。
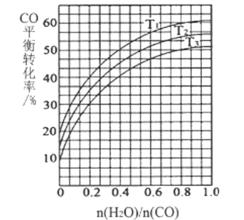
若n(H2O)/n(CO)为0.8,一定量的煤和水蒸气经反应①和反应②后,得到CO与H2的 物质的量之比为1:3,则反应②所对应的温度是_____(填“T1”、“T2”或“T3”)。
Ⅱ.甲烷重整技术主要是利用甲烷和其他原料来制备合成气(CO和h2混合气体)。现在常(见的重整技术有甲烷——二氧化碳重整、甲烷——水蒸气重整,其反应分别为CH4(g)+3CO2(g)⇌2H2O(g)+4CO(g);CH4(g)+H2O(g)⇌CO(g)+3H2(g)
(4)甲烷——二氧化碳重整的催化转化原理如图所示:
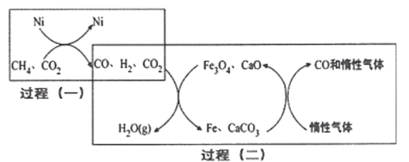
①过程(二)实现了含氢物种与含碳物种的分离,写出生成H2O(g)的化学方程式:______
②假设过程(一)和过程(二)中各步反应均转化完全,则下列说法正确的是_____ (填序号)。
a.过程(一)和过程(二)中均含有氧化还原反应
b.过程(二)中使用的催化剂为Fe3O4和CaCO3
C.若过程(一)投料比
,可导致过程(二)中催化剂失效
(5)通过计算机模拟甲烷——水蒸气重整实验测得,在操作压强为0.1Mpa、水碳比n(H2O)/n(CH4)为1.0,温度为900℃,反应达到平衡时,H2的物质的量分数为0.6。已知该反应的速率方程v=kP(CH4)·P-1(H2),式中k为速率常数,P为气体分压,气体分压=总压×气体物质的量分数,则此时该反应速率v=_____(用含k的式子表示);900℃时,该反应的压强平衡常数Kp=_____(用平衡分压代替平衡浓度计算)。
高三化学填空题困难题查看答案及解析
-
香料G的一种合成工艺如下图所示:
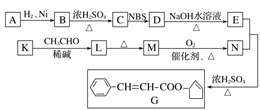
核磁共振氢谱显示A有两种峰,且峰面积之比为1∶1。
已知:CH3CH2CH===CH2
CH3CHBrCH===CH2
CH3CHO+CH3CHO
CH3CHOHCH2CHOCH3CHOHCH2CHO
CH3CH===CHCHO+H2O
请回答下列问题:
(1)A的结简式为__________,G中官能团的名称为___________。
(2)检验M已完全转化为N的实验操作是____________________。
(3)有学生建议,将M→N的转化用KMnO4(H+)代替O2,老师认为不合理,原因是_______________。
(4)写出下列转化的化学方程式,并标出反应类型:
K→L:________________,反应类型:________。
(5)F是M的同系物,比M多一个碳原子。满足下列条件的F的同分异构体有________种。(不考虑立体异构)
①能发生银镜反应 ②能与溴的四氯化碳溶液加成 ③苯环上有2个对位取代基
(6)以丙烯和NBS试剂为原料制备甘油(丙三醇),请设计合成路线(其他无机原料任选)。________
请用以下方式表示:A
 B…
B…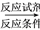 目标产物
目标产物高三化学填空题困难题查看答案及解析
-
2一氨-3—氯苯甲酸是白色晶体,其制备流程如下:
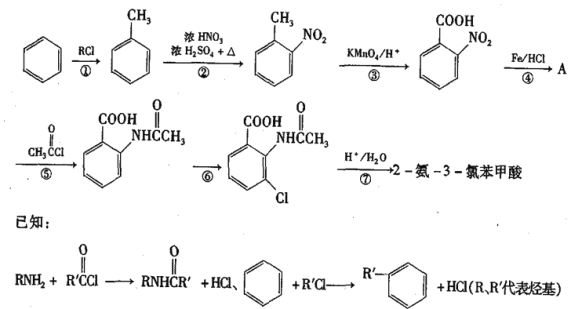
回答下列相关问题
(1)
的名称是___________,2-氨-3-氯苯甲酸中含N官能团的电子式为___________。
(2)反应①中R代表的是___________,反应②的反应类型为___________。
(3)如果反应③中KMnO4的还原产物为MnSO4,请写出该反应的化学方程式___________。
(4)A的结构简式为___________,⑥的反应条件为___________。
(5)符合下列条件的同分异构体的结构简式为___________。
a 式量比
大42的苯的同系物;
b 与酸性KMnO4反应能生成二元羧酸
c 仅有3种等效氢
(6)事实证明上述流程的目标产物的产率很低;据此,研究人员提出将步骤⑥设计为以下三步,产率有了一定提高。
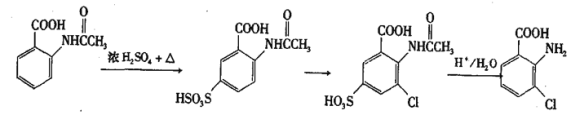
分析产率提高的原因是___________。
高三化学填空题困难题查看答案及解析
-
莫沙朵林是一种镇痛药,它的合成路线如下:
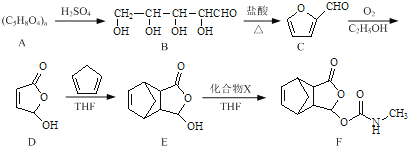
(1)B中手性碳原子数为____________;化合物D中含氧官能团的名称为____________。
(2)C与新制氢氧化铜反应的化学方程式为____________。
(3)写出同时满足下列条件的E的一种同分异构体的结构简式:____________
I.核磁共振氢谱有4个峰;
Ⅱ.能发生银镜反应和水解反应;
Ⅲ.能与FeCl3溶液发生显色反应.
(4)已知E+X→F为加成反应,化合物X的结构简式为____________。
(5)已知:
.化合物
是合成抗病毒药阿昔洛韦的中间体,请设计合理方案以
和
为原料合成该化合物(用合成路线流程图表示,并注明反应条件).______________。
合成路线流程图示例如下:
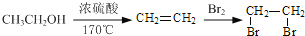 。
。高三化学填空题困难题查看答案及解析
-
盐酸金刚烷胺是一种治疗和预防病毒性感染的药物,可用于抑制病毒穿入宿主细胞,从结构上看是一种对称的三环状胺,可以利用环戊二烯(CPD)来制备合成,流程图如下:
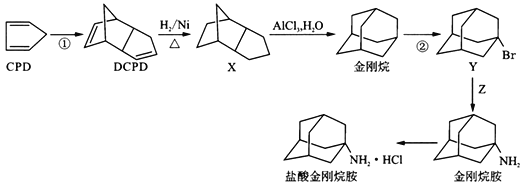
(1)下列关于X和金刚烷说法正确的是_________。
A.金刚烷和X互为同分异构体,均可以发生氧化反应和取代反应
B.金刚烷和X均可以使溴水褪色
C.金刚烷和X均具有与芳香烃相似的化学性质
D.金刚烷和X均不存在手性碳原子
(2)反应①的反应类型为____________,反应②的条件为________________。
(3)有机物Y的一氯代物的同分异构体的数目为___________,写出Y与氢氧化钠的乙醇溶液反应的化学方程式___________________________________。
(4)有机物Z是一种重要的有机氮肥,在核磁共振氢谱谱图中只有一个峰,写出Z与浓硫酸反应的化学方程式___________________________________。
(5)CPD可以与Br2的CCl4溶液反应,写出其所有可能产物的结构简式___________。
(6)参照上述流程图,并用流程图中出现的试剂和
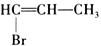 为原料合成
为原料合成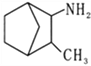 ,设计其合成路线_________。
,设计其合成路线_________。高三化学填空题困难题查看答案及解析
-
磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的价电子排布式为___。
(2)磷的一种同素异形体——白磷(P4)的空间构型为___,其键角为__,推测其在CS2中的溶解度___(填“大于”或“小于”)在水中的溶解度。
(3)膦(PH3)和氨(NH3)的键角分别为93.6°和107°,试用价层电子对互斥理论分析PH3的键角小于NH3的原因:___。
(4)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CCl4、SF6互为等电子体,则A、B的化学式分别为___、__,A的中心原子杂化轨道类型为___。
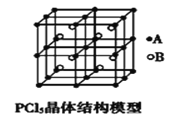
(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素是__(填元素符号)。
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如下表所示。试从结构的角度分析它们熔点不同的原因:__。
物质
BN
AlN
GaN
熔点/℃
3000
2200
1700
高三化学填空题困难题查看答案及解析
-
有机物M常做消毒剂、抗氧化剂等,用芳香烃A制备M的一种合成路线如下:
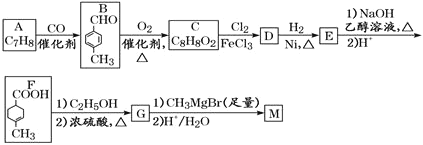
已知:R1COOR2
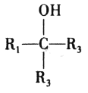
请回答下列问题:
(1)A的结构简式为___________;D中官能团的名称为___________。
(2)C生成D的反应类型为___________;G的分子式为___________。
(3)由E与足量氢氧化钠的乙醇溶液反应的化学方程式为___________。
(4)M的结构简式为___________。
(5)芳香族化合物H与C互为同分异构体,且能发生水解反应,则符合要求的H的结构共有________种;写出其中核磁共振氢谱有4组峰,且峰面积之比为1:2:2:3的任意一种物质的结构简式_________。
(6)参照上述合成路线和信息,以苯甲酸甲酯和CH3MgBr为原料(无机试剂任选)设计制备
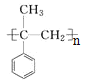 的合成路线___________。
的合成路线___________。高三化学填空题困难题查看答案及解析
-
LiFePO4、聚乙二醇、LiPF6、LiAsF6、LiCl等常用作锂离子聚合物电池的材料和载体。
回答下列问题:
(1)LiFePO4中Fe的价层电子排布式为___________。
(2)LiPF6、LiAsF6和LiCl中所含的四种非金属元素电负性由大到小的顺序为___________。
(3)含氧酸的通式可写为(HO)mROn,根据化学学科的规律下列几种酸中酸性与H3PO4相近的有________。
a.HClO b.HClO3 c.H2SO3 d.HNO2
(4)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸(
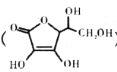 )常被用作碳包覆的碳源,其易溶于水的原因是____________________,该分子中碳原子的杂化方式为___________。
)常被用作碳包覆的碳源,其易溶于水的原因是____________________,该分子中碳原子的杂化方式为___________。(5)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)
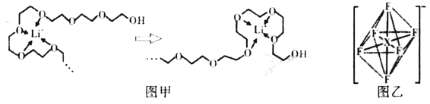
①从化学键角度看,Li+迁移过程发生___________(填“物理变化”或“化学变化”)。
②相同条件,Li+在___________(选填“LiPF6”或“LiAsF6”)中迁移较快,原因是___________。
(6)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl·3H2O属正交晶系(长方体形)晶胞参数为0.72mm、1.0nm、0.56nm。如图为沿x轴投影的晶胞中所有Cl原子的分布图和原子分数坐标。
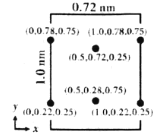
①该晶胞中Cl原子的数目为___________。
②LiCl·3H2O的摩尔质量为Mg·mol-1,设NA为阿伏加德罗常数的值,则LiCl·3H20晶体的密度为___g·cm-3(列出计算表达式)。
高三化学填空题困难题查看答案及解析
-
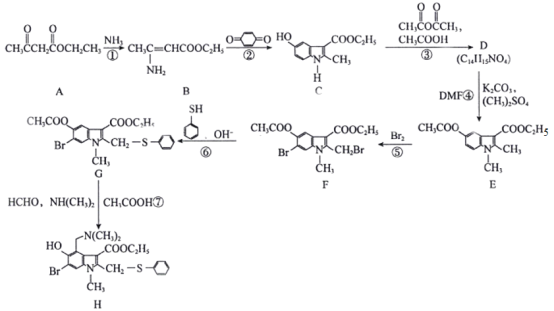
近期,李兰娟院士通过体外细胞实验发现抗病毒药物阿比多尔(H)能有效抑制冠状病毒,同时能显著抑制病毒对细胞的病变效应。合成阿比多尔的一条路线为:
已知:
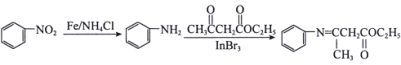 。
。回答下列问题:
(1)阿比多尔分子中的含氧官能团为__________、____________,D的结构简式为______________。
(2)反应②的化学方程式为_______________;反应③的作用是_______________;反应⑤的类型为________________。
(3)A的同分异构体中,能发生银镜反应且能与碳酸氢钠溶液反应放出气体的有______种(不考虑立体异构)。
(4)以下为中间体D的另一条合成路线:
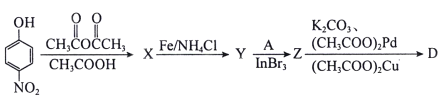
其中X、Y、Z的结构简式分别为_________、__________、_________。
高三化学填空题困难题查看答案及解析