-
肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料。实验室可用苯甲醛和乙酸酐、醋酸钠等原料经下列反应制取肉桂酸,其中苯甲醛为无色油状液体。已知:
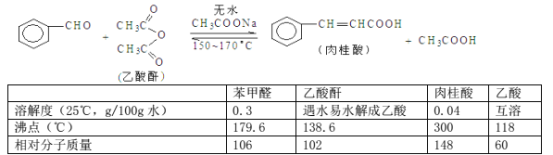
填空:
Ⅰ.合成:反应装置如图所示。向三颈烧瓶中先后加入研细的无水醋酸钠、4.8g苯甲醛和5.6g乙酸酐,振荡使之混合均匀。在150~170℃加热1小时,保持微沸状态。
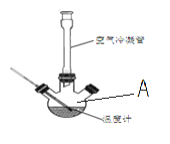
(1)仪器A的名称为___。
(2)空气冷凝管的作用是__,该装置加热要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是__。
(3)不能把无水CH3COONa换成CH3COONa·3H2O的原因是__。
Ⅱ.粗品精制:已知水蒸气蒸馏是分离提纯有机化合物的重要方法之一,可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从而达到分离提纯的目的。
将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
a.在搅拌下,向反应液中加入20mL水
b.再慢慢加入碳酸钠溶液
c.然后进行水蒸气蒸馏
d.待烧瓶内溶液冷却至室温,在搅拌下用加入盐酸酸化,析出大量晶体,过滤,洗涤,干燥。
(4)饱和Na2CO3溶液的作用有__。水蒸气蒸馏可除去的杂质是__;如何判断蒸馏终点___。
(5)若得到的肉桂酸晶体产品不纯,应采用__可得到纯度更高的产品。
(6)若最后得到纯净的肉桂酸5.0g,则该反应中的产率是__(保留两位有效数字)。
高三化学实验题简单题查看答案及解析
-
亚硝酰氯(ClNO)是有机物合成中的重要试剂,其沸点为 -5.5℃,易水解。已知:AgNO2 微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3 +HNO2,某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,相关实验装置如图所示。
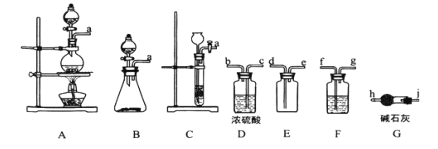
(1)制备 Cl2 的发生装置可以选用 _________ (填字母代号)装置,发生反应的离子方程式为________________________________________ 。
(2)欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为 a→_______→______→ _____→________→_______→______→______→______。(按气流方向,用小写字母表示,根据需要填,可以不填满,也可补充)。
(3)实验室可用下图示装置制备亚硝酰氯。其反应原理为:Cl2+2NO=2ClNO
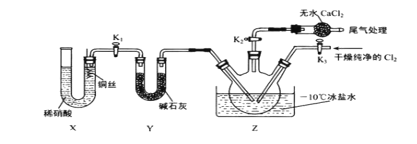
①实验室也可用 B 装置制备 NO , X 装置的优点为___________________ 。
②检验装置气密性并装入药品,打开 K2,然后再打开 K3,通入一段时间气体,其目的是 ___________________,然后进行其他操作,当 Z 中有一定量液体生成时,停止实验。
(4)已知:ClNO 与 H2O 反应生成 HNO2 和 HCl。
①设计实验证明 HNO2 是弱酸:_________________________________________。(仅提供的试剂:1 mol•L-1 盐酸、 1 mol•L-1HNO2 溶液、 NaNO2 溶液、红色石蕊试纸、蓝色石蕊试纸)。
②通过以下实验测定ClNO 样品的纯度。取 Z 中所得液体m g 溶于水,配制成 250 mL 溶液;取出 25.00 mL 样品溶于锥形瓶中,以 K2CrO4 溶液为指示剂,用 c mol•L-1 AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 20.00mL。滴定终点的现象是_____亚硝酰氯(ClNO)的质量分数为 _________。(已知: Ag2CrO4 为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12)
高三化学实验题简单题查看答案及解析
-
(三草酸合铁酸钾晶体)为翠绿色晶体,可用于摄影和蓝色印刷,110℃失去结晶水,230℃分解。某化学研究小组对
受热分解生成的气体产物和固体产物进行探究。
实验I:探究实验所得的气体产物,按下图装置进行实验(夹持仪器已略去,部分装置可重复使用)。
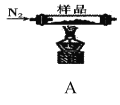
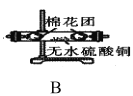
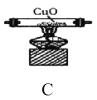



(1)实验室常用饱和
和饱和
的混合液制
,反应的化学方程式为_____________。
(2)装置的连接顺序为:A→__→__→__→__→__→F(填各装置的字母代号)。
(3)检查装置气密性后,先通一段时间
,其目的是________,实验结束时熄灭A、C两处的酒精灯,继续通
至常温,其目的是__________。
(4)实验过程中观察到F中的溶液变浑浊,C中有红色固体生成,则气体产物____(填化学式)。
(实验二)分解产物中固体成分的探究
(5)定性实验:经检验,固体成分含有
。
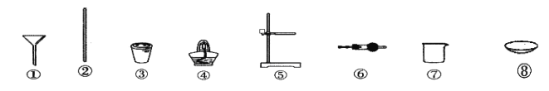
定量实验:将固体产物加水溶解、过滤洗涤、干燥,得到含铁样品。完成上述实验操作,需要用到下列仪器中的__________(填仪器编号)。
设计下列三种实验方案分别对该含铁样品进行含量的测定
(甲方案)

(乙方案)
(丙方案)

你认为以上方案中可以确定样品组成的有_____________方案。
(6)经测定产物中
,写出
分解的化学方程式_________。
高三化学实验题简单题查看答案及解析
-
氯化亚硝酰(NOC1,沸点为-5.5 °C )是有机合成中的重要试剂,为黄色气体,具有刺鼻恶臭味,遇水反应,有多种方法制备氯化亚硝酰。已知:HNO2既有氧化性又有还原性,AgNO2微溶于水,溶于硝酸:AgNO2 + HNO3 =AgNO3+ HNO2。
(1)将5g在300°C下干燥了3h并研细的KCl粉末装入50mL带有接头及抽真空用活塞的玻璃容器内。将容器尽量减压,在减压条件下通入0.002 mol NO2。反应12~36 min即可完成,红棕色的NO2消失,出现黄色的氯化亚硝酰,同时还得到一种盐,该盐的化学式为____________, 氯化钾需要“干燥”的原因是_____________。
(2)实验室可由氯气与一氧化氮在常温常压下合成氯化亚硝酰,装置如图所示。
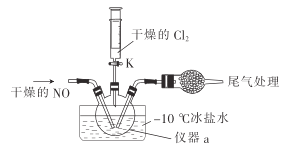
①仪器a的名称为__________。
②干燥管中盛放的试剂为____________。
③生成NOCl的化学方程式为________________。
(3)为验证NOCl与H2O反应后的溶液中存在Cl-和HNO2,设计如下实验步骤,完成下列表格。
步骤
实验现象或反应的化学方程式
①取5ml三颈烧瓶中产品,加入盛有水的烧杯中,充分反应
NOCl与H2O发应的化学方程式_______
②向烧杯中滴加足量AgNO3溶液,有白色沉淀生成,再加入足量稀硝酸
加入稀硝酸后,实验现象为___________
③向步骤②烧杯中滴加酸性KMnO4溶液
实验现象为___________
高三化学实验题简单题查看答案及解析
-
乳酸亚铁晶体([CH3CH(OH)COO]2Fe·3H2O,Mr=288)是常用的补铁剂易溶于水,吸收效果比无机铁好。乳酸亚铁可由乳酸与FeCO3反应制得。
I.制备碳酸亚铁(FeCO3)
已知FeCO3易被氧化:4FeCO3+6H2O+O2=4Fe(OH)3+4CO2。某兴趣小组设计如下方案制备FeCO3,实验装置如图:
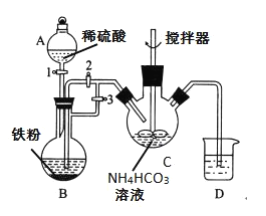
(1)仪器B的名称是__。
(2)利用如图所示装置进行实验,进行以下两步操作:
第一步:打开活塞1、3,关闭活塞2,反应一段时间;
第二步:关闭活塞3,打开活塞2,发现C中有白色沉淀和气体生成。
①第一步骤的目的是__。
②C中反应生成白色沉淀的离子方程式是:__。
③仪器C中的混合物经过滤,洗涤后得到FeCO3沉淀。实验室中进行过滤后沉淀洗涤的操作是:__。
④装置D中可盛装适量的水,该装置作用是__。
II.制备乳酸亚铁晶体和定量测量
(1)制备乳酸亚铁晶体。将制得的FeCO3加入到乳酸溶液中,加入少量铁粉,在70℃下搅拌使反应充分进行,一段时间后,经过分离提纯操作,从所得溶液中得到乳酸亚铁晶体。现需要设计实验检测产品在制备过程是否因氧化而发生变质,可选用的试剂__。
(2)用碘量法测定晶体样品中铁元素的含量并计算样品的纯度。称取3.00g晶体样品,在足量空气中灼烧成灰,加足量稀硫酸溶解,将所有可溶物配成l00mL溶液。取25.00mL该溶液加入过量的KI反应,加入几滴__(试剂名称)作指示剂,用0.l0mol/L的硫代硫酸钠溶液滴定(I2+2S2O32-=S4O62-+2I-),重复实验3次,滴定终点时平均消耗硫代硫酸钠25.00mL,则样品纯度为__。
高三化学实验题简单题查看答案及解析
-
已知1-丁醇的沸点为117.7℃,乙酸的沸点为118℃。甲同学拟在浓硫酸作用下,使1-丁醇和乙酸进行酯化反应制乙酸丁酯(反应温度115~125℃)。
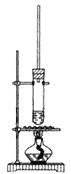
(1)反应装置不使用水浴加热或直接加热,而采取如图加热操作方式,其原因是____________________________。
(2)操作中使用相对较多乙酸的理由是______________________________。
(3)洗涤粗产物:将粗产物移至分液漏斗中,先用水洗涤,然后用10%Na2CO3溶液洗涤至中性,再用水洗涤,分液得有机层。如果不能判断哪层是有机层,可以用__________方法来判断。对有机层,进行洗涤除杂、除水后可得到粗产品。
(4)收集产物:将干燥好的产物移至蒸馏烧瓶中,加热蒸馏,收集125~127℃的馏分。要证明最终产物是纯净的乙酸丁酯,其方法是__________________________________。乙同学拟通过蒸馏的方法将1-丁醇和乙酸的无水混合物分离开。
实验步骤:①连接好装置,检查装置的气密性。②将混合物加入到蒸馏烧瓶中,并加入适量的试剂a。③加热到118℃,并收集馏分。④冷却后,再向烧瓶中加入试剂b。⑤加热到118℃,并收集馏分。
(5)试剂a 是___________,其作用是_________________________________。
(6)下列实验也需要用到温度计的是 ____________。
a.实验室制备硝基苯 b.实验室制备溴苯 c.实验室制备乙烯 d.银镜反应
高三化学实验题简单题查看答案及解析
-
在实验室里制取乙烯时,常因温度过高而发生副反应,部分乙醇跟浓H2SO4反应生成SO2,CO2,水蒸气和炭黑。
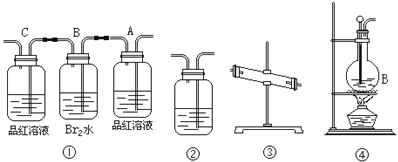
(1)用编号为①→④的实验装置设计一个实验,以验证上述反应混合气体中含CO2,SO2和水蒸气。用装置的连接顺序(按产物气流从左到右的流向): → → → 。___
(2)实验的装置(1)中A瓶的现象是___;结论为___;B瓶中的现象是___;B瓶溶液作用为___。若C瓶中品红溶液不褪色,可得到结论为___。
(3)装置③中加的固体药品是___,以验证混合气体中有___。装置②中盛的溶液是___,以验证混合气体中有___。
高三化学实验题简单题查看答案及解析
-
某化学研究性学习小组为了模拟工业流程从浓缩的海水中提取液溴,查阅资料知:Br2的沸点为59℃,微溶于水,有毒性。设计了如下操作步骤及主要实验装置(夹持装置略去):

①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入氯气至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③进行步骤②的同时,向B中通入足量SO2;
④关闭b,打开a,再通过A向B中缓慢通入足量Cl2;
⑤将B中所得液体进行蒸馏,收集液溴。
请回答:
(1)工业上采用电解饱和食盐水的方法来制备氯气,该反应的化学方程式为______________________________________________________________________;
(2)步骤②中鼓入热空气的作用为___________________________________;此实验中尾气可用_____(填选项字母)吸收处理。
a.水 b.浓硫酸 c.NaOH溶液 d.饱和NaCl溶液
(3)步骤③中发生的主要反应的离子方程式为______________________________。
(4)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C中反应生成了NaBr、NaBrO3等,该反应的化学方程式为___________________________________。
(5)与B装置相比,采用C装置的优点为________________,__________________________。
高三化学实验题简单题查看答案及解析
-
某化学兴趣小组的同学利用如图所示实验装置进行某些气体的制备、物质性质的探究等实验(图中夹持装置省略)。
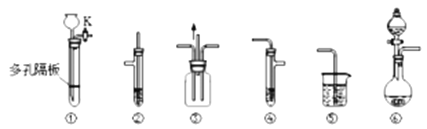
请按要求填空:
(1)实验室制取SO2气体时,可选择的合适试剂___(选填编号)。
a.15%的H2SO4溶液 b.75%的H2SO4溶液 c.Na2SO3固体 d.CaSO3固体
相应的制取装置是___(填图中装置下方编号)。
(2)实验室若用装置①来制取H2S气体,可选择的固体反应物是___(选填编号)。
a.Na2S固体 b.CuS固体 c.FeS固体 d.FeS2固体
反应的离子方程式为___。
(3)如何检验装置①的气密性?简述其操作:___。
(4)实验室里可用浓硫酸和无水酒精反应制取乙烯,除了题中的仪器外,制取装置中还缺少的玻璃仪器是___。
(5)该化学兴趣小组为探究制备乙烯是否存在副产物SO2和CO2,制备的气体从发生装置出来除去乙烯后依次选择了装置②、④、⑤,其中装置②盛有的试剂是___,装置④盛有的试剂是___。
高三化学实验题简单题查看答案及解析
-
二氧化氯(ClO2)是一种高效消毒剂,易溶于水,沸点为11.0℃,极易爆炸。在干燥空气稀释条件下,用干燥的氯气与固体亚氯酸钠制备二氧化氯,装置如图:
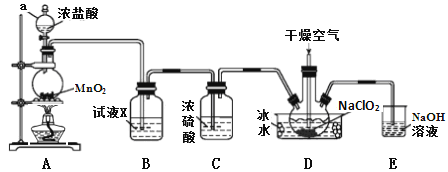
(1)仪器a的名称为_____________,装置A中反应的离子方程式为_______________。
(2)试剂X是_______________________。
(3)装置D中冰水的主要作用是___________。装置D内发生反应的化学方程式为_______________。
(4)装置E中主要反应的离子方程式为:____________________________。
(5)已知NaClO2饱和溶液在不同温度时析出的晶体情况如下表。
温度
<38℃
38℃~60℃
>60℃
析出晶体
NaClO2·3H2O
NaClO2
分解成NaClO3和NaCl
利用NaClO2溶液制得NaClO2晶体的操作步骤: 55℃蒸发结晶、_________、38~60℃的温水洗涤、低于60℃干燥。
(6)工业上也常用以下方法制备ClO2。
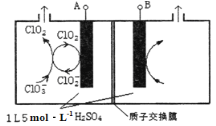
①酸性条件下双氧水与NaClO3反应,则反应的离子方程式为_______________________。
②如图所示为直接电解氯酸钠、自动催化循环制备高纯ClO2的实验。则阴极电极反应式为____________。
高三化学实验题简单题查看答案及解析