-
某种矿石中铁元素以氧化物FemOn形式存在,现进行如下实验:将少量铁矿石样品粉碎,称取25.0 g样品于烧杯中,加入稀硫酸充分溶解,并不断加热、搅拌,滤去不溶物。向所得滤液中加入10.0 g铜粉充分反应后过滤、洗涤、干燥得剩余固体3.6 g。剩下滤液用浓度为2 mol·L-1的酸性KMnO4滴定,至终点时消耗KMnO4溶液体积为25.0 mL。(提示:2Fe3++Cu=2Fe2++Cu2+,8H++MnO4-+5Fe2+=Mn2++5Fe3++4H2O。)
(1)计算该铁矿石中铁元素的质量分数。_____
(2)计算氧化物FemOn的化学式(m、n为正整数)。_______
高三化学计算题困难题查看答案及解析
-
回答以下问题:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是__________________________。
(2)另称取已去除表面氧化物的铁钉(碳素钢)6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。写出生成Fe2+所有可能的离子方程式:______________。
②乙同学取336mL(标准状况)气体Y通入足量氯水中,发生反应的化学方程式为:______________。
然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中SO2的体积分数为___________。
(3)向100mL水中投入Na和Al共16克,充分反应后剩余金属1g。计算放出H2的体积为________升(标准状况下)
(4)向含有0.3mol NaAlO2的溶液中滴加1mol/L HCl,当生成7.8克沉淀时,加入盐酸的体积为________mL
(5)向一定量的Fe、Fe2O3和CuO混合物投入120 ml 2.2 mol/L的硫酸溶液中,充分反应后生成896 mL标准状况下的气体,得不溶物1.28 g,过滤后,向滤液中加入2 mol/L的NaOH溶液,加至40 mL时开始出现沉淀,则滤液中FeSO4的物质的量浓度为(设滤液体积为120 ml)_________mol/L
高三化学计算题困难题查看答案及解析
-
有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。
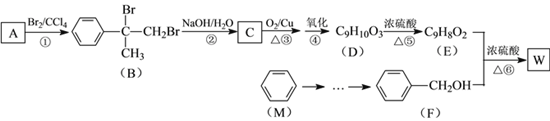
已知:
+CH3Cl
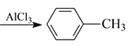 +HCl
+HCl请回答下列问题:
(1)F的化学名称是__,②的反应类型是___。
(2)D中含有的官能团是__(写名称),D聚合生成高分子化合物的结构简式为___。
(3)反应③的化学方程式是___。
(4)反应⑥的化学方程式是___。
(5)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为___。
(6)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线(无机试剂任选)___。
[示例:CH3CH2OH
CH2=CH2
BrCH2CH2Br]
高三化学计算题困难题查看答案及解析
-
人们利用焦炭制取水煤气的上艺已广泛用于工业生产中。
I.以焦炭制各水煤气
已知:①C(s)+H2O (g)=CO(g)+H2(g)
H= +130.0KJ/mol
②CO2 (g)+H2(g)=CO(g)+H2O(g)
H= +40.0KJ/mol
(1) 在工业上,反应①是煤的综合利用的一种途径,其名称是______。 焦炭与水蒸气反应生成二氧化碳和氢气的热化学方程式为_____ 。
I I •焦炭废气的再利用
500°C时,在密闭容器中将焦炭废气中的CO2转化为二甲醚,其相关反应为:
主反应:2CO2 (g)+6H2(g)
 CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)副反应:CO2 (g)+3H2(g)
 CH3OH(g)+2H2O(g)
CH3OH(g)+2H2O(g)(2)测得不同时间段部分物质的浓度如下表:
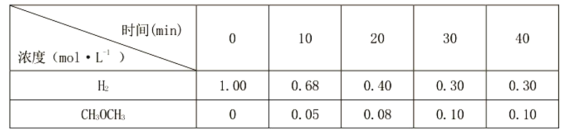
①10〜20 m in内,CH3OCH3的平均反应速率V(CH3OCH3)=__________。 ② 在上述特定条件下,己知主反应的速率方程为v=kca(CO2)×cb(H2)/cm(CH3OCH3) (k 为速率常数,a、 b、m均大于0 ) , 下列措施一定能提高主反应的反应速率的是______ (填字母序号)。
A . 适当温度 B .分离出二甲醚
C . 恒压减小c(CO2)/c(H2) D . 恒容下增大c(CO2)
②提高CH3OCH3产率的关键的因素是选用合适的催化剂,其原因是______ 。 若起始时CO2 和H2的浓度比为1:3,根据以上数据计算,上述主反应的平衡常数的计算表达式K= ______
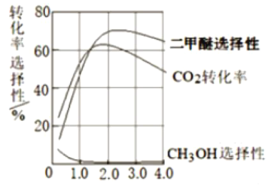
(3)对该反应实验研究得出:在相同温度下,CO2的转化率等物理量随催化剂的组成比的变化关系如图所示。若温度不变,催化剂中n(Mn)/n(Cu)约是______ 时最有利于二甲瞇的合成,此时,若增大反应投料比n(H2)/n(CO2),平衡常数K将____ (填 “增大”、“减小”或 “不变”).
高三化学计算题困难题查看答案及解析
-
肉桂酸甲酯在医药工业中可作为有机合成的中间体,其中一种合成路线如下:
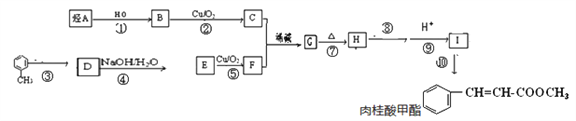
已知:①烃A是最简单的烯烃
②醛与醛能在一定条件下反应,原理如下:
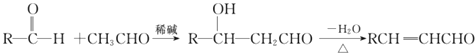
回答下列问题:
(1)烃A的结构简式为____________。
(2)反应③的试剂和反应条件为___________;反应⑩的试剂和反应条件为______________;反应⑧的反应试剂______________(填“能”或“不能”)改用酸性高锰酸钾溶液,其原因是___________________。
(3)反应⑦的反应类型为______。
(4)H与银氨溶液反应的化学方程式为______________________。
(5)符合下列条件的I的同分异构体共有______种。
①除苯环外不含有其他环状结构;②能发生水解反应和银镜反应。
其中核磁共振氢谱显示为5组峰,且峰面积比为1:1:2:2:2的是______(写结构简式)
高三化学计算题困难题查看答案及解析
-
有未知浓度的Ba(OH)2和NaOH混合溶液,量取四份该溶液分别通入等量的CO2(已折算成标准状况下的体积,不考虑CO2在水中的溶解),生成沉淀的物质的量如下表:
实验序号
Ⅰ
Ⅱ
Ⅲ
Ⅳ
CO2体积(mL)
2352
2352
2352
2352
样品体积(mL)
20.0
30.0
40.0
50.0
沉淀物质的量(×10-2 mol)
1.50
4.50
6.00
7.50
(1)该混合溶液中Ba(OH)2的物质的量浓度为_____________________。
(2)实验Ⅲ 最后所得溶液中碳酸钠的物质的量为________________。
高三化学计算题困难题查看答案及解析
-
32g铜与150mL一定浓度的硝酸恰好完全反应,产生的NO2和NO混合气体在标准状况下的体积为11.2L.请回答:(不要求写计算过程)
(1)写出铜与稀硝酸反应的化学方程式________________。
(2)NO为_________ mol.标准状况V(NO):V(NO2)=________
(3)原硝酸溶液的浓度为__________ mol•L-1 。
(4)试描述实验过程中试管内产生气体现象___________________________
高三化学计算题困难题查看答案及解析
-
湿法炼锌产生的黄铵铁矾[(NH4)xFey(SO4)z(OH)w]渣的综合利用具有广泛前景。
(1)黄铵铁矾高温下分解可得到一种红棕色固体,该红棕色固体的化学式为______________。
(2)在酸性媒介中,黄铵铁矾对H2O2氧化去除水溶液中的MB(对亚甲基蓝)有催化作用。反应温度高于80℃时MB的去除率下降,其原因可能是__________________________________。
(3)为测定某黄铵铁矾样品的组成,进行下列实验:
① 取一定量黄铵铁矾样品,将其溶于少量稀盐酸中,再加水稀释至250.00 mL,得到溶液A。
② 取25.00 mL溶液A,加足量的NaOH溶液并充分加热,生成NH3 224mL(标准状况),将产生的沉淀过滤、洗涤,滤液合并后加入足量的BaCl2溶液,生成白色沉淀4.66 g。
③ 另取25.00 mL溶液A,用SnCl2将Fe3+还原为Fe2+,再用HgCl2除去过量的SnCl2,最后用0.2000 mol·L-1 K2Cr2O7标准溶液滴定至终点(Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O),消耗标准溶液25.00 mL。通过计算确定该样品的化学式(写出计算过程)。_______________
高三化学计算题困难题查看答案及解析
-
分别取等物质的量浓度的氢氧化钠溶液各
,再通入一定量的
,随后分别各取
溶液,向其中逐滴滴入
的盐酸,在标准状况下产生
的体积(y轴)与所加入盐酸的体积(x轴)的关系如图(分A、B两种情况):
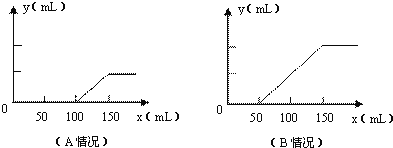
(1)在A情况下,溶质是(填化学式)_____________________ ,其物质的量之比为______________
(2)在B情况下,溶质是(填化学式)____________________其物质的量之比为______________
(3)原氢氧化钠溶液的物质的量浓度 _____________________
高三化学计算题困难题查看答案及解析
-
向一定体积 CaCl2 和 HCl 的混合溶液中逐滴加入浓度为 1.00mol·L-1的 Na2CO3溶液,反应过程中加入的 Na2CO3 溶液的体积与产生沉淀或气体的质量关系如图所示。
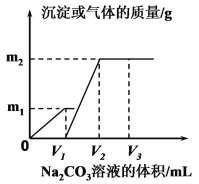
已知:图中 V1 :V2=1:2,当加入 V2mL Na2CO3溶液时,所得溶液的浓度为 1.00 mol·L-1,体积为 200mL。求:
(1)混合溶液中 CaCl2和 HCl 物质的量之比n(CaCl2)∶n(HCl)=_______(2)m2=______g。
高三化学计算题困难题查看答案及解析