-
端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
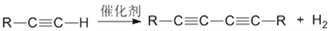
该反应在研究新型发光材料、超分子化学等方面具有重要价值。如图是用利用Glaser反应制备化合物E的一种合成路线:
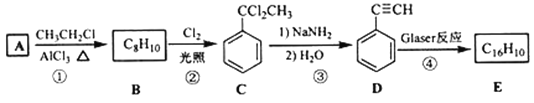
回答下列问题:
(1)B的化学名称为______________________________。
(2)③的反应类型为_________________________________。
(3)E的结构简式为__________________________________________________。用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气________________________________mol。
(4)化合物(
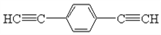 )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中2种的结构简式_______________________________________________________________。
高三化学简答题中等难度题查看答案及解析
-
炼锌厂的铜镉废渣中含有铜、锌、镉、铁、砷等元素,其含量依次减少。对这些元素进行提取分离能减少环境污染,同时制得ZnSO4‧7H2O实现资源的再利用。其流程图如下。已知FeAsO4难溶于水;ZnSO4‧7H2O易溶于水,难溶于乙醇。

金属离子
Fe3+
Zn2+
Mn2+
Cu2+
Cd2+
开始沉淀pH
2.7
6.5
7.7
5.2
6.9
沉淀完全pH
3.2
8.0
9.8
6.4
9.4
请回答下列问题:
(1)提高浸出率可以采用的方法是(写出其中一点即可)______________。
(2)滤液I中有少量的AsO33-,AsO33-与Cd反应会产生一种有毒氢化物气体,该气体的分子式为_________。向滤液I中滴入酸性KMnO4溶液可发生如下反应,完成该反应的离子方程式:____ Fe2++ ___ AsO33-+___MnO4-+ ___□= ___Mn 2++___FeAsO4↓+___□,
_________________________,判断该滴定终点的现象是_____________________________________ 。
(3)流程中②调节pH时可以选用的试剂为__________,滤渣Ⅱ的主要成份为________。
(4)制得的ZnSO4‧7H2O需洗涤,洗涤晶体时可选用试剂为(________)。
A.水 B.乙醇 C. 饱和硫酸锌溶液 D.稀硫酸
高三化学简答题中等难度题查看答案及解析
-
已知某混合物含有A单质与化合物B,在一定条件下可按图所示发生转化。
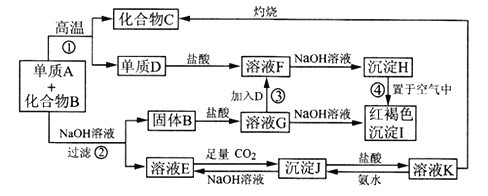
(1)沉淀H变沉淀I的化学方程式_____________________________。
(2)反应②的化学方程式_____________________________。
(3)溶液E中通入过量二氧化碳的离子方程式_______________________________。
(4)用化学反应方程式和简洁的语言解释图中溶液K制取化合物C的过程: __________。
(5)若要保存F溶液,应向溶液中加入两种物质为:_________、________(填化学式)。
高三化学简答题中等难度题查看答案及解析
-
化合物H是合成植物生长调节剂赤霉酸的重要中间体,其合成路线如下:
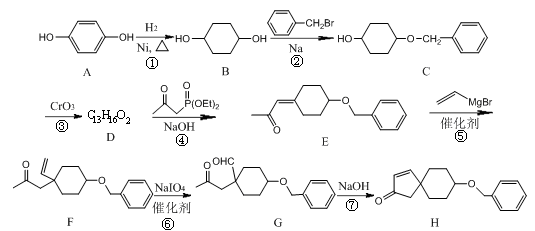
(1)化合物E的含氧官能团为______和______(填官能团的名称)。
(2)反应②的类型为__________。
(3)写出一种满足下列条件的C的同分异构体的结构简式____________。
I.分子含有1个苯环;
II.能发生银镜反应和水解反应;
III.分子有4种不同化学环境的氢。
(4)化合物C被氧化生成化合物D,D的结构简式为_______________。
(5)根据已有知识并结合相关信息,写出以
为有机原料制备
的合成路线流程图(无机试剂任用,可选择适当有机溶剂,合成路线流程图示例见本题题干)___________________。
高三化学简答题中等难度题查看答案及解析
-
合成氨的流程示意图如下:
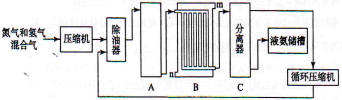
回答下列问题:
(1)工业合成氨的原料是氮气和氢气。氮气是从空气中分离出来的,通常使用的两种分离方法是 , ;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学反应方程式 , ;
(2)设备A中含有电加热器,触媒和热交换器,设备A的名称是 ,其中发生的化学反应方程式为 ;
(3)设备B的名称是 ,其中m和n是两个通水口,入水口是 (填“m”或“n”)。不宜从相反方向通水的原因是 ;
(4)设备C的作用是 ;
(5)在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过以下反应来实现:
CO(g)+H2O(g)
CO2(g)+H2(g)
已知1000K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中的c(H2O):c(CO)不低于 。
高三化学简答题中等难度题查看答案及解析
-
铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域。回答下列问题:
(1)铜原子基态电子排布式为 ;
(2)用晶体的x射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.00g·cm-3,则铜晶胞的体积是
cm3、晶胞的质量是 g,阿伏加德罗常数为 (列式计算,己知Ar(Cu)=63.6);
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为 。已知其中一种化合物的化学式为KCuCl3,另一种的化学式为 ;
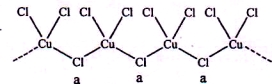
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是 ,反应的化学方应程式为 。
高三化学简答题中等难度题查看答案及解析
-
碳及其化合物在生活、化工领域发挥着重要的作用。试回答下列问题:
(1)有科学家提出由CO2制取C的太阳能工艺如图所示。若重整系统发生的反应中
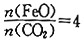 ,则重整系统中发生反应的化学方程式为______________。
,则重整系统中发生反应的化学方程式为______________。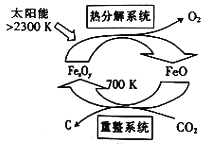
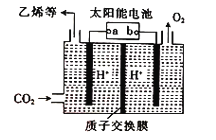
(2)以CO2为原料利用电解法可制取乙烯,其装置如图所示。电极a为电源的_____(填正极”或“负极” ),溶液中的H+由_______(填“阴”或“阳”,下同)极区流向____极区。
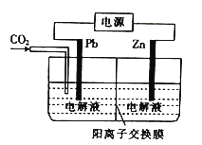
(3)草酸锌可应用于有机合成、电子工业等。工业上制取ZnC2O4的原理如图所示(电解液不参加反应),Zn电极是________(填“正” “负”“阴”或“阳”)极。己知在Pb电极区得到ZnC2O4,则Pb电极上的电极反应式为_________________。
高三化学简答题中等难度题查看答案及解析
-
NH3、N2H4在工业生产和国防建设中都有广泛应用。回答下列问题:
(1)①N2H4 (g)
N2(g)+2H2(g) △H1
②N2(g)+3H2(g)
2NH3(g) △H2
③7N2H4(g)
8NH3(g)+3N2(g)+2H2(g) △H3
△H3=___________(用含△H1和△H2的代数式表示)。
(2)纳米钴的催化作用下,N2H4可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。当反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图所示。
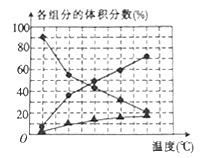
该反应的△H________(填“>”或“<”)0,N2H4发生分解反应的化学方程式为___________。
(3)T℃时,向一体积为5L 的恒容密闭容器中充入总物质的量为2 mol的CO2和NH3,在一定条件下发生反应:2NH3(g)+CO2(g)====CO(NH2)2(s)+H2O(g)。混合气体中氨气的体积分数随反应时间的变化如图所示。
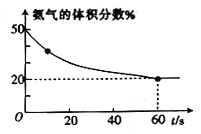
① 0~60s内,反应速率v(CO2)=________mol/(L·s)
② T℃时,该反应的化学平衡常数K=________。
高三化学简答题中等难度题查看答案及解析
-
煤气中主要的含硫杂质有H2S以及COS(有机硫),煤气燃烧后含硫杂质会转化成SO2从而引起大气污染。煤气中H2S的脱除程度已成为其洁净度的一个重要指标。回答下列问题:
(1)将H2S通入FeCl3溶液中,该反应的还原产物为___________。
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为_____________。
②Br2的KOH溶液将COS氧化为硫酸盐和碳酸盐的离子方程式为_____________。
③已知断裂1mol化学键所需的能量如下:
化学键
H—H
C═O
C═S
H—S
C≡O
E/kJ•mol-1
436
745
577
339
1072
H2还原COS发生的反应为H2(g)+COS(g) ═H2S(g)+CO(g),该反应的ΔH=________kJ·mol-1。
④用活性α—Al2O3催化COS水解的反应为COS(g)+ H2 O(g)
CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与
的关系如图2所示。
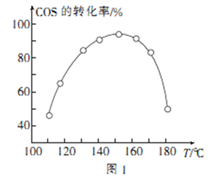
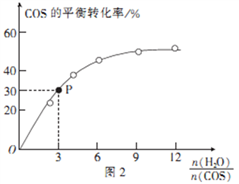
由图1可知,催化剂活性最大时对应的温度约为____________;由图2可知,P点时平衡常数K=_____
(保留2位有效数字)。
(3)常温下可发生反应:ZnS(s)+2H+(aq)
Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=_______[已知:Ksp(ZnS)=2.93×10-25;H2S电离常数;Ka1=9.5×10-8,Ka2=1.3×10-14]。
高三化学简答题中等难度题查看答案及解析
-
碳和碳的化合物广泛的存
在于我们的生活中。
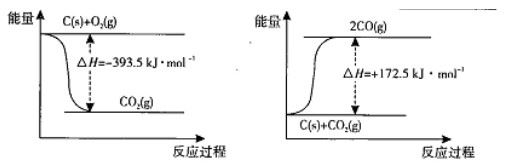
(1)根据下列反应的能量变化示意图,2C(s)+O2(g) =2CO(g) △H= ________________________________________________。
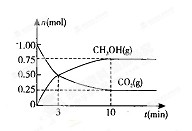
(2)在体积为2L的密闭容器中,充人1 mol CO2和3mol H2,一定
条件下发生反应:
CO2(g)+3H2(g)
CH3OH(g)+H2O(g) △H
测得CO2(g)和CH3OH(g)的物质的量随时间变化的曲线如右图所示:
①从反应开始到平衡,H2O的平均反应速率v(H2O)= ________________________________________________________________________________________________ 。
②下列措施中能使化学平衡向正反应方向移动的是 ________________________________________________________________(填编号)。
A.升高温度 B.将CH3OH(g)及时液化移出
C.选择高效催化剂 D.再充入l mol CO2和4 mol H2
(3) CO2溶于水生成碳酸。已知下列数据:
弱电解质
H2CO3
NH3.H2O
电离平衡常数( 25℃)
Ka1=
4.30 × 10一7
Ka2= 5.61× 10一11
Kb = 1.77× 10一5
现有常温下1 mol·L-1的( NH4)2CO3溶液,已知:NH4+水解的平衡常数Kh=Kw/Kb,
CO32-第一步水解的平衡常数Kh=Kw/Ka2。
①判断该溶液呈 ________________________________________(填“酸”、“中”、 “碱”)性,写出该溶液中CO32-
发生第一步水解的离子方程式________________________________________________________________________________________________________________ 。
②下列粒子之间的关系式,其中正确的是 。
A.c(NH4+)>c(HCO3-)> c(CO32-)>(NH4+)
B.c(NH4+)+c(H+)= c(HCO3-)+c(OH-)+ c(CO32-)
C. c(CO32-)+ c(HCO3-)+c(H2CO3)=1mol/L
D. c(NH4+)+ c(NH3.H2O)=2 c(CO32-)+ 2c(HCO3-) +2c(H2CO3)
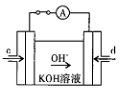
(4)据报道,科学家在实验室已研制出在燃料电池的反应容器中,利用特
殊电极材料以CO和O2为原料做成电池。原理如图所示:通入CO的管口是________________________________ (填“c”或“d”),写出该电极的电极反应式:________________________________________________________________________ 。
高三化学简答题中等难度题查看答案及解析