-
根据下列化合物:①Na2CO3;②NaHC03;③ HCl;④NH4Cl;⑤ CH3COONa;⑥CH3COOH;⑦NH3·H2O。回答下列问题
(l)常温下,将0.1mol/LHCl和0.1mol/L NH3·H2O等体积混合后溶液的pH____7(填“<”“>”或“=”)。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=_____;在pH=3的CH3COOH溶液中,水电离出来的c(H+)与酸电离出的c(H+)之比等于_______。
(3)已知纯水中存在如下平衡:H2O+H2O====H3O++OH- △H>0 ,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是__(填序号)。
A.向水中加入NaHSO4固体
B.向水中加入(NH4)2SO4固体
C.加热至100℃ [其中c(H+)=1×10-6mol/L]
D.向水中加入Na2CO3固体
(4)将①和②等浓度、等体积混合后溶液中各离子浓度由大到小的顺序为_________。
II.(l)用惰性电极电解80℃无隔膜热的氯化钠水溶液,电解后最终得到NaClO3溶液,写出该电解池中发生的总反应方程式:_____________;当温度低于80℃时,会有部分NaClO生成,若NaCl、NaClO、NaClO3的混合物中氯元素的质量分数为50%,则混合物中氧元素的质量分数为__________。
(2)写出电解NaClO3生成NaClO4时的阳极反应式:___________。
高三化学简答题困难题查看答案及解析
-
查尔酮是一种重要的化工原料,可以通过如下过程合成。请回答下列有关问题:
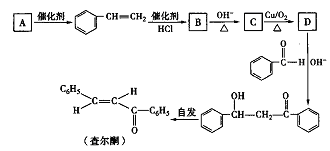
(1)已知A的分子式为C8H10,它的结构简式为_______。查尔酮的结构属于烯烃的_____ (填“顺式”或“反式”)异构。
(2) B转化成C的反应类刑属于________;C分子中含氧官能团为______。
(3)D物质在OH-存在时与苯甲醛反应的化学方程式为___________。
(4) D的同分异构体中,属于芳香醛的有_____种;其中核磁共振氢谱吸收峰种类最少的一种同分异构体的名称为________。
(5)参照上述合成路线,写出由CH3CH=CH2制取丙酮的流程图:____________。
高三化学简答题困难题查看答案及解析
-
砷化稼(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)基态Ga原子的核外电子排布式为[Ar]_______________。
(2)根据元素周期律,元素的电负性Ga______(填“大于”或“小于”, 下同)As,第一电离能B ____ Ga;BF3和NH3的分子能够通过配位键相结合的原因是_______。
(3)杀虫剂Na3AsO4中阴离子的空问构型为______,As原子采取________杂化。
(4)组成相似的GaF3和GaCl3晶体,前者属于离子晶体,后者属于分子晶体。从F-和Cl-结构的不同分析其原因是____________。
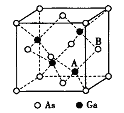
(5)原子晶体GaAs的晶胞参数a=xpm,它的晶胞结构如下图所示。该晶胞内部存在的共价健数为______;A原子距离B原子所在六面体的侧面的最短距离为______ (用x表示)pm ;该晶胞的密度为_____g·cm-3。(阿伏伽德罗常数用NA表示)。
高三化学简答题中等难度题查看答案及解析
-
无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如下图所示(夹持仪器略去)。主要步骤如下:
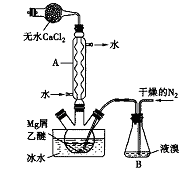
步骤l:三颈瓶中装入10g镁屑和150mL无水乙醚,装置B中加入适量的液溴。
步骤2:缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3:反应完毕后恢复至室温,过滤,将滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4:常温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性。
②MgBr2+3C2H5OC2H5= MgBr2·3C2H5OC2H5
请回答:
(1)仪器A的名称是___________,它在实验中的作用是____________。
(2)步骡2中,可以将B装置中的溴完全导入三颈瓶中的原因是_______;该实验如果将所用液溴一次性全部加入三颈瓶中,其后果是_____________。
(3)步骡3中,第一次过滤得到的固体物质是______;根据步骤3、4,请总结出三乙醚合溴化镁所具有的物理性质:_________。
(4)请根据Mg的性质设计实验证明O2的氧化性比N2的强:________。
(5)将步骤得到的产品在干燥器中冷却到室温后,称量,其质量为61.4g。则该实验制取MgBr2的产率是_____________。
高三化学简答题中等难度题查看答案及解析
-
消除氮氧化物污染对优化空气质境至关重要。
(1)用CH4催化还原氮氧化物消除氮氧化物的污染发生的反应如下:
CH4(g)+4NO2(g)
4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+4NO2(g)
2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ/mol
若用0.2molCH4将NO2还原为N2,则整个过程中放出的热量为________kJ。(假设水全部以气态形式存在)
(2)用活性炭可处理大气污染物NO。在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F。当沮度分别在T1和T2时.测得反应达到平衡时各物质物质的量如下表;
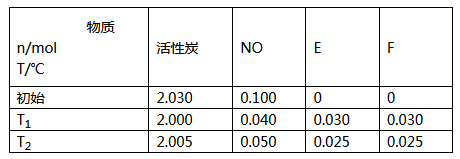
①请结合上表数据.写出NO与活性炭反应的化学方程式_______________。
②T1℃ 时,上述反应的平衡常数的值为________。如果已知T2>T1,则该反应正反应的△H___(填“>”“<”或“=”)0
③ 在T1温度下反应达到平衡后,下列措施不能增大NO转化率的是_______。
a.降低温度 b.增大压强 c.增大c(NO) d.移去部分F
(3)汽车尾气处理中的反应有2NO+2CO
2CO2+N2。某温度时,在1L密闭容器中充入0.1molCO和0.1mol NO,5s时反应达到平衡,测得NO的浓度为0.02mol/L,则反应开始至平衡时,NO的平均反应速率v(NO)=________。若此温度下,某时刻测得CO、NO、N2、CO2的浓度分别为0.01mol/L、amol/L、0.01mol/L、0.04mol/L,要使反应向正反应方向进行,a的取值范围为_____________。
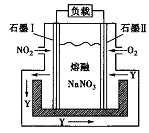
(4)某课题组利用下图所示装置,探究NO2和O2化合生成N2O5形成原电池的过程。物质Y的名称为_______,该电池的正极反应式应为___________。
高三化学简答题困难题查看答案及解析
-
PFS是水处理中重要的絮凝剂,下图是以回收的废铁屑为原料制备PFS的一种工艺流程。
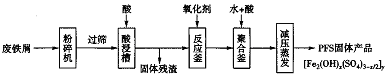
(1)酸浸槽以及聚合釜中用到的酸应是__________;PFS中铁元素的化合价为__________;在酸浸槽中,为了提高浸出率,可以采取的措施有_________(写两条)。
(2)若废铁属含有较多铁锈(Fe2O3·xH2O),则酸浸时反应的化学方程式有_____________。
(3)如果反应釜中用H2O2作氧化剂,则反应的离子方程式为________;生产过程中,发现反应釜中产生了大量的气体,且温度明显升高,其原因可能是___________。
(4)聚合釜中溶液的pH必须控制在一定的范围内。如果溶液酸性过强,造成的后果是________。如果溶液酸性太弱又会生成大量的氢氧化铁沉淀。若溶液中Fe3+的浓度为1mol·L-1,当Fe3+开始沉淀时,涪液的pH约为_________。[已知Fe(OH)3的Ksp≈1.0×10-39]。
高三化学简答题困难题查看答案及解析
-
黄酮醋酸(F)具有独特抗癌活性,它的合成路线如下:
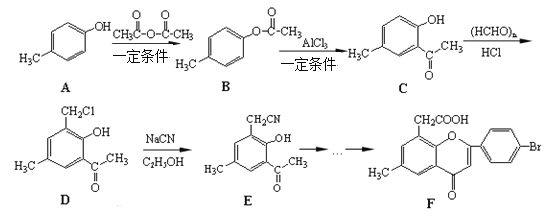
已知:RCN在酸性条件下发生水解反应: RCN
RCOOH
(1)上述路线中A转化为B的反应为取代反应,写出该反应的化学方程式________。
(2)F分子中有3种含氧官能团,名称分别为醚键、_____________和______________。
(3)E在酸性条件下水解的产物可通过缩聚反应生成高分子化合物,该高分子化合物的结构简式为_________________________。一定条件
(4)写出一种符合下列条件的D.的同分异构体的结构简式________________。
①分子中有4种化学环境不同的氢原子
②可发生水解反应,且一种水解产物含有酚羟基,另一种水解产物含有醛基。
(5)对羟基苯乙酸乙酯(
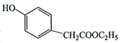 )是一种重要的医药中间体。写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选)。______________
)是一种重要的医药中间体。写出以A和乙醇为主要原料制备对羟基苯乙酸乙酯的合成路线流程图(无机试剂任选)。______________合成路线流程图请参考如下形式:

高三化学简答题中等难度题查看答案及解析
-
某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO4•7H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).
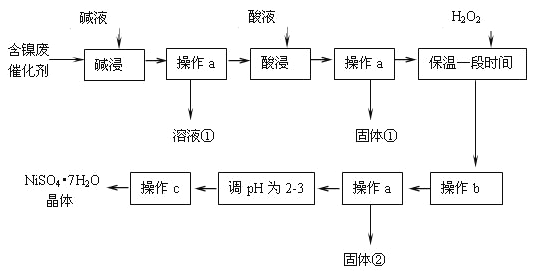
部分阳离子以氢氧化物形式沉淀时的pH如下:
沉淀物
开始沉淀时的pH
完全沉淀时的pH
Al(OH)3
3.8
5.2
Fe(OH)3
2.7
3.2
Fe(OH)2
7.6
9.7
Ni(OH)2
7.1
9.2
(1)操作a应选用下列哪种方法或装置:_____
A.
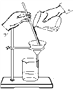 B.
B. C.
C.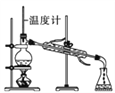 D.
D.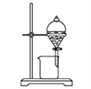
(2)“碱浸”过程中发生反应的离子方程式是________
(3)“酸浸”时所加入的酸是________(填化学式).
(4)加入H2O2时发生反应的离子方程式为________
(5)操作b为调节溶液的pH,你认为pH的调控范围是________
(6)产品晶体中有时会混有少量绿矾(FeSO4•7H2O),其原因可能是____(写出一点即可).
(7)NiSO4•7H2O可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为________.
高三化学简答题困难题查看答案及解析
-
作为目前发现的最薄、强度最大、导电导热性能最强的一种新型纳米材料,石墨烯被称为“黑金”,是“新材料之王”,科学家甚至预言石墨烯将“彻底改变21世纪”。极有可能掀起一场席卷全球的颠覆性新技术新产业革命。石墨烯一层层叠起来就是石墨,厚1毫米的石墨大约包含300万层石墨烯。英国曼彻斯特大学的两位科学家安德烈·盖姆(AnD.re Geim)和克斯特亚·诺沃消洛夫(Konstantin Novoselov)从高定向热解石墨中剥离出石墨片,然后将薄片的两面粘在一种特殊的胶带上,撕开胶带,就能把石墨片一分为二。不断地这样操作,于是薄片越来越薄,最后,他们得到了仅由一层碳原子构成的薄片,这就是石墨烯(如图)。
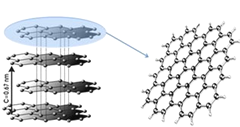
石墨 石墨稀
(1))石墨、金刚石、C60等互称为___________________;
(2)已知25℃,101KPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨) + O2(g) = CO2(g);△H=-393.51kJ.mol-1
C(金刚石) + O2(g) = CO2(g);△H=-395.41kJ.mol-1
C(金刚石)=C(石墨);△H =________kJ/mol
(3)石墨和金刚石相比,更稳定的是:________________;
(4)请用化学知识解释科学家为什么可以用特殊的胶带将石墨不断地粘撕得到石墨烯: _______________。
(5)12g石墨烯中含有___________NA个如图所示的六元环。
高三化学简答题中等难度题查看答案及解析
-
下图所示转化关系(部分物质未列出)中,A的焰色反应呈黄色,C、D、E是常见气体且C、D是单质。
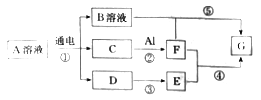
请回答下列问题:
(1)A的化学式为__________,电解时B在________极生成。
(2)工业上由D生成E的化学方程式为_____________。
(3)B溶液与G反应的离子方程式为_________________。
(4)上述转化中,属于非氧化还原反应的是__________(填数字代号)。
(5)取适量0.1mol/L 的F溶液,通入过量的E,现象是____________,充分反应后,所得溶液的pH=5.00,则此温度下残留在溶液中的c(Al3+)=________。[已知实验条件下Kap(G)=1.3×10-33]
高三化学简答题中等难度题查看答案及解析