-
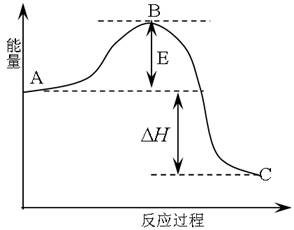
已知反应X + Y = M + N为吸热反应,对这个反应的下列说法中正确的是
A.X的能量一定低于M的,Y的能量一定低于N的
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
难度: 中等查看答案及解析
-
下列说法都正确的是
①江河入海口三角洲的形成通常与胶体的性质有关
②四川灾区重建使用了大量钢材,钢材是合金
③“钡餐”中使用的硫酸钡是弱电解质
④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤常用的自来水消毒剂有氯气和二氧化氯,两者都含有极性键
⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物
A.①②③④ B.①②④⑥ C.①②⑤⑥ D.③④⑤⑥
难度: 简单查看答案及解析
-
只含有一种元素的物质
A.可能是纯净物也可能是混合物 B.可能是单质也可能是化合物
C.一定是纯净物 D.一定是一种单质
难度: 简单查看答案及解析
-
下列各组物质中前一种是混合物,后两种是纯净物的是
A.蓝矾 玻璃 无色的刚玉 B.汽油 液氯 醋酸
C.石蜡 纯盐酸 王水 D.干冰 铝热剂 铁触媒
难度: 简单查看答案及解析
-
现有两种不含结晶水的盐,它们在不同温度下的溶解度分别是:
20℃
60℃
A的溶解度
35.7g
46.4g
B的溶解度
31.6g
110g
下列说法中,正确的是
A.两种盐在某一温度下具有相同的溶解度
B.若把110gB的饱和溶液从60℃降到20℃,析出的B是78.4g
C.在20℃时,A、B都可以配成25%的不饱和溶液
D.若要使A、B混合物分离,可采用重结晶法
难度: 简单查看答案及解析
-
下列关于氧化物的叙述正确的是
A.酸性氧化物均可跟碱起反应 B.酸性氧化物在常温常压下均为气态
C.金属氧化物都是碱性氧化物 D.不能跟酸反应的氧化物一定能跟碱反应
难度: 简单查看答案及解析
-
下列实验过程中产生的现象与对应的图形相符合的是
A.NaHSO3粉末加入HNO3溶液中 B.H2S气体通入氯水中
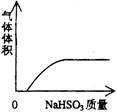
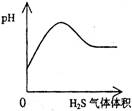
C.NaOH溶液滴入Ba(HCO3)2溶液中 D.CO2气体通入澄清石灰水中
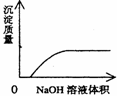

难度: 简单查看答案及解析
-
下列各组中的两种物质相互反应时,无论哪种过量,都可以用同一个离子方程式表示的是:①碳酸钠溶液与盐酸 ②偏铝酸钠溶液与盐酸 ③苯酚钠溶液与CO2 ④硝酸银溶液与氨水 ⑤氯化铝溶液与氨水 ⑥碳酸氢钠溶液与澄清的石灰水
A.③⑤ B.①③⑥ C.仅有⑤ D.②④
难度: 简单查看答案及解析
-
下列离子方程式正确的是
A.碳酸氢镁溶液和过量的NaOH溶液反应:Mg2++2OH-=Mg(OH)2↓
B.二氧化硫气体通入过量的Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.Ba(OH)2溶液中滴入NaHSO4至pH等于7:Ba2++OH-+H++SO42-=BaSO4↓+H2O
D.KHS的水解 HS-+H2O
H2S+OH-
难度: 简单查看答案及解析
-
某结晶水合物的化学式为A·xH2O,其相对分子质量为B。在60ºC时,mg该晶体溶于ng水中,制得VmL密度为dg·mL-1的饱和溶液。下列表示式或判断正确的是
A.该溶液的物质的量浓度为
B.该温度下A的溶解度为
C.将10gA投入到饱和溶液中,析出的晶体大于10g,且溶液质量减少,但浓度不变
D.该溶液的质量分数为
难度: 简单查看答案及解析
-
下列说法正确的是
①标况下,6.02×1023个分子所占的体积约是22.4 L ②0.5 mol H2所占体积为11.2 L ③标况下,1 mol H2O的体积为22.4 L ④标况下,28 g CO与N2的混合气体的体积约为22.4 L ⑤各种气体的气体摩尔体积都约为22.4 L·mol-1 ⑥标准状况下,体积相同的气体的分子数相同
A.①③⑤ B.④⑥ C.③④⑥ D.①④⑥
难度: 简单查看答案及解析
-
某不纯的烧碱样品,含Na2CO3 3.8%(质量百分含量)、H2O 5.8%、NaHCO3 0.004%。取m g样品溶于40 mL 2 mol·L-1的盐酸后,并用 2 mol·L-1 NaOH溶液中和剩余的酸,在蒸发后可得干燥的固体的质量为
A.4.68 g B.5.58 g C.2.34 g D.2.34 mg
难度: 简单查看答案及解析
-
在反应X+2Y﹦R+2M中,已知R和M的摩尔质量之比为22:9,当1.6gX与Y完全反应后,生成4.4gR,则在此反应中Y和M的质量比为
A.16:9 B.23:9 C.32:9 D.46:9
难度: 简单查看答案及解析
-
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。反应中镁和铝的

A.物质的量之比为3︰2 B.质量之比为3︰2
C.摩尔质量之比为2︰3 D.反应速率之比为2︰3
难度: 简单查看答案及解析
-
下列各组物质的燃烧热相等的是:
A.碳和一氧化碳 B.1moL碳和2moL碳
C.1moL乙炔和2moL碳 D.淀粉和纤维素
难度: 简单查看答案及解析
-
下列说法或表示方法中正确的是
A.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多
B.氢气的燃烧热为285.8 kJ·mol-1,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)====2H2O(l) ΔH=285.8 kJ·mol-1
C.Ba(OH)2·8H2O(s)+2NH4Cl(s) ====BaCl2(s)+2NH3(g)+10H2O(l) ΔH<0
D.已知中和热为57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量要大于57.3 kJ
难度: 简单查看答案及解析
-
在一种酸性溶液中可能存在Fe3+、NO3-、Cl-、I-中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推断溶液中
A.一定含有I-,不能确定是否含有Cl- B.可能含有NO3-、Cl-和I-
C.可能含有NO3- D.肯定含有Fe3+
难度: 简单查看答案及解析
-
质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为
A.大于2c mol/L B.等于2c mol/L
C.小于2c mol/L D.在c mol/L~2c mol/L之间
难度: 简单查看答案及解析
-
下列说法正确的是
A.一定温度下,1L0.5mol·L-1NH4Cl溶液与1L0.25mol·L-1NH4Cl溶液中NH4+ 物质的量之比为2:1
B.100g硫酸溶液的物质的量浓度为18.4mol/L,用水稀释到物质的量浓度为9.8mol/L,需要水100g.
C.标准状况下,22.4LCH3Cl和CHCl3的混合物中所含有的碳原子个数一定为NA
D.在2Na2O2+2CO2=2Na2CO3+O2反应中,每生成16g氧气,则转移NA个电子
难度: 简单查看答案及解析
-
下列关于某溶液所含离子检验的方法和结论正确的是
A.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,说明有Ca2+
B.通入少量Cl2后,溶液变为黄色,再加入淀粉溶液后,溶液变蓝,说明有I-
C.加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中一定有CO32-或SO32-
D.往溶液中加入BaCl2溶液和稀HNO3,有白色沉淀生成,说明一定有SO42-
难度: 简单查看答案及解析