-
下列有关物质的名称(或主要成分)与化学式,不相对应的是
A.火碱:NaOH B.硫酸铁:FeSO4
C.石英:SiO2 D.明矾:KAl(SO4)2·12H2O
难度: 中等查看答案及解析
-
在炼铁、制玻璃、制水泥三种工业生产中,都需要的原料是
A.纯碱 B.石灰石 C.石英 D.粘土
难度: 中等查看答案及解析
-
高岭土的组成可以表示为Al2Si2Ox(OH)y,其中x,y的数值分别为
A.7、2 B.5、4 C.6、3 D.6、4
难度: 中等查看答案及解析
-
为除去FeSO4溶液中的Fe2(SO4)3和CuSO4,最好选用
A.烧碱溶液 B.浓氨水 C.镁粉 D.铁粉
难度: 中等查看答案及解析
-
下列说法中,正确的是
A.水晶和陶瓷的主要成分都属于硅酸盐
B.单质硅是制造光导纤维的材料
C.硅酸钠是制备硅胶和木材防火剂的原料
D.SiO2是酸性氧化物,它不溶于水也水溶于任何酸
难度: 中等查看答案及解析
-
往AlCl3溶液中逐滴滴入NaOH溶液至过量,可观察到的现象是
A.有白色絮状沉淀产生,且不溶解
B.先有白色絮状沉淀,后又溶解
C.一直无明显现象
D.先无现象,后有白色絮状沉淀
难度: 中等查看答案及解析
-
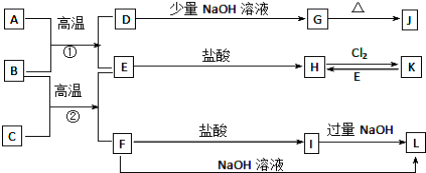
下列物质既可以通过金属与氯气反应制得,又可以通过金属与稀盐酸反应制得
A.FeCl2 B.FeCl3 C.CuCl2 D.AlCl3
难度: 中等查看答案及解析
-
,在以Al2O3为原料制备Al(OH)3时,X适宜用的试剂是
A.NH3 B.CO2 C.NaOH D.HCl
难度: 简单查看答案及解析
-
除去SO2中混有的HC1气体,可选用的试剂是
A.石灰水 B.浓硫酸
C.饱和NaHSO3溶液 D.饱和Na2SO3溶液
难度: 中等查看答案及解析
-
两份等质量的铝粉,一份投入足量的稀盐酸中,另一份投入足量的氢氧化钠溶液中,则生成氢气的质量比为
A.2:3 B.3:2 C.36.5:40 D.1:1
难度: 中等查看答案及解析
-
广州亚运会开幕式上的礼花,让广州显得更加辉煌、浪漫。其中镁粉可用来制造焰火,工业上制取镁粉的方法是将镁的蒸气进行冷却,其中最适宜的方法是
A.在氮气的容器内冷却 B.在水中冷却
C.在氦气的环境里冷却 D.在二氧化碳气体里冷却
难度: 中等查看答案及解析
-
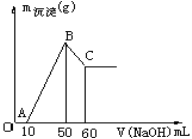
取含有 0.02 mol 的硫酸溶液,先投入0.24 g 镁粉,再滴入NaOH 溶液,当使溶液中的镁离子全部转化为沉淀时, 需要NaOH的物质的量为
A.0.02 mol B.0.03 mol C.0.04 mol D.0.01 mol
难度: 中等查看答案及解析
-
只用一种试剂鉴别硫酸钠、硫酸镁、硫酸铝、硫酸铵四种溶液,这种试剂是
A.氨水 B.硝酸银溶液 C.氢氧化钠 D.盐酸
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A.铁与盐酸反应:Fe+2H+ = Fe3++ H2↑
B.氢氧化钡溶液和稀硫酸反应:Ba2++ SO42-= BaSO4↓
C.氯化铝中加入过量的氨水:Al3++4NH3·H2O= AlO+4NH4++2H2O
D.向水玻璃中加盐酸:SiO32-+2H+ = H2SiO3↓
难度: 中等查看答案及解析
-
在某无色酸性溶液中能大量共存的一组离子是
A.NH4+、SO42- 、Al3+、NO3- B.Na+、K+、HCO3-、NO3-
C.Na+ 、Ca2+ 、NO3- 、CO32- D.K+、Cu2+、NH4+、NO3-
难度: 中等查看答案及解析
-
向盛有氯化铁溶液的烧杯中加入过量的铜粉,反应结束后,溶液中大量存在的金属离子是
A.Fe2+、Fe3+ B.Fe2+、Cu2+
C.Fe3+、Cu2+ D.Cu+、Cu2+
难度: 中等查看答案及解析
-
将下列四种铁的化合物溶于稀盐酸,滴加硫氰化钾溶液没有颜色变化,再加入氯水即呈红色的是
A.FeS B.Fe2O3 C.FeCl3 D.Fe2(SO4)3
难度: 中等查看答案及解析
-
下列物质中既能与稀H2SO4反应, 又能与NaOH溶液反应的是
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3
A.③④ B.①②③④ C.②③④ D.全部
难度: 中等查看答案及解析
-
某无色溶液中,含有H+、Mg2+、Al3+等阳离子,向溶液中逐滴加入NaOH溶液,则消耗NaOH溶液的体积(x)和生成沉淀的质量(y)之间的函数关系可用如图表示,其中正确的是

难度: 中等查看答案及解析
-
下列有关二氧化硫的说法中,错误的是
A.二氧化硫能漂白某些物质,说明它具有氧化性
B.二氧化硫的水溶液能使紫色石蕊溶液变红,说明它能与水反应生成H2SO3
C.将足量二氧化硫通入酸性高锰酸钾溶液中,溶液褪色,说明二氧化硫具有还原性
D.实验室可用氢氧化钠溶液处理含有二氧化硫的尾气
难度: 中等查看答案及解析
-
下列实验装置与操作正确的是

难度: 中等查看答案及解析
-
由FeSO4和Fe2(SO4)3组成的混合物中,含硫为a%,则所含铁的质量百分含量为
A.3a% B.(100-2a)% C.20% D.1-3a%
难度: 中等查看答案及解析
-
将适量的铁粉加入FeCl3溶液中,充分反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的的Fe3+和未反应的Fe3+的物质的量之比为
A.2∶3 B.3∶2 C.1∶2 D.1∶1
难度: 中等查看答案及解析