-
中国诗词中常蕴含着一些自然科学知识,针对下列一些诗词,从化学角度解读正确的是
A. “落红不是无情物,化作春泥更护花”蕴藏着自然界中碳、氮的循环
B. “纷纷灿烂如星陨,赫赫喧豗似火攻”描述了显色反应的现象
C. “独忆飞絮鹅毛下,非复青丝马尾垂”中的“飞絮”与“马尾”化学成分相同
D. “日照香炉生紫烟,遥看瀑布挂前川”中的“紫烟”是碘的升华现象
难度: 简单查看答案及解析
-
某有机物M 分子的模型如图所示,其中不同颜色的球表示不同的原子,其中原子之间的化学键可以是单键、双键或叁键。关于该有机物M的说法正确的是
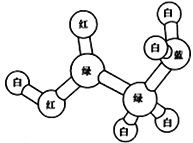
A. 难溶于水,易溶解于烧碱溶液
B. 同一平面上最多有6个原子
C. 含有不饱和键,可以发生加聚反应生成高分子化合物
D. 分子中含有两种官能团
难度: 中等查看答案及解析
-
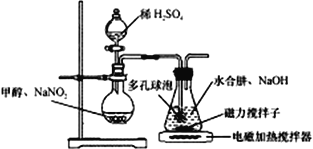
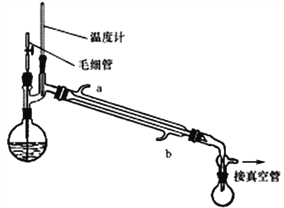
下面装置是用于FeSO4受热分解及产品检验,已知亚硝酸铵受热易分解,下列相关说法正确的是
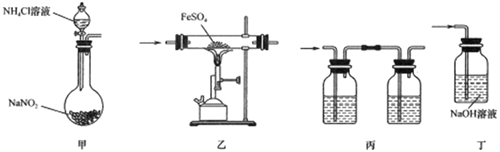
A. 装置甲是N2的制备装置,实验时采用酒精灯直接加热至85℃
B. 点燃装置乙处酒精喷灯前应先通入一段时间N2
C. 装置丙依次装入品红溶液,BaCl2溶液检验产生的气体
D. 采用装置丁,可更好地吸收尾气且避免了尾气外逸污染环境
难度: 中等查看答案及解析
-
我国科学家研制出“可充室温Na-CO2电池”(Rechargeable Room-Temperature Na-CO2 Batter-ies)现已取得突破性进展,其有望取代即将“枯竭”的锂电池,该电池结构如图所示。下列说法错误的是

A. 电池工作时,正极发生反应:4Na++3CO2+4e-==2Na2CO3+C
B. 电池工作时,外电路中流过0.02 mol电子,负极材料减重0.46 g
C. 多壁碳纳米管的作用主要是导电及吸附CO2
D. 电池中四甘醇二甲醚可用饱和食盐水代替实现Na+传导
难度: 中等查看答案及解析
-
NH4Al(SO4)2·12H2O俗称铵明矾,其性质稳定,是化学实验常用的基准试剂,借助碳酸氢铵与硫酸钠可以制备纯净的铵明矾,制备过程如下图,下面相关说法错误的是
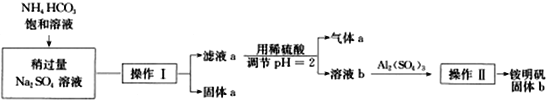
A. 为加快操作I的速率实验时采用抽滤,常用玻璃纤维替代滤纸
B. 操作I的基本过程为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
C. 使用NaOH 和BaCl2试剂可以检验铵明矾的三种离子
D. 若气体a通入到饱和的纯碱溶液中会有晶体析出,该晶体与固体a相同
难度: 中等查看答案及解析
-
W、X、Y、Z四种短周期元素,其原子序数依次增大,W 与X同周期且相邻,含有18电子的X与Z的氢化物可反应生成淡黄色固体,Y元素是地壳中含量最高的金属元素。下列说法正确的是
A. Y、Z元素的最高价氧化物对应的水化物可相互反应
B. 简单离子半径:r(W)<r(X)<r(Y)<r(Z)
C. W、Z的氧化物均为酸性氧化物
D. 简单氢化物的沸点:W<Z
难度: 中等查看答案及解析
-
25℃某二元碱B(OH)2水溶液中,B2+、B(OH)+和B(OH)2 三者各自的物质的量分数δ随溶液pH的变化曲线如图所示,下列说法错误的是(已知多元碱的电离是逐级进行的)
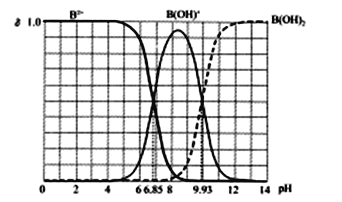
A. Kb2[B(OH)2] 的数量级为10-8
B. 在B(OH)Cl溶液中c(OH-)>c(H+)
C. 等物质的量的BCl2和B(OH)Cl混合溶液中δ(B2+)<δ[B(OH)+]
D. B(OH)Cl溶液中,若c[B(OH)2]+ 2c(B2+)+c(H+)-c(OH-),则δ[B(OH)2]=δ[B(OH)+]
难度: 困难查看答案及解析