-
下列说法错误的是 ( )
A. 硝酸铵溶于水溶液温度升高
B. 向固体中滴加稀盐酸有气泡产生,该固体不一定是碳酸盐
C. 用洗洁精洗去餐具上的油污属于乳化在日常生活中的应用
D. 配制6%的氯化钠溶液时仰视量筒刻度会使所配溶液溶质质量分数偏低
难度: 中等查看答案及解析
-
实施“清水蓝天”工程,保证社会的可持续发展。下列不利于此项工程实施的是
A. 分类回收垃圾 B. 使用太阳能路灯 C. 开发氢燃料电池客车 D. 直接排放生活污水
难度: 中等查看答案及解析
-
下列工艺中属于物理变化的是
A. 酿造米酒 B. 雕刻石像 C. 烧制陶瓷 D. 冶炼钢铁
难度: 中等查看答案及解析
-
下列物品所使用的材料中,不属于有机合成高分子材料的是
A. 尼龙绳子 B. 塑料水杯 C. 纯棉T裇 D. 篮球
难度: 中等查看答案及解析
-
下列各组物质按单质、氧化物、混合物的顺序排列的是
A. 氧气、生石灰、乙醇汽油 B. 氮气、氯酸钾、葡萄糖
C. 硫粉、碳铵、赤铁矿 D. 钢、干冰、液态空气
难度: 中等查看答案及解析
-
下列物质由原子直接构成的是
A. 氧气 B. 氩气 C. 氯化钠 D. 二氧化碳
难度: 简单查看答案及解析
-
下列实验操作错误的是

A. A B. B C. C D. D
难度: 中等查看答案及解析
-
防止垃圾污染环境,分类回收是关键,下图表示可回收标志是

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
物质性质决定用途,下列说法不正确的是
A. 甲醛能使蛋白质变性,可用于海鲜等水产品的防腐
B. 不锈钢具有较强的耐腐蚀性,可用于制作医疗器械
C. Ca(OH)2具有碱性,可用于改良酸性土壤
D. 食醋具有酸性,可除去玻璃水壶中的水垢
难度: 中等查看答案及解析
-
下列各组物质在水溶液中能够共存,而且加入酚酞溶液显红色的是
A. NaOH、CuSO4、H2SO4
B. NaCl、Na2SO4、NaOH
C. NaCl、Ba(NO3)2、HCl
D. NH4NO3、NaOH、Na2SO4
难度: 中等查看答案及解析
-
从植物中提取的秋水仙碱有润肺止咳功效,其化学式为C22H25NO6。下列说法正确的是
A. 秋水仙碱中氧元素的质量分数约为24% B. 秋水仙碱由54个原子构成
C. 秋水仙碱中碳、氢元素质量比为22∶25 D. 秋水仙碱属于有机高分子化合物
难度: 中等查看答案及解析
-
工业上利用黄铁矿(主要成分是FeS2)生产硫酸。同时还能得到一种副产品氧化铁用于炼铁,其反应原理为:①4FeS2+11O2
2Fe2O3+8SO2 ②2SO2+O2
2SO3 ③SO3+H2O=H2SO4 ④ Fe2O3+3CO
2Fe+3CO2
下列说法不正确的是
A. 反应①②④均有元素化合价发生变化 B. 四个反应的产物都有氧化物
C. 反应①④不属于四种基本反应类型中的任何一种 D. 反应②③属于化合反应
难度: 中等查看答案及解析
-
下图可表示一定条件下发生的某个化学反应,下列说法正确的

A. 该反应前后分子、原子个数都不变 B. 该反应中各物质都为化合物
C. 该反应不符合质量守恒定律 D. 该反应为置换反应
难度: 中等查看答案及解析
-
下列现象的描述正确的是
A. 磷在空气中燃烧产生大量白色烟雾 B. 碱式碳酸铜受热分解固体由黑色变成绿色
C. 铁丝在空气中燃烧时火星四射 D. 蚕丝和羊毛灼烧都产生烧焦羽毛的气味
难度: 中等查看答案及解析
-
向稀硫酸中加入铜粉,无气泡冒出,用导管向稀硫酸中通入空气并加热,铜粉逐渐减少,溶液由无色逐渐变为蓝色,测得溶液质量与试验时间的关系如图。下列说法错误的是

A. ab段说明Cu不能置换出硫酸中的氢
B. 从b点到c 点,溶液的pH逐渐增大
C. 从c点到d点,溶液中的溶质只能有一种
D. bc段反应为2Cu +O2 +2H2SO4
2CuSO4 + 2H2O
难度: 困难查看答案及解析
-
下列实验目的、操作、现象、结论都正确的是
选项
实验目的
实验操作
实验现象
实验结论
A
测溶液pH
用玻璃棒蘸取待测液滴在用蒸馏水润湿的pH试纸上
试纸变为浅红色
溶液pH为2
B
鉴别NaOH和NH4NO3
在装有等量水的试管中分别加入a、b固体
加a的试管水温升高,加b的试管水温降低
a是NaOH
b是NH4NO3
C
验证燃烧是否需要O2

前者不燃烧,后者燃烧
燃烧需要O2
D
比较Al、Cu的活泼性
将未经打磨的Al条放入CuSO4溶液中
无明显现象
活泼性Al<Cu
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
除去下列各组物质中的杂质,所用试剂和方法均正确的是
物 质
杂 质
除杂质所用试剂和方法
A
CO2气体
CO气体
先通入少量氧气,再点燃
B
NaOH溶液
Na2CO3溶液
先加入过量Ca(OH)2溶液,再过滤
C
KCl固体
KClO3固体
先加入少量MnO2,再加热
D
氢气
水蒸气
通过装有足量无水氯化钙的干燥管
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
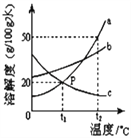
下图能正确反映其对应操作中各种量的变化关系的是

A. 在氢氧化钠溶液中加入一定量的稀盐酸,溶液pH的变化曲线
B. 将相同质量的Zn粉和Mg粉分别加入足量的稀盐酸中
C. 水的电解
D. 向盐酸和氯化铁混合溶液中加入过量的氢氧化钠溶液
难度: 困难查看答案及解析



 洁厕灵
洁厕灵