-
下列化学用语书写正确的是
A. 四氯化碳的电子式:
B. 2-丁烯的键线式:
C. 乙烯的结构简式: CH2CH2 D. 乙酸的结构简式: C2H4O2
难度: 简单查看答案及解析
-
下列说法错误的是
A. 乙烷室温下能与浓盐酸发生取代反应
B. 乙烯可以用作生产食品包装材料的原料
C. 乙醇室温下在水中的溶解度大于溴乙烷
D. 乙酸在甲酸甲酯互为同分异构体
难度: 中等查看答案及解析
-
下列有关实验的叙述,正确的是
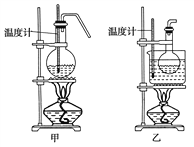
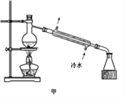
A. 石油分馏时,温度计的水银球应位于蒸馏烧瓶的支管口处
B. 用浓氨水洗涤做过银镜反应的试管
C. 配制银氨溶液时,先在试管中加入稀氨水,再逐滴加入AgNO3溶液
D. 配制Cu(OH)2悬浊液时,在2mL 10% CuSO4溶液中滴入几滴2%NaOH溶液
难度: 简单查看答案及解析
-
下列各组中的物质均能发生加成反应的是
A. 乙烯和乙醇 B. 苯和聚氯乙烯 C. 乙酸和溴乙烷 D. 丙烯和乙醛
难度: 简单查看答案及解析
-
下列分子式中只能表示一种物质的是( )
A.CH2O B.C2H4O2 C.C2H6O D.C3H7OH
难度: 中等查看答案及解析
-
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的的是
混合物
试剂
分离方法
A
乙炔(硫化氢)
硫酸铜溶液
洗气
B
乙烷(乙烯)
酸性高锰酸钾溶液
洗气
C
乙酸乙酯(乙酸)
氢氧化钠溶液
分液
D
苯(苯酚)
浓溴水
过滤
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
过量的下列溶液与
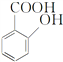 反应能得到化学式为C7H5O3Na的是
反应能得到化学式为C7H5O3Na的是A. Na2CO3溶液 B. NaHCO3溶液
C. NaOH溶液 D. NaCl溶液
难度: 中等查看答案及解析
-
某有机物是农药生产中的一种中间体,其结构简式如图。下列叙述不正确的是
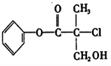
A. 在一定条件下能发生水解反应 B. 在一定条件下能发生消去反应
C. 1mol该有机物最多消耗2molNaOH D. 在一定条件下能发生加成反应
难度: 中等查看答案及解析
 _________________________________;
_________________________________;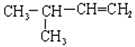 _________________________________;
_________________________________;