-
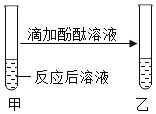
要使右图装置中的小气球鼓起来,则使用的固体和滴入液体可以是

①石灰石和稀盐酸 ②镁和稀硫酸
③固体氢氧化钠和水 ④生石灰和水
A. ①②③ B. ①②③④ C. ①②④ D. ②③④
难度: 中等查看答案及解析
-
下列各组物质,按混合物、单质顺序排列的是( )
A. 海水、干冰 B. 冰水、水银 C. 食醋、糖水 D. 煤、金刚石
难度: 简单查看答案及解析
-
中和反应在生活中有广泛应用。下列应用不属于中和反应的是( )
A.用盐酸除铁锈 B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤 D.用硫酸处理印染厂含碱废水
难度: 中等查看答案及解析
-
下列物质需要密封保存的是
A.浓硫酸 B.大理石 C.硝酸钾 D.氧化铜
难度: 中等查看答案及解析
-
下列固体物质加入水后,溶液温度会降低的是
A. NH4NO3 B. NaCl C. CaO D. NaOH
难度: 中等查看答案及解析
-
农作物生长需要含较多氮、磷、钾元素的化肥,下列化肥属于含磷复合肥料的是( )
A. NH4NO3 B. Ca(H2PO4)2 C. (NH4)2HPO4 D. KNO3
难度: 简单查看答案及解析
-
下列属于物理变化的是
A. 无色酚酞试液遇到氢氧化钠溶液变红 B. 浓盐酸瓶口产生白雾
C. 生石灰吸收空气中的水蒸气 D. 氢氧化钠在空气中变质
难度: 中等查看答案及解析
-
推理和归纳是学习化学的重要方法。以下说法正确的是( )
A.同种分子构成的物质是纯净物,则纯净物都是由同种分子构成
B.酸碱中和反应生成盐和水,则生成盐和水的反应都是中和反应
C.碳酸盐与盐酸反应放出气体,则与盐酸反应放出气体的物质都是碳酸盐
D.点燃H2和O2的混合物可能爆炸,则点燃可燃性气体和O2的混合物都可能爆炸
难度: 中等查看答案及解析
-
现有20°C时的硝酸钾钾饱和溶液200克,下列操作能改变该溶液中溶质的质量分数是
A. 温度不变加入10克硝酸钾
B. 温度不变加10克水
C. 温度不变蒸发掉10克水
D. 将此饱和溶液升温
难度: 中等查看答案及解析
-
元素氢、氧和R的化合价分别是+1、-2, +5,这三种元素组成的化合物可能是
A. HRO B. HRO2 C. H2RO3 D. H3RO4
难度: 中等查看答案及解析
-
欲除去氯化钙溶液中含有少量的盐酸,在不用酸碱指示剂的条件下,应加入的试剂是( )
A.石灰水 B.生石灰 C.纯碱 D.石灰石粉末
难度: 中等查看答案及解析
-
下列试剂中,能一次性将KOH溶液、稀硫酸、CaCl2溶液鉴别出来的是
A. 稀盐酸 B. K2CO3溶液 C. 无色酚酞 D. NaNO3溶液
难度: 困难查看答案及解析
-
对某pH=9的溶液成分进行分析、检测,下列结果合理的是( )
A.NaOH KCl Na2SO4 B.NH4Cl K2SO4 KNO3
C.H2SO4 ZnCl2 Mg(NO3)2 D.K2CO3 NaNO3 CaCl2
难度: 中等查看答案及解析
-
下列对实验意外事故的处理错误的是
A. 若不慎将燃着的酒精灯碰倒,洒出的酒精在桌上燃烧,应立刻用湿抹布扑盖
B. 若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液
C. 若不慎将腐蚀性药液溅入眼睛,要先用手揉眼睛,再立即用水冲洗
D. 若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液
难度: 中等查看答案及解析
-
.向一定量的氢氧化钡溶液中逐滴滴加稀硫酸至过量,下列图像与该反应事实相符合的是
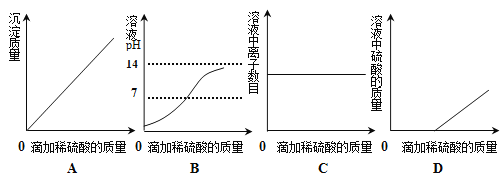
难度: 中等查看答案及解析
-
有甲、乙、丙、丁四种金属。只有甲在自然界主要以单质形式存在;丁盐的水溶液不能用乙制的容器盛放,但可用丙制的容器盛放。这四种金属的活动性由强到弱的顺序是
A. 甲>乙>丁>丙 B. 丙>丁>乙>甲 C. 丙>乙>丁>甲 D. 乙>丁>丙>甲
难度: 中等查看答案及解析
-
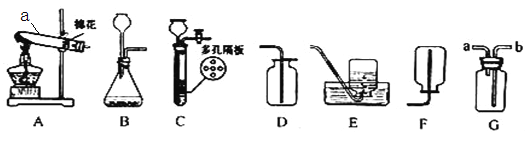
.如图是收集某气体的装置。由实验装置可推测该气体的有关性质为
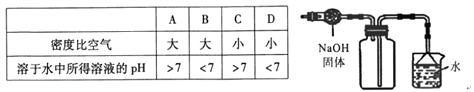
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列说法中,正确的是
A. 面粉发酵生成有机酸,在做面食之前要用小苏打去中和有机酸,该反应是中和反应
B. 为了提高铵态氮肥的肥效,可适量的与显碱性的物质草木灰(主要成分是碳酸钾)混合施用
C. 要除去铝制水壶中的水垢,应该用过量的稀盐酸长时间浸泡
D. 配制波尔多液时不能使用铁桶
难度: 中等查看答案及解析
-
实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化。测定结果如下图所示。下列说法不正确的是

A.反应过程中有热量放出
B.30s时,溶液中溶质为HCl和NaCl
C.该实验是将稀盐酸滴入稀NaOH溶液
D.从20s到40s,溶液的温度升高、pH增大
难度: 中等查看答案及解析
-
实验室配制50 g溶质质量分数为15%的氯化钠溶液。下列说法中错误的是
A. 实验的步骤为计算、称取、量取、溶解、转移
B. 溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率
C. 量取水时,用规格为50 mL的量筒量取42.5 mL蒸馏水
D. 把配制好的氯化钠溶液倒入刚用蒸馏水洗过的试剂瓶中,并贴上标签
难度: 中等查看答案及解析
-
下列几组物质中能按照右边关系图进行转化的一组是(→表示反应一步完成)
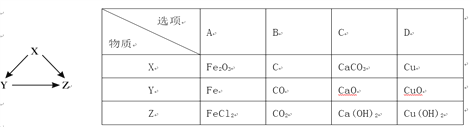
A. A B. B C. C D. D
难度: 困难查看答案及解析