-
(核磁共振)可用于含碳化合物的结构分析
N—NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关。
叙述正确的是

A.
与砖
N具有相同的中子数 B.
C与
是同一种物质
C.
N与
N互为同位素 D.
N的核外电子数与中子数相同
难度: 简单查看答案及解析
-
下列化学用语书写正确的是
A.氮气分子的结构式: N≡N
B.高氯酸的分子式:
C.氯化镁的电子式:
D.用电子式表示氯化氢分子的形成过程:
难度: 简单查看答案及解析
-
在期表主族元素中,甲元素与乙、丙、丁三元素相邻,甲、乙的原子序数之和等于丙的原子序数;这四种元素原子的最外层电子数之和为20。下列判断中,正确的是
A.气态氢化物的稳定性:甲>丙
B.原子半径:丙>乙>甲>丁
C.最高价氧化物对应水化物的酸性:丁>甲
D.乙和甲或乙和丁所能形成的化合物都是有毒物质
难度: 简单查看答案及解析
-
将mg块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如下图的实线所示,在相同的条件下,将mg粉末状碳酸钙与同浓度足量盐酸反应,则相应的曲线(图中虚线所示)正确的是
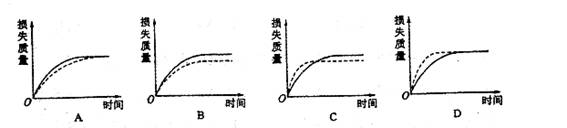
难度: 简单查看答案及解析
-
下列叙述中,金属a的活泼性肯定比金属b的活泼性强的是
A.a原子的最外层电子数比B原子的最外层电子数少
B.常温时,a能从水中置换出氢,而b不能
C.1mol a从酸中置换H+生成的
比l mol b从酸中置换
生成的
多
D.a原子电子层数比b原子的电子层数多
难度: 简单查看答案及解析
-
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是
元素代号
L
M
Q
R
T
原子半径/nm
0.160
0.134
0.089
0.102
0.074
主要化合价
+2
+3
+2
+6、-2
-2
A.
与
的核外电子数相等
B.L与T形成的化合物具有两性
C.氢化物的稳定性为
<
D.单质与浓度相等的稀盐酸反应的速率为Q<L
难度: 简单查看答案及解析
-
下列反应是吸热反应的是
A.铝片与稀硫酸反应 B.甲烷在氧气中燃烧
C.NaOH溶液和稀盐酸 D.
与
的反应
难度: 简单查看答案及解析
-
已知
、
、Z
、
四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,正确的是
A.原子序数:Y>X>Z>W B.原子半径:X>Y>Z>W
C.原子最外层电子数:Y>X>Z>W D.金属性:X<Y,还原性:
>
难度: 简单查看答案及解析
-
某元素最高正价氧化物对应的水化物的化学式是
,这种元素的气态氢化物的化学式为
A.HX B
C
D.
难度: 简单查看答案及解析
-
在2A+B
3C+4D反应中,表示该反应速率最快的是
A.
’ B.
C.
’ D.
难度: 简单查看答案及解析
-
下列各表中的数字代表的是原子序数,表中数字所表示的元素与它们在周期表中
位置相符的一组是

难度: 简单查看答案及解析
-
参照反应Br+
HBr+H的能量对
反应历程的示意图,下列叙述中正确的是

A.正反应为放热反应
B.加人催化剂,该化学反应的反应热不
改变
C.反应物总能量高于生成物总总量
D.升高温度可增大正反应速率,降低逆反应速率
难度: 简单查看答案及解析
-
把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c.b、c相连时,c上有大量气泡.b、d相
连时,d上有大量气泡产生,则这四种金属的活动顺序由强到弱为
A.a>b>c>d B.a>c>b>d
C.c>a>b>d D.b>d>c>a
难度: 简单查看答案及解析
-
下列说法正确的
A.需加热才能发生的反应一定是吸热反应
B.放热的反应在常温下一定易进行
C.反应是放热还是吸热是由反应物和生成物所具有的能量的相对大小决定的
D.质量数相同的原子,其化学性质也一定相同
难度: 简单查看答案及解析
-
一定条件下,在容积固定的某密闭容器中发生的反应
。在10s内
的浓度由5mol/L降至4mol/L下列说法正确的是
A.用
表示的化学反应速率为0.1mol/(L·s)
B.使用合适的催化剂,可以加快该反应的速率
C.增加
的浓度或降低温度都会加快该反应的速率
D.反应足够长时间,
、
中至少有一种物质浓度降为零
难度: 简单查看答案及解析
-
锗(Ge)是第四周期第ⅣA元素,处于周期表中金属区与非金属区的交界线上,下列叙述正确的是
A.锗是一种金属性很强的元素 B.锗的单质具有半导体的性能
C.锗化氢
稳定性很强 D.锗酸(
是难溶于水的强酸
难度: 简单查看答案及解析
-
某课外活动小组使用下列用品设计原电池。用品:铜片、铁片、导线、金属夹、发光二极管、果汁(橙汁、苹果汁)500mL,、烧杯。下列说法正确的是
A.该装置能将电能转化为化学能 B.实验过程中铜片逐渐溶解
C.电子由铁片通过导线流向铜片 D.铁片上会析出红色的铜
难度: 简单查看答案及解析
-
下列各组物质中化学键的类型相同的是
A.HCI
B.
C.NaOFI
D.
难度: 简单查看答案及解析