-
3月11日的日本大地震使福岛第一核电站受损,泄漏放射性物质131I、132I、和134Cs、137Cs等导致核污染.服用一定剂量的碘片可防放射性碘的伤害.下列说法错误的是( )
A.131I、132I、134Cs、137Cs是四种不同的核素
B.食用碘盐不能防辐射
C.碘片的主要成分是I2
D.核能仍然是重要能源之一难度: 中等查看答案及解析
-
常温下,甲溶液由50mL 0.1mol/L氨水(pH=11)和50mL水混合而成,乙溶液由50mL 0.1mol/L氨水和50mL 0.1mol/L NH4Cl溶液混合而成.下列判断错误的是( )
A.甲溶液的pH:10<pH(甲)<11
B.乙溶液的pH:7<pH(乙)<11
C.乙溶液中:c(NH4+)+c=c(Cl-)
D.甲、乙两溶液中分别加入0.2gNaOH后:pH(甲)>pH(乙)难度: 中等查看答案及解析
-
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A.1mol羟基(-OH)与17gNH3所含电子数都为NA
B.12.4g白磷(分子式为P4)中含有P-P共价键0.6NA
C.电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g
D.适量铜粉溶解于1L0.5mol•L-1稀硝酸中,当生成2.24LNO时,溶液中氮原子数为0.4NA难度: 中等查看答案及解析
-
关于如图所示实验装置的叙述错误的是( )
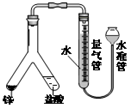
A.将水准管上提,液面高于量气管且不下降,说明装置不漏气
B.可用来测定气体摩尔体积
C.可用来测定锌的相对原子质量
D.用CCl4代替水,测得氢气的体积更准确难度: 中等查看答案及解析
-
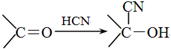
有机物甲(结构如图所示)是合成西洛他唑(商品名platal)的重要中间体,也是合成抗血栓药、哮喘药、强心药等药的重要中间体.下列对它的分析合理的是( )
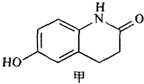
A.甲中只含酚羟基、羰基等两含氧官能团,不能发生水解反应
B.甲的核磁共振氢谱图上有7种不同的峰
C.常温下甲易使溴水褪色、易被氧气氧化、易跟氢气加成
D.1mol甲最多可以分别和1molNaOH、2molBr2反应难度: 中等查看答案及解析
-
香花石由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍.下列说法错误的是( )
A.原子半径:Y>Z>R>T
B.气态氢化物的稳定性:W<R<T
C.最高价氧化物对应的水化物碱性:X>Z
D.XR2、WR2两化合物中R的化合价相同难度: 中等查看答案及解析
-
向盛有a g镁铝合金的烧杯中加入cl mol/L稀硫酸V1L,合金完全溶解后,再加入c2 mol/L的NaOH溶液V2L,生成沉淀的质量恰好达到最大值bg.则下列关系式不正确的是( )
A.2c1V1=c2V2
B.反应产生氢气的质量m(H2)=
C.b≤a+17c2V2
D.合金中含镁的质量分数ϖ(Mg)=100%
难度: 中等查看答案及解析