-
下列说法正确的是( )
A.浓硫酸与亚硫酸钠反应制取二氧化硫,体现浓硫酸具有强氧化性
B.铵盐受热易分解,均有NH3产生
C.浓硝酸保存在棕色的细口瓶中
D.化工厂可通过加高烟囱排放废气,防止形成酸雨
难度: 中等查看答案及解析
-
一定量的锎(98252Cf)是有用的中子源,在医学上常用作治疗恶性肿瘤的中子源。下列有关锎的说法错误的是( )
A.98252Cf原子中,中子数为154 B.98252Cf原子中,质子数为98
C.98252Cf原子中,电子数为 98 D.锎元素位于第6周期
难度: 中等查看答案及解析
-
已知元素X、Y的核电荷数分别是a和b,它们的离子Xm + 和Yn - 的核外电
子排布相同,则下列关系式正确的是( )
A.a = b+m+n B.a = b-m+n C.a = b+m-n D.a=b-m-n
难度: 中等查看答案及解析
-
光导纤维传输信息容量大,而且抗干扰、防窃听,光导纤维的主要成分是
A.晶体硅 B.二氧化硅 C.硅酸盐 D.铝硅合金
难度: 简单查看答案及解析
-
在1L/mol氨水中,下列叙述正确的是( )
A.含1molNH3·H2O
B.含NH3 、NH4+之和为1mol
C.只含有1molNH3
D.NH3、 NH3·H2O、 NH4+之和为1mol
难度: 中等查看答案及解析
-
下列反应的现象均是溶液褪色,问其中能体现二氧化硫有漂白性的是( )
A.将SO2气体通入含有氢氧化钠的酚酞溶液中,溶液褪色
B.将SO2气体通入氯水中,溶液褪色
C.将SO2通入品红溶液中,溶液褪色
D.将SO2气体通入酸性高锰酸钾溶液中,溶液褪色
难度: 中等查看答案及解析
-
短周期元素X、Y、Z的原子序数依次增大,Y为ⅠA族元素,X与Z同主族,3种元素原子的最外层电子数之和为13,下列判断正确的是( )
A.Y元素位于第2周期 B.Y、Z均能与X形成不只一种化合物
C.X是VA族元素 D.氢化物的稳定性:HnZ > HnX
难度: 中等查看答案及解析
-
在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器接触室(见图)。按此密闭体系中气体的流向,则在A处流出的气体为( )

A.SO2 B.SO3、O2 C.SO2、SO3 D.SO2、O2
难度: 简单查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是( )
A.大理石与盐酸反应:CO32-+ 2H+ =H2O+CO2↑
B.向NH4HCO3溶液中加过量的NaOH溶液并加热: NH4++OH-
NH3↑+H2O
C.将过量SO2通入冷氨水中: SO2+NH3·H2O =HSO3-+NH4+
D.用稀硝酸洗涤试管内壁的银镜: Ag+2H++NO3-=Ag++NO↑+H2O
难度: 中等查看答案及解析
-
喷泉实验是一种常见的自然现象,其产生原因是存在压强差。在图中的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )

A.Cu与稀盐酸 B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸 D.NH4HCO3与稀盐酸
难度: 中等查看答案及解析
-
某溶液能与锌片作用产生H2,则该溶液中可以大量共存的离子组是( )
A.Na+、NO3-、K+、Fe2+ B.Fe2+、Na+、SO42-、K+
C.K+、I-、NO3-、H+ D.NH4+、NO3-、Na+、HCO3-
难度: 中等查看答案及解析
-
在体积为100mL浓度为18mol·L-1的浓硫酸中加入过量铜片并加热,问被还原的硫酸的物质的量为( )
A、等于0.9mol B、大于0.9mol C、小于0.9mol D无法确定
难度: 简单查看答案及解析
-
KClO3与浓盐酸发生如下反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,有关该反应,说法不正确的是:( )
A.被氧化的元素和被还原的元素的质量之比5:1
B.Cl2既是氧化产物,又是还原产物
C.盐酸既体现酸性,又体现酸性还原性
D.转移5mol电子时,产生67.2L的Cl2
难度: 中等查看答案及解析
-
在稀硫酸中加入铜粉,铜粉不溶解,再加入某X物质,发现铜粉逐渐溶解,问神秘的X不可能是( )
A.FeCl3 B.HNO3 C.HCl D.KNO3
难度: 中等查看答案及解析
-
已知下列氧化剂均能氧化+4价的硫元素,为除去稀硫酸中混有的亚硫酸,以得到纯净的稀硫酸,应选用的最合理的氧化剂是( )
A.KMnO4 B.Ca(ClO)2 C.H2O2 D.Cl2
难度: 中等查看答案及解析
-
某硫酸厂废气厂SO2的回收利用方案如下图所示,下列说法不正确的是:
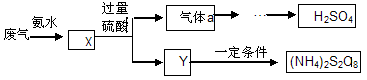
A.X可能含有2种盐 B.a是SO3
C.Y可能含(NH4)2SO4 D.(NH4)2S2O8中S元素的化合价不可能为+7
难度: 中等查看答案及解析
-
往2支分别装有浅绿色的Fe(NO3)2和FeSO4溶液的试管中,逐滴加入稀盐酸时,溶液的颜色变化应该是
A.前者基本没有改变、后者变棕黄色
B.前者变棕黄色、后者也变棕黄色
C.前者变棕黄色、后者基本没有改变
D.前者、后者都基本没有改变
难度: 中等查看答案及解析
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A的原子最外层电子数是次外层电子数的2倍,元素B的原子最外层电子数是其电子层数的3倍,D与A为同主族元素,元素C与E形成的化合物CE是厨房常用调味品。下列说法正确的是
A.原子半径:C>D>B>A
B.A、D、E最高价氧化物对应水化物酸性增强
C.只含B元素的物质一定是纯净物
D.化合物C2AB3的水溶液显碱性,可用于洗去铜片表面的油污
难度: 中等查看答案及解析
-
强酸X的转化关系如图:
 图中单质可能为( )
图中单质可能为( )A.C B.Fe C.Al D.Cu
难度: 中等查看答案及解析
-
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可使湿润的红色石蕊试纸变蓝,由此可知( )
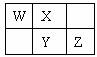
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性强于Y
D.Z元素单质在化学反应中只表现氧化性
难度: 中等查看答案及解析
-
可用如图装置制取(必要时可加热)、净化、收集的气体是( )
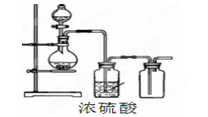
A.铜和稀硝酸制一氧化氮 B.氯化钠与浓硫酸制氯化氢
C.锌和稀硫酸制氢气 D.硫化亚铁与稀硫酸制硫化氢
难度: 简单查看答案及解析
-
高温下硫酸亚铁发生如下反应:2FeSO4
Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀物是( )
A.BaSO3和BaSO4 B.BaS C.BaSO3 D.BaSO4
难度: 中等查看答案及解析
-
下列有关物质鉴别方案不正确的一组是:( )
A.可用Ba(OH)2溶液鉴别(NH4)2CO3、Na2SO4、NH4NO3三种氮肥
B.MgCl2溶液、NaOH溶液、H2SO4溶液、CuSO4溶液,不加任何试剂即可鉴别
C.NH4Cl和NaCl两种固体物质的分离可用加热法
D.CuO粉末、炭粉、铁粉三种黑色粉末,用一种试剂无法鉴别
难度: 中等查看答案及解析
-
已知下列元素的原子半径如下表所示:
根据以上数据,磷原子的半径可能是
A.1.10 ×10-10 m B.0.80×10-10 m C.1.20× 0-10 m D.0.70×10-10 m
难度: 中等查看答案及解析
-
19.2g铜与适量的浓HNO3反应,铜全部反应后,共收集到11.2 LNO和NO2混合气体(标准状况),反应消耗HNO3的物质的量是( )
A.0.8 mol B.1.1 mol C.1.2 mol D.2.0 mol
难度: 中等查看答案及解析