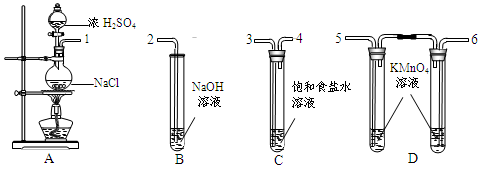
-
能用作自来水消毒剂的是
A.液氯 B.纯净的盐酸 C.洗衣粉 D.石灰石
难度: 中等查看答案及解析
-
自然界中最常见的钠的化合物是
A.NaCl B.Na2O2 C.Na2O D.Na
难度: 中等查看答案及解析
-
下列物质属于电解质的是
A.乙醇 B.铜单质 C.碳酸钠 D.蔗糖
难度: 中等查看答案及解析
-
与1mol NH3所含有的分子数目相同的是
A.0.5mol O2 B.1mol Fe C.2mol H2 D.2mol H2O
难度: 中等查看答案及解析
-
为高空或海底作业提供氧气的物质是
A.KClO3 B.KMnO4 C.Na2O2 D.H2O
难度: 中等查看答案及解析
-
下列物质的保存方法不正确的是
A.新制氯水应密封保存 B.盛液溴的试剂瓶常加少量水
C.少量的金属钠应保存在煤油中 D.固态碘放在棕色细口瓶中
难度: 中等查看答案及解析
-
下列叙述正确的是
A.1mol任何气体的体积一定是22.4L
B.同温同压下两种气体,只要它们的分子数相同,所占体积也一定相同
C.在标准状况下,体积为22.4L的物质都是1mol
D.在非标准状况下,1mol任何气体的体积不可能是22.4L
难度: 中等查看答案及解析
-
用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是
A.干燥的 B.瓶塞不漏水的
C.用欲配制的溶液润洗过的 D.以上三项均须要求的
难度: 中等查看答案及解析
-
下列变化中,需要添加还原剂的是
A.CaO→Ca(OH)2 B.Cu2+→Cu C.Fe2+→Fe3+ D.CO→CO2
难度: 中等查看答案及解析
-
做焰色反应实验时所用的铂丝,每次用毕后都要
A.用水多洗几次
B.先用稀盐酸洗,再用水洗
C.用稀盐酸洗,再在火焰上灼烧到没有什么颜色为止
D.放在火焰上灼烧,直到铂丝发红为止
难度: 中等查看答案及解析
-
下列离子方程式中,书写不正确的是
A.氯化钠溶液中加入硝酸银溶液:Ag+ + Cl- = AgCl↓
B.把金属钠放入水中:Na + 2H2O = Na+ +2OH- + H2
C.将溴水加入碘化钾溶液中:Br2 + 2I- = 2Br- + I2
D.盐酸滴在石灰石上:CaCO3 + 2H+ = Ca2+ + CO2↑ + H2O
难度: 中等查看答案及解析
-
下列各溶液中,Na+物质的量浓度最大的是
A.1 L 0.3mol/L Na2SO4溶液 B.1 L 0.3mol/L NaCl溶液
C.2 L 0.4mol/L NaOH溶液 D.2 L 0.15mol/L Na3PO4溶液
难度: 中等查看答案及解析
-
下列各组离子中,能在溶液中大量共存的是
A.H+、Ca2+、Cl-、CO32- B.I-、ClO-、K+、H+
C.Na+、Fe3+、SO42-、OH- D.Na+、Cu2+、Cl-、SO42-
难度: 中等查看答案及解析
-
将同体积同物质的量浓度的NaCl、MgCl2、AlCl3三种溶液中的Cl-完全沉淀,则
需同物质的量浓度的AgNO3溶液的体积比为
A.1∶2∶3 B.3∶2∶1 C.1∶1∶1 D.6∶3∶2
难度: 中等查看答案及解析
-
取两份物质的量相同的小苏打(NaHCO3)和苏打(Na2CO3),同时与相同浓度的盐酸反应。下列有关说法正确的是
A.前者消耗盐酸的体积多
B.后者消耗盐酸的体积多
C.将反应过程中产生的气体完全收集,前者产生的气体体积多(相同状况)
D.将反应过程中产生的气体完全收集,后者产生的气体体积多(相同状况)
难度: 中等查看答案及解析
-
下列说法中正确的是
A.在化学反应中某元素由化合物变为单质,该元素一定是被还原了
B.失电子难的原子获得电子能力一定强
C.卤族元素的原子半径随核电荷数的增加而减少
D.卤族元素中,核外电子数少的元素一定比核外电子数较它多的元素活泼
难度: 中等查看答案及解析
-
如图所示,锥形瓶内盛有干燥的气体X,胶头滴管内盛有液体Y,若挤压胶头
滴管,使液体Y滴入瓶中,振荡,一会儿可见小气球a鼓起。则气体X和液体Y不可能的是
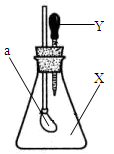
A.X是Cl2,Y是NaOH溶液
B.X是HCl,Y是稀氨水
C.X是CO2,Y是稀硫酸
D.X是SO2,Y是NaOH溶液
难度: 中等查看答案及解析
-
设
表示阿伏加德罗常数,下列说法正确的是
A.23 g钠与足量氧气充分反应,转移的电子个数为
B.1mol Cl2与水充分反应,转移的电子个数为
C.1mol Na2O2与水完全反应时转移电子数为2NA
D.18 g H2O含有的电子数为18NA
难度: 中等查看答案及解析
-
下列说法正确的是
A.某溶液中滴入AgNO3溶液,生成白色沉淀,该溶液中可能含Cl-
B.实验已经证明,氯水是可以导电的,所以氯水是电解质
C.某溶液与淀粉碘化钾溶液反应后出现蓝色,则证明该溶液是氯水
D.氟气跟氯化钠水溶液反应,有HF和O2生成
难度: 中等查看答案及解析
-
为了将FeCl2溶液转化成FeCl3溶液,最好的方法是向此溶液中
A.通入氯气 B.加入HCl
C.加入Fe D.加入Cu
难度: 中等查看答案及解析
-
某无色气体,可能含HCl、CO2、HI中的一种或两种,将其通入氯水中,得到无色透明溶液。加入硝酸酸化的AgNO3溶液,有白色沉淀生成。对于原无色气体推断一定正确的是
A.一定存在HCl B.一定存在CO2
C.肯定没有HI D.不能肯定是否含有HI
难度: 中等查看答案及解析