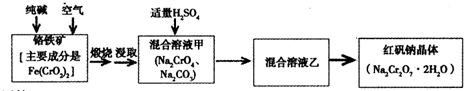
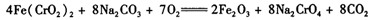-
空气、水、土壤及食品的污染,一定程度影响了人类生活,下列有关说法错误的是
A.雾霾天气中的主要污染物是PM2.5,其中含氮的有机物和光发生化学作用,可形成光化学烟雾
B.砷是水污染的重要因素之一,其最高价含氧酸砷酸的酸性比磷酸酸性弱
C.土壤污染物可分为无机污染物和有机污染物,农药污染多为有机污染物
D.苏丹红是人工合成的一种工业染料,若掺入饲料中饲养禽类会污染蛋类食品,它的结构简式是
 其分子式是:C22H18N4O
其分子式是:C22H18N4O难度: 中等查看答案及解析
-
下列说法及对应化学方程式或离子方程式正确的是
A.84消毒液与洁厕灵混合可能产生毒气: ClO- + Cl- + 2H+ = Cl2↑ + H2O
B.用二氧化硅和水反应可制得硅酸: SiO2 + H2O = H2SiO3
C.食醋与蛋壳反应: CaCO3 + 2H+ = Ca2+ + CO2↑ + H2O
D.铁在氯气中燃烧: Fe + Cl2 = FeCl2
难度: 中等查看答案及解析
-
下列说法正确的是
A.苯酚显酸性,是因为羟基对苯环影响的结果
B.分子式为C2H4和C3H6的物质一定互为同系物
C.聚合物
是苯酚和甲醛在一定条件下反应得到的高分子化合物
D. 1mol
与足量的NaOH溶液加热充分反应,最多能消耗5 mol NaOH
难度: 中等查看答案及解析
-
下图所示的实验装置或操作不能达到实验目的的是

难度: 中等查看答案及解析
-
下列说法正确的是
A.100℃时,KW =10-12,此温度下PH =6的溶液一定显酸性
B.25℃时,0.1mol/L的NaHSO3溶液pH =4,说明HSO3-在水溶液中只存在电离
C.NH4Cl、CH3COONa、NaHCO3、NaHSO4溶于水,对水的电离都有促进作用
D.25℃时,10mL 0.1mol/L CH3COOH溶液与5mL 0.1mol/L NaOH溶液混合,所得溶液中有
2c(Na+)= c(CH3COO-) + c(CH3COOH)
难度: 中等查看答案及解析
-
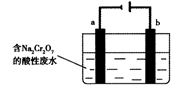
下图是一套电化学装置,对其有关说法错误的是
A.装置A是原电池,装置B是电解池
B.反应一段时间后,装置B中溶液PH增大
C.a口若消耗1mol CH4,d口可产生4mol气体
D. a口通入C2H6时的电极反应为 C2H6 -14e- + 18OH- = 2CO32- + 12H2O
难度: 中等查看答案及解析
-
在容积为1L的密闭容器中,充入1mol CO2和3mol H2,在温度500℃时发生反应:CO2(g)+ 3H2(g)
CH3OH(g)+ H2O(g) △H<0。CH3OH的浓度随时间变化如图,下列说法不正确的是
A.从反应开始到10分钟时,H2的平均反应速率v(H2)=0.15 mol/(L·min)
B.从20分钟到25分钟达到新的平衡,可能是增大压强
C.其它条件不变,将温度升到800℃,再次达平衡时平衡常数减小
D.从开始到25分钟,CO2的转化率是70%
难度: 中等查看答案及解析
 (R、R’为烃基或其他基团)应用上述反应原理合成防晒霜主要成分K的路线如下图所示(部分反应试剂和条件未注明):
(R、R’为烃基或其他基团)应用上述反应原理合成防晒霜主要成分K的路线如下图所示(部分反应试剂和条件未注明):