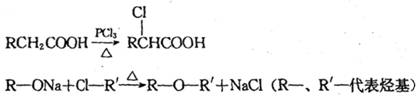-
(1分)W、X、Y、Z、L、M为元索周期表中原子序数依次增大的短周期元素。
已知:①X的单质在Z2中燃烧可生成XZ和XZ2两种气体;
②L是一种金屑单质,该金属与Z2反应可生成L2Z和L2Z2两种固体;
③M的单质在Z2中燃烧的产物可使品红溶液褪色,加热后恢复原色;
请回答下列问题:
(1) 写出L2Z的电子式________
(2) 写出L2Z2与XZ2气体反应的化学方程式________________________________
(3) X、Y、Z分别与W可形成10电子化合物,这三种化合物中沸点最髙的是(填化学式)________________, W、Y、Z可形成离子化合物W4Y2Z3,其水溶液中各离子浓度由大到小的顺序为________________________, W2Z2与FeSO4混合溶于稀硫酸中,反应的离子方程式为________________________________________;
(4) 在容积为2L的密闭容器中加人0.48mol MZ2和0.22mol Z2, —定温度下反应达到平衡时得到0. 24 mol MZ3,则反应的化学平衡常数K=________,若温度不变,再加人0.50 mol Z2后重新达到平衡,则Z2的转化率________ (填“升高”、“不变”或“降低”),MZ3的体积分数________ (填“增大”、“不变”或“减小”)。
-
(12分)甲醇作为新型汽车动力燃料,工业上可由CO和H2合成。该反应的热化学方程式: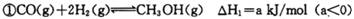
该反应的原料CO和H2本身可作为燃料,它们的热化学方程式为:
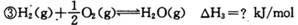
某些化学键的键能数据如下表

请回答下列问题:
(1)反应③中的ΔH3=________kJ/mol
(2) CH3OH燃烧生成CO2(g)和H2O(g)的热化学方程式为
 ,该反应的焓变
,该反应的焓变 =________kJ/mol (用含a、b的式子表示);
=________kJ/mol (用含a、b的式子表示);
(3) 若降低温度,反应①的化学平衡常数K值将________ (填“增大”、“减小”或“不变”);
(4) 甲醇一空气电池是一种髙效、低污染质子交换腆燃料电池,电池总反应为 。甲醉在催化剂作用下提供质子和电子。右图为该电池的示意图,则电极d上发生的电极反应式为________________。
。甲醉在催化剂作用下提供质子和电子。右图为该电池的示意图,则电极d上发生的电极反应式为________________。
-
【化学――选修化学与技术】(15分)
氨在国民经济中占有重要地位,下图是合成氨的简要流程:
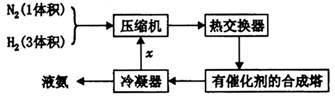
I.原料气的制备:
(1) 合成氨所需氮气来自空气,方法之一是将空气液化后再加热分馆;请另设计一种从空气中分离出氮气的方法:_________________________________________________________;
(2) 请写出工业上获得氢气的一种方法(用化学方程式表示)____________
II.原料气的净化:、
为防止催化剂“中毒”,原料气在进人压缩机之前必须经过净化、精制处理,“精制”过程通常是将含有少量CO、CO2、O2和H2S等杂质的原料气体通入含有氨水的醋酸亚铜二氨( )溶液,以获得纯净原料气。其中,吸收CO的反应为:
)溶液,以获得纯净原料气。其中,吸收CO的反应为:

(3) 为提髙CO吸收率,可采取的有效措施是__________________
(4) 除去氧气时,氧气将 氧化为
氧化为 ,则反应中还原剂与氧化剂的物质的量之比是____________;
,则反应中还原剂与氧化剂的物质的量之比是____________;
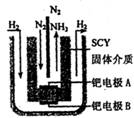
III.氨的合成:
(5)据报道,科学家采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了髙温常压下高转化率的电化学合成氨。其实验装置如图。请写出钯电极A上的电极反应式________________________
-
【化学――选修物质结构与性质】(15分)
有A、B、C、D、E五种元素。其相关信息如下:

请回答下列问题。
(1) 写出E元素原子基态时的电子排布式__________________;
(2) C元素的第一电离能比氧元索的第一电离能 ______ ______ (填“大”或“小”);
(3) CA3分子中C原子的杂化轨道类型是____________;
(4) A、C、E三种元素可形成 配离子,其中存在的化学键类型有 ______ (填序号);
配离子,其中存在的化学键类型有 ______ (填序号);

①配位键 ②金属键③极性共价键④非极性共价键⑤离子键 ⑥氢键
若 具有对称的空间构型,且当
具有对称的空间构型,且当 中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则
中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则 的空间构型为 ______ ______ (填序号);
的空间构型为 ______ ______ (填序号);
a.平面正方形 b.正四面体 c.三角锥型 d. V型
(5) B与D可形成离子化合物,其晶胞结构如右图所示。其中D离子的配位数为_____,若该晶体的密度为ag • cm-3,则该晶胞的体积是______cm-3 (写出表达式即可)。
-
【化学―――选修有机化学基础】(15分)
氯贝特是临床上一种降脂抗血栓药物,其结构如下图所示: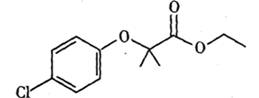
它的一条合成路线如下: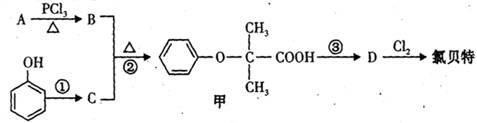
提示:(图中部分反应条件及部分反应物、生成物已略去)
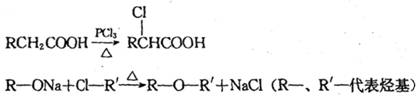
(1)氯贝特的分子式为__________________
(2) 若8.8gA与足量NaHCO3溶液反应生成2.24LCO2(标准状况),且B的核磁共振氢谱有两个峰,则A的结构简式为______, B中含有的官能团名称为______
(3) 要实现反应①所示的转化,加入下列物质不能达到目的的是____________
a. NaOH b. Na2CO3 c d.
d.
(4) 反应②的反应类型为____________,其产物甲有多种同分异构体,请判断同时满足以下条件的所有同分异构体X有______种
①1,3, 5—三取代苯;
②属于酯类且既能与FeCl3溶液显紫色,又能发生银镜反应;
③1molX最多能与3molNaOH反应。
(5)反应③的化学方程式为________________________
)。偏二甲肼的同分异构体中含碳碳单键的化合物种类共有
中,每生成4molCl2转移的电子数为8NA
B (a — b) mol
D. (a+b) mol
达到平衡,n(H2)和n(NH3)随时间变化的关系如图所示。下列有关叙述一定正确的是

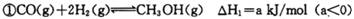
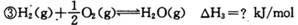

 ,该反应的焓变
,该反应的焓变