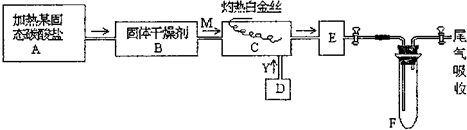
-
某溶液中含有较大量的Cl-、CO32-、OH-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液;②过滤;③滴加AgNO3溶液;④滴加Ba(NO3)2溶液.
A.①②④②③
B.④②①②③
C.①②③②④
D.④②③②①难度: 中等查看答案及解析
-
已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;
②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;
③取实验②生成的溶液滴在淀粉KI试纸上,试纸变为蓝色.
下列判断正确的为( )
A.上述实验证明氧化性:MnO4->Cl2>Fe2+>I2
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性难度: 中等查看答案及解析
-
下列说法正确的是( )
A.第ⅠA族元素的金属性比第ⅡA族元素的金属性强
B.第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D.第三周期元素的离子半径从左到右逐渐减小难度: 中等查看答案及解析
-
进行化学实验必须注意安全,下列操作不正确的是( )
A.做CO还原CuO的实验,尾气用点燃的方法除去
B.不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗
C.实验室制备并收集乙烯,实验结束时应先熄灭酒精灯再撤导管
D.实验室制Cl2实验的尾气用NaOH溶液吸收难度: 中等查看答案及解析
-
以NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.7.8gNa2O2固体中,含有0.2NA个阴离子
B.1mol-CH3(甲基)中含有8NA个电子
C.31g白磷中含有NA个P-P键
D.16gO3中含有NA个氧原子难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.直径介于1nm~10nm之间的微粒称为胶体
B.电泳现象可证明胶体属于电解质溶液
C.利用丁达尔效应可以区别溶液与胶体
D.胶体粒子很小,可以透过半透膜难度: 中等查看答案及解析
-
将质量分数为5%和25%的氨水等体积混合后,所得溶液中溶质的质量分数为( )
A.等于15%
B.小于15%
C.大于15%
D.不能确定难度: 中等查看答案及解析
-
下列各组离子中,在碱性溶液中能大量共存,且加入盐酸过程中会产生气体和沉淀的是( )
A.Na+、NO、AlO
、SO
B.Na+、NO、SiO
、K+
C.K+、Cl-、AlO、CO
D.Na+、Cl-、HCO、Ca2+
难度: 中等查看答案及解析
-
已知元素砷(As)的原子序数为33,下列叙述中不正确的是( )
A.砷原子的第3电子层含有18个电子
B.砷元素的最高化合价为+5价
C.砷的氧化物的水溶液呈强碱性
D.砷是第4 周期的主族元素难度: 中等查看答案及解析
-
化合物甲是由氟元素和氧元素形成的一种不稳定的物质,10mL甲气体可分解成15mLO2和10mLF2(气体都在同温同压下测定).下列关于化合物甲的说法正确的是( )
A.甲具有很强的氧化性
B.该化合物的分子式为O2F2
C.其电子式可表示为F:O:O:F
D.甲中氧元素的化合价为-2价难度: 中等查看答案及解析
-
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.因而称为释迦牟尼分子(的有原子在同一平面).有关该有机分子的说法正确的是( )
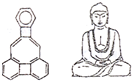
A.该有机物不属于芳香烃
B.该有机物属于苯的同系称
C.该有机物分子中含有22个碳原子
D.该有机物一氯代物只有3种难度: 中等查看答案及解析
-
高温下硫酸亚铁发生如下反应:2FeSO4
Fe2O3+SO2↑+SO3↑若将生成的气体通入硝酸钡溶液中,得到的沉淀是( )
A.BaSO3和BaSO4
B.BaS
C.BaSO3
D.BaSO4难度: 中等查看答案及解析
-
如图是一种试验某气体化学性质的实验装置,图中B为开关.若先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去.则D瓶中盛有的溶液是( )
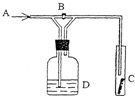
A.浓H2SO4
B.饱和NaCl溶液
C.浓NaOH溶液
D.浓NaBr溶液难度: 中等查看答案及解析
-
①Na2O②NaOH③Na2O2④Na2SO3,上述固体物质各1mol,长时间放置于空气中,最后质量增加情况是(不考虑潮解因素)( )
A.①=②>③>④
B.②>①=③>④
C.①>③>④>②
D.④>②>③>①难度: 中等查看答案及解析
-
在某100mL混合酸中,HNO3物质的量浓度为0.4mol/L,H2SO4物质的量浓度为0.2mol/L.向其中加入1.92克铜粉微热,待充分反应后,溶液中的Cu2+物质的量浓度为( )
A.0.15mol/L
B.0.3mol/L
C.0.225mol/L
D.无法计算难度: 中等查看答案及解析
-
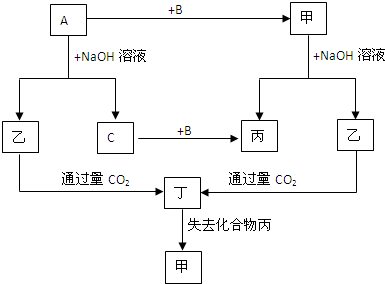
已知结构为正四面体型的离子E和直线型离子G反应,生成三角锥型分子L和V形分子M(组成E、G、L、M微粒的元素原子序数均小于10),反应过程用下图表示,则下列判断错误的是( )
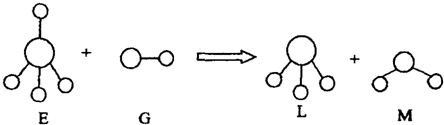
A.E、G、L、M都是10e-微粒
B.L、M都是极性分子
C.L能使紫色石蕊试液变蓝色
D.E离子中,质子数一定大于中子数难度: 中等查看答案及解析
-
在硫酸铜溶液中加入碘化钾溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析证明白色沉淀是碘化亚铜.则能正确表示这个氧化还原反应的离子方程式是( )
A.Cu2++3I-═CuI↓+I2
B.Cu2++2I-═Cu++I2
C.2Cu2++2I-═2Cu++I2
D.2Cu2++4I-═2CuI↓+I2难度: 中等查看答案及解析
-
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
A.洗气瓶中产生的沉淀是碳酸钡
B.洗气瓶中产生的沉淀是硫酸钡
C.在Z导管出来的气体中没有二氧化碳
D.在Z导管口有红棕色气体出现难度: 中等查看答案及解析
-
往100mL2mol•L-1的AlCl3溶液中,逐滴加入NaOH溶液100mL时,产生沉淀为7.8g则所加入NaOH溶液物质的量浓度是( )
A.1 mol•L-1
B.1.5 mol•L-1
C.3 mol•L-1
D.7mol•L-1难度: 中等查看答案及解析
-
X、Y、Z、M代表四种金属元素.金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+离子共存的溶液时,Y先析出;又知M2+离子的氧化性强于Y2+离子.则这四种金属的活动性由强到弱的顺序为( )
A.X>Y>Z>M
B.X>Z>Y>M
C.M>Z>X>Y
D.X>Z>M>Y难度: 中等查看答案及解析
-
下列实验操作中,仪器需插入液面下的有:①制备Fe(OH)2用胶头滴管将NaOH溶液滴入FeSO4溶液中;②制备氢气,简易装置中长颈漏斗的下端管口;③分馏石油时测量温度所用的温度计;④用乙醇制备乙烯时所用的温度计;⑤有水吸收氨气时的导气管;⑥向试官中的BaCl2溶液中滴加稀硫酸( )
A.③⑤⑥
B.②⑤
C.①②④
D.①②③④⑤⑥难度: 中等查看答案及解析
-
下列实验过程中产生的现象与对应的图形相符合的是( )
A.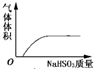 NaHSO3粉末加入HNO3溶液中
NaHSO3粉末加入HNO3溶液中
B.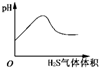 H2S气体通入氯水中
H2S气体通入氯水中
C.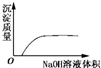 NaOH溶液滴入Ba(HCO3)2溶液中
NaOH溶液滴入Ba(HCO3)2溶液中
D. CO2气体通入澄清石灰水中
CO2气体通入澄清石灰水中 难度: 中等查看答案及解析
-
在同一条件下,体积相同的三个烧瓶中分别盛有NH3、HCl、NO2气体,并分别倒立在水槽中,充分反应后,烧瓶内三种溶液的物质的量浓度之比为(设烧瓶中的溶液未扩散到水槽里)( )
A.1:1:1
B.2:2:3
C.3:3:2
D.2:2:1难度: 中等查看答案及解析
-
2mol/L的稀盐酸与H2SO4各100mL,分别加入等量的Fe粉.反应结束后,产生的气体质量比为2:3,则向盐酸中加入铁粉的质量是( )
A.8.4g
B.2.8g
C.11.2g
D.5.6g难度: 中等查看答案及解析
-
等物质的量的主族金属A、B、C分别与足量的稀盐酸反应,所得氢气的体积依次为VA、VB、VC,已知VB=2VC,且VA=VB+VC,则在C的生成物中,该金属元素的化合价为( )
A.+1
B.+2
C.+3
D.+4难度: 中等查看答案及解析