-
化学与生活、能源、材料和环境关系非常密切,下列说法不正确的是
A. 用K2FeO4代替Cl2处理饮用水,既能杀菌又能净水
B. 使用乙醇汽油既能节约能源,又能减少污染物的排放
C. 金属材料都是导体,非金属材料都是绝缘体
D. 酸雨以及光化学烟雾的形成通常都与氮的含氧化合物有关
难度: 简单查看答案及解析
-
从化学视角看“烟”和“雾”是有区别的,下列含有“烟”字的诗句中.烟"实则为“雾”的是
A. 大漠孤烟直,长河落日圆
B. 暖暖远人村,依依墟里烟
C. 烟笼寒水月笼沙,夜泊秦淮近酒家
D. 故人西辞黄鹤楼,烟花三月下扬州
难度: 中等查看答案及解析
-
设
为阿伏加德罗常数的值。下列说法正确的是
A. 39gNa2O2与CO2完全反应,转移的电子数为
B. 6.0gNO和3.2gO2混合,所得气体的分子数目为0.2
C. 84gFe完全转化为Fe3O4,失去的电子数为4
D. 1molCu和2mol热浓硫酸反应,生成SO2分子数目为
难度: 简单查看答案及解析
-
下列图示实验操作与对应的实验目的合理的是

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸。已知:KMnO4+ 16HC1=2KCl+5Cl2↑ +2MnCl2+8H2O,向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。

下列有关说法正确的是
A. a处变蓝、b处变棕红说明非金属性:C12> Br2 > I2
B. c处先变红、后褪色说明Cl2与H2O反应生成HC1
C. d处立即褪色说明Cl2与H2O反应生成HCIO
D. e处变红说明Cl2与Fe2+反应生成Fe3+
难度: 中等查看答案及解析
-
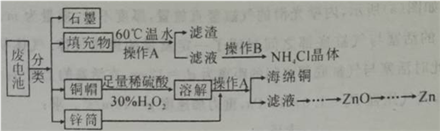
实验室用NH4Cl盐酸、NaClO2(亚氯酸纳)为原料制备C1O2的过程如下图所示。

下列说法不正确的是
A. X中大量存在的阴离子有C1-和OH-
B. NH3和NC13中N元素的化合价相同
C. NaClO2变成ClO2发生了氧化反应
D. 制取lmolClO2至少需要
molNH4Cl
难度: 简单查看答案及解析
-
Hg可用KMnO4溶液吸收。在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如下图所示。下列有关说法不正确的是

A. pH对Hg吸收率的影响规律是随pH升高Hg的吸收率先降低后升高
B. pH=l时Hg的吸收率高达90%的原因是KMnO4在酸性条件下氧化性强
C. pH = 2时反应的离子方程式为Hg+MnO4-+8H+=Hg2++Mn2++4H2O
D. pH = 12时反应的离子方程式为3Hg+2MnO4-+ H2O=3HgO+2Mn02+2OH-
难度: 中等查看答案及解析