-
下列有关氨水和氯水的说法正确的是
A. 含有的微粒种类数相同 B. 敞口放置后溶液的pH均可能减小
C. 都能与S02发生氧化还原反应 D. 均具有强氧化性
难度: 中等查看答案及解析
-
下列说法正确的是
①正常雨水的pH为7.0,酸雨的pH小于7.0
②严格执行机动车尾气排放标准有利于防止大气污染
③使用二氧化硫和某些含硫化合物进行增白的食品会对人体健康产生损害
④使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害
⑤食品厂产生的含丰富氮、磷营养元素的废水可长期排向水库养鱼
A. ①②③ B. ①④⑤ C. ②③④ D. ③④⑤
难度: 中等查看答案及解析
-
下列物质中,属于纯净物的是( )
①陶瓷 ②水泥 ③玻璃 ④漂白粉 ⑤胆矾 ⑥氯水 ⑦液氯
A. ①③⑤ B. ②④⑥ C. ⑤⑦ D. ⑥⑦
难度: 中等查看答案及解析
-
浓硫酸在下列转化中,既表现出氧化性又表现出酸性的是 ( )
A. Cu―→CuSO4 B. C―→CO2
C. Fe(OH)3―→Fe2(SO4)3 D. Fe2O3―→Fe2(SO4)3
难度: 简单查看答案及解析
-
将铁屑溶于过量盐酸后,再加入下列物质,会有三价铁生成的是( )
①硫酸 ②氯水 ③硝酸锌 ④氯化铜
A. ② B. ③ C. ②③ D. ①④
难度: 中等查看答案及解析
-
下列说法不正确的是( )
A. 活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同
B. 非金属氧化物不一定是酸性氧化物,金属氧化物多数是碱性氧化物
C. 同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积相同
D. 将CO2气体通入BaCl2溶液中至饱和未见沉淀生成,继续通入NO2则有沉淀生成
难度: 简单查看答案及解析
-
下列实验过程中,始终无明显现象的是 ( )
A. NO2通入FeSO4溶液中
B. CO2通入CaCl2溶液中
C. NH3通入AlCl3溶液中
D. SO2通入已酸化的Ba(NO3)2溶液中
难度: 简单查看答案及解析
-
在如下图的实验装置中,实验开始一段时间后,对看到的现象叙述不正确的是 ( )
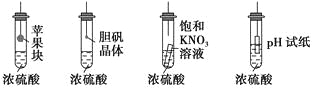
A. 苹果块会干瘪 B. 胆矾晶体表面有“白斑”
C. 小试管内有KNO3晶体析出 D. pH试纸变红
难度: 中等查看答案及解析
-
下列物质中既能与盐酸反应又能与氢氧化钠溶液反应的是( )
A. Al(OH)3 B. Fe(OH)3 C. Mg(OH)2 D. Cu(OH)2
难度: 中等查看答案及解析
-
下列各组反应中最终肯定得到白色沉淀的是( )
A. AlCl3溶液中加入过量氨水
B. Al2(SO4)3溶液中加入过量KOH溶液
C. FeCl2溶液中加入过量氨水
D. Fe2(SO4)3溶液中加入过量KOH溶液
难度: 中等查看答案及解析
-
下列物质的鉴别方法不正确的是( )
A. 用焰色反应鉴别NaCl、KCl和Na2SO4
B. 用氢氧化钠溶液鉴别MgCl2溶液、AlCl3溶液
C. 利用丁达尔效应鉴别Fe(OH)3胶体与FeCl3溶液
D. 用氯化钙溶液鉴别Na2CO3和NaHCO3两种溶液
难度: 中等查看答案及解析
-
能正确表示下列反应的离子方程式是
A. 向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
B. 向次氯酸钙溶液通入SO2:Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO
C. 氢氧化钙溶液与碳酸氢镁溶液反应:Ca2++OH-+HCO3-=CaCO3↓+H2O
D. 在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑
难度: 简单查看答案及解析
-
检验SO2气体中是否混有CO2气体,可采用的方法是
A. 通过品红溶液
B. 通过澄清石灰水
C. 先通过NaOH溶液,再通过澄清石灰水
D. 先通过酸性KMnO4溶液,再通过澄清石灰水
难度: 中等查看答案及解析
-
在含2molH2SO4的浓硫酸中加入足量的锌粉,使其充分反应,下列推断中错误的是
①放出的气体除SO2外还有H2 ②只放出1molSO2气体 ③反应结束时转移4mol电子
A.① B.② C.②③ D.①②
难度: 困难查看答案及解析
-
久置在空气中不易变质的物质是
A、亚硫酸钠 B、硅酸钠 C、硫酸钠 D、漂白粉
难度: 简单查看答案及解析
-
下列关于物质性质的叙述中,正确的是( )
A.Cl2能与金属活动顺序表中大多数金属反应
B.N2是大气中的主要成分之一,雷雨时,可直接转化为NO2
C.硫是一种淡黄色的能溶于水的晶体,既有氧化性又有还原性
D.硅是应用广泛的半导体材料,常温下化学性质活泼
难度: 中等查看答案及解析
-
下列推断正确的是
A. SiO2是酸性氧化物,能与NaOH溶液反应
B. Na2O、Na2O2组成元素相同,与CO2反应产物也相同
C. CO、NO、NO2都是大气污染物气体,在空气中都能温室存在
D. 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分震荡后溶液显红色
难度: 简单查看答案及解析
-
下列反应中,其产物的颜色按红、红褐、淡黄、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧;
②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间
③FeCl3溶液中滴入KSCN溶液;
④无水硫酸铜放入医用酒精中。
A. ②③①④ B. ③②①④ C. ③①②④ D. ①②③④
难度: 中等查看答案及解析
-
把4.6g钠放入200mL0.1mol·L-1AlCl3溶液中,待其充分反应后,下列叙述中错误的是( )
A. Cl-的浓度几乎不变 B. 溶液变浑浊
C. 溶液中Al3+全部转化为AlO2- D. 溶液中存在最多的离子是Na+
难度: 中等查看答案及解析