-
在盛放浓硫酸的试剂瓶标签上应印有下列警示标记中的

难度: 简单查看答案及解析
-
下列化学实验操作或事故处理方法不正确的是
A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸
C.酒精灯着火时可用湿布扑灭
D.蒸馏时,温度计水银球应浸没在液体中
难度: 中等查看答案及解析
-
下列关于过滤操作的说法中,错误的是
A.玻璃棒下端要紧靠在三层滤纸处
B.滤纸边缘低于漏斗边缘,多余部分要剪去,并用蒸馏水润湿贴紧,不留气泡
C.过滤时将液体沿玻璃棒注入过滤器,并使液面高于滤纸边缘
D.漏斗下端紧靠烧杯内壁
难度: 中等查看答案及解析
-
在“粗盐提纯”的实验中,蒸发时正确的操作是
A.把浑浊的液体倒入蒸发皿内加热
B.开始析出晶体后再用玻璃棒搅拌
C.待水分完全蒸干后停止加热
D.蒸发皿中出现大量固体时即停止加热
难度: 中等查看答案及解析
-
在蒸馏实验中,下列叙述不正确的是
A.在蒸馏烧瓶中盛约1/3体积的自来水并放入几粒沸石
B.将温度计水银球插入自来水中
C.不可用酒精灯直接加热蒸馏烧瓶
D.收集蒸馏水时应弃去开始馏出的部分
难度: 中等查看答案及解析
-
现有三组实验:①除去混在植物油中的水;②回收碘的CCl4溶液中的CCl4;③用食用酒精浸泡中草药提取其中的有效成分。分离以上各混合液的正确方法依次为
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
难度: 中等查看答案及解析
-
下列实验操作:①用50 mL量筒量取5 mL蒸馏水;②称量没有腐蚀性固体药品时,把药品放在托盘上称量;③倾倒液体时试剂不对准容器口;④块状药品都要用药匙取用;⑤固体药品用广口瓶保存.其中不正确的是
A.①②③④ B.③④
C.②⑤ D.①②④⑤
难度: 中等查看答案及解析
-
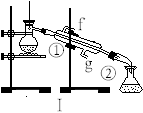
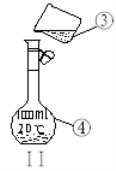
下列图示的四种实验操作名称从左到右依次是

A.过滤、蒸发、蒸馏、分液
B.过滤、蒸馏、蒸发、分液
C.蒸发、蒸馏、过滤、分液
D.分液、蒸馏、蒸发、过滤
难度: 中等查看答案及解析
-
检验某未知溶液中是否含有SO42-,下列操作最合理的是
A.加入HNO3酸化的Ba(NO3)2溶液
B.先加入HNO3酸化,再加Ba(NO3)2
C.加入盐酸酸化的BaCl2
D.先用盐酸酸化,若有沉淀,则过滤,滤液中再加BaCl2溶液
难度: 中等查看答案及解析
-
下列对于“摩尔”的理解正确的是
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔是物质的量的单位,简称摩,符号为mol
C.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D.国际上规定,0.012 kg碳原子所含有的碳原子数目为1 mol
难度: 简单查看答案及解析
-
设NA为阿伏伽德罗常数的值,下列有关说法不正确的是
A.标准状况下,48gO3含有的氧原子数为3NA
B.1molOH-离子中含电子数目为10NA
C.0.5L 0.2mol·L-1的NaCl溶液中含有的Na+数是0.1NA
D.常温常压下,33.6LCO中含有的原子数是3NA
难度: 中等查看答案及解析
-
下列说法中正确的是
A.在一定温度和压强下,各种气态物质体积大小由构成气体分子大小决定
B.在一定温度和压强下,各种气态物质体积的大小由构成气体的分子数决定
C.不同的气体,若体积不同,则它们所含的分子数一定不同
D.气体摩尔体积是指1mol任何气体所占的体积约为22.4L
难度: 中等查看答案及解析
-
在同温同压下,分子数目相同的任意两种气体,下列说法正确的是
A.体积都是22.4L B.密度相同
C.所占的体积相同 D.原子数目一定相同
难度: 中等查看答案及解析
-
如果1g H2O中含有m个H原子,则阿伏加德罗常数为
A.18m B.9m C.2m D.m/9
难度: 中等查看答案及解析
-
关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是
A.①②③④ B.②③
C.①②④ D.②③④
难度: 简单查看答案及解析
-
下列说法正确的是
A.选择萃取剂将碘从碘水中萃取出来,这种萃取剂应具备的性质是不溶于水,且比水的密度大。
B.选择萃取剂将碘从碘水中萃取出来,这种萃取剂应具备的性质是不溶于水,且比水的密度小。
C.在使用分液漏斗进行分液时,上层液体经漏斗下口放出。
D.选择萃取剂将碘从碘水中萃取出来,碘在四氯化碳中的溶解度比在水中的溶解度大
难度: 中等查看答案及解析
-
下列有关0.2mol·L-1 BaCl2溶液的说法不正确的是
A.500mL溶液中Cl-离子浓度为0.2mol·L-1
B.500mL溶液中Ba2+离子浓度为0.2mol·L-1
C.500mL溶液中Cl-离子总数为0.2NA
D.500mL溶液中Ba2+和Cl-离子总数为0.3NA
难度: 中等查看答案及解析
-
某同学想用实验证明FeCl3溶液显黄色不是Cl-造成的,下列实验中无意义的是
A.观察KCl溶液没有颜色
B.加水稀释后FeCl3溶液黄色变浅
C.向FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失
D.向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失
难度: 中等查看答案及解析
-
一定量的质量分数为14%的氢氧化钾溶液,若将其蒸发掉50 g水后,其溶质质量分数恰好扩大一倍,体积变为62.5 mL,则浓缩后溶液的物质的量浓度为
A.2.2 mol/L B.4 mol/L
C.5 mol/L D.6.25 mol/L
难度: 中等查看答案及解析
-
下图锥形瓶中装满了c mol·Lˉ1的Na2SO4溶液,经测定其中含有a mol SO42-,则锥形瓶容积为

A.
L B.
L C.acL D.2acL
难度: 中等查看答案及解析
-
已知N2、CO2的混合气体的质量共9.6克,标准状况下,体积为6.72L,则该混合气体中N2和CO2的体积比为
A.3:1 B.1:3 C.2:3 D.1:2
难度: 中等查看答案及解析
-
A、B、C、D可能是Na2CO3、HCl、AgNO3、BaCl2四种无色溶液中的某一种,把它们两两混合后产生的现象如下表,则A、B、C、D四种物质按顺序排列正确的是
反应物
A+B
A+C
B+C
C+D
B+D
现象
白↓
白↓
白↓
白↓
无色↑
A.BaCl2、 Na2CO3、 AgNO3、 HCl
B.Na2CO3、 HCl、 AgNO3、 BaCl2
C.HCl、 AgNO3、 Na2CO3、 BaCl2
D.AgNO3、 Na2CO3、 BaCl2、 HCl
难度: 中等查看答案及解析
-
某种气体的摩尔质量为M g·mol-1,将标况下的该气体V L溶解在1000 g水中,该气体不与水反应,所得溶液密度为ρ g·cm-3,则所得溶液中溶质的物质的量浓度为 ( ) mol·L-1
A.V/22.4 B.V ρ/(MV+22400)
C.V ρ/22400 D.1000V ρ/(MV+22400)
难度: 中等查看答案及解析