-
将纯水加热至较高温度,下列叙述正确的是( )
A.水的离子积变大、pH变小、呈酸性
B.水的离子积变大、pH变小、呈中性
C.水的离子积变小、pH变大、呈碱性
D.水的离子积不变、pH不变、呈中性难度: 中等查看答案及解析
-
下列关于常见有机物的说法不正确的是( )
A.乙烯和苯都能与溴水反应
B.乙酸和油脂都能与氢氧化钠溶液反应
C.糖类和蛋白质都是人体重要的营养物质
D.乙烯和甲烷可用酸性高锰酸钾溶液鉴别难度: 中等查看答案及解析
-
配制100mL 1.0mol/LNa2CO3溶液,下列操作正确的是( )
A.称取10.6g无水碳酸钠,加入100mL容量瓶中,加水溶解、定容
B.称取10.6g无水碳酸钠,加入100mL蒸馏水,搅拌、溶解
C.转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中
D.定容后,塞好瓶塞,反复倒转、摇匀难度: 中等查看答案及解析
-
下列反应的离子方程式书写正确的是( )
A.氯化铝溶液中加入过量氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O
B.氧化钠与水反应:O2-+H2O=2OH-
C.碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O
D.氯化亚铁溶液中通入氯气:2Fe2++Cl2=2Fe3++2Cl-难度: 中等查看答案及解析
-
下列类型的反应,一定发生电子转移的是( )
A.化合反应
B.分解反应
C.置换反应
D.复分解反应难度: 中等查看答案及解析
-
已知汽车尾气无害化处理反应为2NO(g)+2CO(g)⇌N2(g)+2CO2(g),下列说法不正确的是( )
A.升高温度可使该反应的逆反应速率降低
B.使用高效催化剂可有效提高正反应速率
C.反应达到平衡后,NO的反应速率保持恒定
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡难度: 中等查看答案及解析
-
下列说法正确的是( )
A.向0.1mol/LNa2CO3溶液中加酚酞,溶液变红色
B.Al3+、NO3-、Cl-、CO32-、Na+可大量共存于pH=2的溶液中
C.乙醇和乙酸都能溶于水,都是电解质
D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.直径介于1nm~10nm之间的微粒称为胶体
B.电泳现象可证明胶体属于电解质溶液
C.利用丁达尔效应可以区别溶液与胶体
D.胶体粒子很小,可以透过半透膜难度: 中等查看答案及解析
-
25℃、101kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,则下列热化学方程式正确的是( )
A.C(s)+O2(g)=CO(g);△H=-393.5kJ/mol
B.2H2(g)+O2(g)=2H2O(g);△H=+571.6kJ/mol
C.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-890.3kJ/mol
D.C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l);△H=-1400kJ/mol
难度: 中等查看答案及解析
-
“脚印”、“笑脸”、“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关.下列说法中正确的是( )
A.非金属单质燃烧时火焰均为无色
B.NaCl与Na2CO3灼烧时火焰颜色相同
C.焰色反应均应透过蓝色钴玻璃观察
D.只有金属单质灼烧时火焰才有颜色难度: 中等查看答案及解析
-
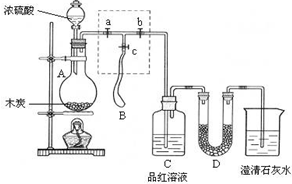
实验室制Cl2的反应为4HCl(浓)十MnO2
MnCl2+Cl2↑+2H2O.下列说法错误的是( )
A.还原剂是HCl,氧化剂是MnO2
B.每生成1mol Cl2,转移电子的物质的量为2mol
C.每消耗1mol MnO2,起还原剂作用的HCl消耗4mol
D.生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质难度: 中等查看答案及解析
-
关于Na元素和F元素的叙述正确的是( )
A.原子半径Na<F
B.原子序数Na>F
C.原子的电子层数Na<F
D.原子最外层电子数Na>F难度: 中等查看答案及解析
-
实验室常采用点滴板来完成部分实验,这样既可以节约药品的用量,又便于观察实验现象.图中所示的实验,点滴板上描述的现象正确的是( )
①装有铜片的孔穴中溶液呈蓝色;②装有胆矾的孔穴中固体的颜色变白;③装有铁片的孔穴中溶液呈浅绿色;④装有铁片的孔穴中溶液呈黄色;⑤装有蛋清溶液的孔穴中呈黄色.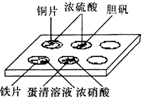
A.①④
B.②③
C.①⑤
D.②⑤难度: 中等查看答案及解析
-
下列表述正确的是( )
①人造刚玉熔点很高,可用作高级耐火材料,主要成分是二氧化硅;
②化学家采用玛瑙研钵磨擦固体反应物进行无熔剂合成,玛瑙的主要成分是硅酸盐;
③提前建成的三峡大坝使用了大量水泥,水泥是硅酸盐材料;
④夏天到了,游客佩戴由添加氧化亚铜的二氧化硅玻璃璃制作的变色眼镜来保护眼睛;
⑤太阳能电池可采用硅材料制作,其应用有利于环保、节能.
A.①②③
B.②④
C.③④⑤
D.③⑤难度: 中等查看答案及解析
-
下列关于氨气的说法正确的是( )
A.氨气的检验方法为:将沾有浓盐酸的玻璃棒或者用沾有湿润的蓝色石蕊试纸玻璃棒靠近容器口
B.氨水能导电,所以NH3是电解质
C.制取氨气可以使用NH4Cl受热分解
D.用向下排空气法收集NH3难度: 中等查看答案及解析
-
在强碱溶液中,下列各组离子能够大量共存的是( )
A.Mg2+、Ca2+、HCO3-、Cl-
B.Na+、Al3+、ClO-、SO42-
C.K+、Fe2+、SO42-、Br-
D.ClO-、K+、Cl-、SO42-难度: 中等查看答案及解析
-
铝分别与足量的氢氧化钠和稀盐酸溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的NaOH和HCl物质的量之比为( )
A.2:1
B.3:1
C.1:1
D.1:3难度: 中等查看答案及解析
-
某有机物A的结构简式如图所示,下列叙述正确的是( )

A.A分子中最多有10个原子处于同一平面内
B.1molA物质能与6molH2在一定条件下发生加成反应
C.1mol该物质最多能与3molNaOH反应
D.该物质能发生加成反应、水解反应、酯化反应,但不能发生消去反应难度: 中等查看答案及解析