-
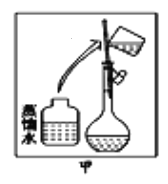
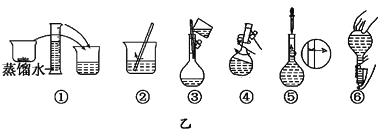
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离这三组溶液用到的方法分别是( )
A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
难度: 中等查看答案及解析
-
能够直接鉴别BaCl2、NaCl、Na2CO3三种溶液的试剂是 ( )
A. AgNO3溶液 B. 稀硫酸 C. 稀盐酸 D. 稀硝酸
难度: 简单查看答案及解析
-
进行过滤操作应选用的一组仪器是( )
A. 滤纸、烧杯、试管、漏斗、玻璃棒
B. 烧杯、酒精灯、试管、漏斗
C. 漏斗、玻璃棒、烧杯、铁架台、滤纸
D. 玻璃棒、滤纸、蒸馏烧瓶、漏斗、铁架台
难度: 简单查看答案及解析
-
下列实验仪器不宜直接用来加热的是( )
A. 试管 B. 坩埚 C. 蒸发皿 D. 烧杯
难度: 简单查看答案及解析
-
下列事故处理不正确的是
A. 眼睛里不慎溅进药品,应立即用手揉眼睛,以便产生眼泪挤出药液
B. 将CO中毒者移到通风处抢救
C. 不慎碰倒酒精灯,洒出的酒精在桌面上燃烧时,立即用湿抹布扑盖
D. 浓硫酸溅到皮肤上,先用大量水冲洗,然后涂抹稀碳酸氢钠溶液
难度: 困难查看答案及解析
-
下列溶液中Cl-浓度与50 mL 1 mol·L-1 AlCl3溶液中Cl-浓度相等的是 ( )
A. 150 mL 1 mol·L-1的NaCl溶液 B. 75 mL 1 mol·L-1的FeCl3溶液
C. 25 mL 2 mol·L-1的KCl溶液 D. 75 mL 2 mol·L-1 NH4Cl溶液
难度: 中等查看答案及解析
-
装运乙醇的包装箱应贴的图标是( )
A.
 B.
B. 
C.
 D.
D. 
难度: 简单查看答案及解析
-
如图所示的五种尾气吸收装置中,适合吸收极易溶于水的气体,且能防止产生倒吸现象(溶液进入气体发生装置中)的是 ( )
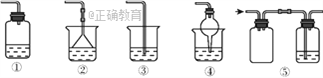
A. ②④⑤ B. ①②④ C. ①②③ D. ①②④⑤
难度: 中等查看答案及解析
-
蒸发操作中必须用到蒸发皿,下面对蒸发皿的操作中正确的是
A. 将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热
B. 将蒸发皿放置在铁架台的铁圈上直接用酒精灯火焰加热
C. 将灼热的蒸发皿直接放在冷水中冲洗
D. 将灼热的蒸发皿用手拿离火焰,直接放在实验台上
难度: 中等查看答案及解析
-
萃取碘水中的碘,可用的萃取剂是 ①四氯化碳 ②苯 ③酒精
A. 只有① B. ①和③ C. ①和② D. ①②③
难度: 中等查看答案及解析
-
下列各组混合物中,能用分液漏斗进行分离的是
A. 碘和四氯化碳 B. 水和四氯化碳 C. 酒精和水 D. 酒精和汽油
难度: 中等查看答案及解析
-
在蒸馏实验中,下列叙述不正确的是
A. 在蒸馏烧瓶中盛约1/3 体积的自来水,并放入几粒沸石
B. 蒸馏时加入沸石或碎瓷片的目的是防爆炸
C. 冷水从冷凝管下口入,上口出
D. 制作蒸馏水的主要仪器是:烧瓶、酒精灯、铁架台、冷凝管、锥形瓶
难度: 困难查看答案及解析
-
“粗盐提纯”实验中,下列操作正确的是
A. 过滤时用玻璃棒搅拌漏斗内的液体,以加速过滤
B. 蒸发到析出晶体时才需要用玻璃棒搅拌
C. 当蒸发皿中出现较多晶体时就应停止加热
D. 待溶液蒸干后即可停止加热
难度: 中等查看答案及解析
-
为了除去粗盐中Ca2+、Mg2+、SO
及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是( )
①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
A. ②④⑤①③ B. ④②⑤①③ C. ②⑤④①③ D. ⑤②④③①
难度: 简单查看答案及解析
-
实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯②固定铁圈的位置③放上蒸发皿④加热搅拌⑤停止加热、余热蒸干,其中正确的操作顺序是( )
A. ①②③④ B. ①②③④⑤
C. ②③①④⑤ D. ②①③④⑤
难度: 中等查看答案及解析
-
除去溶液中溶解的杂质,下列做法中不正确的是(括号内的物质为杂质)( )
A. NaCl溶液(Na2SO4)加入适量Ba(NO3)2溶液后,过滤
B. NaNO3溶液(NaCl)加入适量AgNO3溶液后,过滤
C. NaCl溶液(CaCl2)加入适量Na2CO3溶液后,过滤
D. NaCl溶液(碘I2)加入四氯化碳后,分液
难度: 简单查看答案及解析
-
下列对“摩尔”的理解正确的是
A. 摩尔是国际科学界建议采用的一种物理量
B. 摩尔是物质的量的单位,简称摩,符号mol
C. 摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D. 国际上规定,0.012kg C原子所含的碳原子数为1mol
难度: 简单查看答案及解析
-
下列说法正确的是
A. 2 mol的大米 B. 0.3 mol HCl C. 0.1 mol氢 D. 4 mol的氧元素
难度: 中等查看答案及解析
-
下列说法中正确的是 ( )
A. 氢氧化钠的摩尔质量为40克
B. 1摩尔氧原子的质量就是氧的相对原子质量
C. H2SO4的摩尔质量为96g·mol-1
D. 1 mol CO2的质量以克为单位时,在数值上等于CO2的相对分子质量
难度: 简单查看答案及解析
-
下列有关气体摩尔体积的描述中正确的是 ( )
A. 单位物质的量的气体所占的体积就是气体摩尔体积
B. 通常状况下的气体摩尔体积约为22.4L
C. 标准状况下的气体摩尔体积约为22.4L
D. 相同物质的量的气体摩尔体积也相同
难度: 中等查看答案及解析
-
将30mL5mol/L NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为( )
A. 0.3 mol/L B. 3 mol/L C. 0.15 mol/L D. 1.5 mol/L
难度: 中等查看答案及解析
-
某气体在标准状况下的密度为1.25 g / L,该气体的相对分子质量为( )
A. 44 B. 28 C. 32 D. 16
难度: 简单查看答案及解析
-
下列溶液中溶质的物质的量浓度为1 mol·L-1的是 ( )。
A. 将58.5 g NaCl溶解于1 L水中配成的溶液
B. 将80 g SO3溶于水并配成1 L溶液
C. 将0.5 mol·L-1的NaNO3溶液100 mL加热蒸发掉50 g水的溶液
D. 含K+为2 mol的K2SO4溶液
难度: 简单查看答案及解析
-
某硫酸溶液的密度为1.48g/cm3,溶质质量分数为49%.该溶液的溶质的物质的量浓度是( )
A. 0.0074mol/L B. 0.74mol/L C. 7.4mol/L D. 4.9mol/L
难度: 简单查看答案及解析
-
若某原子的摩尔质量是
g·mol-1,则一个该原子的真实质量是( )
A.
g B.
g C.
g D.
g
难度: 中等查看答案及解析
-
在标准状况下,若
L甲烷中含有的氢原子个数为
,则阿伏加德罗常数可表示为( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
已知空气的平均相对分子质量是29。现有一真空瓶质量为
,该瓶充入空气后质量为
。在相同状况下,若改为充入某气体A时,总质量为
。则A的相对分子质量是
A.
×29 B.
×29 C.
×29 D.
×29
难度: 困难查看答案及解析
-
相同条件下,相同质量的甲烷、二氧化碳、硫化氢、氮气四种气体,其体积、密度、分子数、原子数从小到大排列不正确的是()
A. 体积:二氧化碳、硫化氢、氮气、甲烷
B. 密度:甲烷、氮气、硫化氢、二氧化碳
C. 分子数:二氧化碳、硫化氢、氮气、甲烷
D. 原子数:甲烷、氮气、硫化氢、二氧化碳
难度: 中等查看答案及解析