-
以下是一些常用的危险品标志,装运浓硫酸的包装箱应贴的图标是( )

难度: 简单查看答案及解析
-
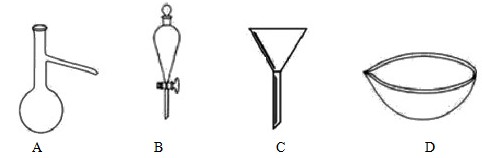
下列实验操作有错误的是( )
A、用CCl4萃取溴水中的溴分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B、蒸馏中,冷却水应从冷凝管的下口通入,上口流出
C、用焰色反应检验Na+时,用玻璃棒蘸取试样置于火焰上灼烧观察火焰颜色
D、蒸发结晶时,当加热到有大量固体出现时停止加热,用余热蒸干
难度: 简单查看答案及解析
-
下列对实验过程的评价正确的是( )
A、某固体中加入稀盐酸,产生了无色无味的气体,证明该固体一定是CaCO3
B、某溶液中加入氢氧化钠溶液并加热,产生了能使湿润的红色石蕊试纸变蓝的气体,该溶液中一定含有NH4+
C、某溶液中滴入氯化钡溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含有SO42-
D、验证NaOH溶液中是否混有Cl-,先加稀盐酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明有Cl-
难度: 简单查看答案及解析
-
下列有关物质的分类正确的是( )
A. 混合物:空气 有色玻璃 水银 B. 碱:Ba(OH)2 Cu2(OH)2CO3 NH3•H2O
C. 盐:硫酸钠 氯化铵 纯碱 D. 氧化物:H2O CO CH3CH2OH
难度: 简单查看答案及解析
-
下列反应中,属于氧化还原反应的是( )
A、SO2+2KOH=K2SO3+ H2O B、CaCO3
CaO+CO2↑
C、Na2CO3+CaCl2===CaCO3↓+2NaCl D、Fe+2FeCl3= 3FeCl2
难度: 简单查看答案及解析
-
下列说法正确的是( )
A、酸性氧化物就是非金属氧化物
B、纯净物与混合物的区别是看是否只含有一种元素
C、强弱电解质的区别是溶液的导电能力的大小
D、氧化还原反应的判断依据是反应过程中元素的化合价是否发生变化
难度: 简单查看答案及解析
-
用NA表示阿伏德罗常数,下列叙述正确的是( )
A、标准状况下,22.4 L H2O含有的分子数为1 NA
B、常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02 NA
C、通常状况下,1 NA 个CO2分子占有的体积为22.4 L
D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为1 NA
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A、6.02×1023mol-1叫做阿伏伽德罗常数
B、NH3的摩尔质量为17 g
C、3.01×1023个SO2分子的质量为32g
D、标准状况下,1 mol任何物质体积均为22.4 L
难度: 简单查看答案及解析
-
已知3.01×1023个X气体分子的质量为16g,则X气体的相对分子质量是( )
A、32 B、16 C、32 g /mol D、16 g
难度: 简单查看答案及解析
-
0.5 L 1 mol/L FeCl3溶液与0.2 L 1 mol/L KCl溶液中的Cl-的物质的量浓度之比为( )
A、5:2 B、3:1 C、15:2 D、5:2
难度: 简单查看答案及解析
-
下列关于胶体的叙述不正确的是( )
A、光线透过胶体时,胶体中可发生丁达尔效应
B、用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
C、Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
D、胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间
难度: 简单查看答案及解析
-
下列关于电解质的叙述中错误的是( )
A、在水溶液中和熔融状态下均不导电的化合物叫做非电解质
B、电解质、非电解质都是指化合物,单质和混合物均不属于此范畴
C、其水溶液导电的物质不一定是电解质
D、纯水的导电性很差,所以水不是电解质
难度: 简单查看答案及解析
-
能正确表示下列化学反应的离子方程式的是 ( )
A、实验室用大理石和稀盐酸制取CO2 :2H++CO32- = CO2↑+H2O
B、硫酸铜与氢氧化钡溶液反应:Ba2++SO42- = BaSO4 ↓
C、Fe(OH)3与盐酸反应:H++ OH- = H2O
D、Fe2O3溶于稀硫酸: 6H++ Fe2O3 = 2 Fe 3++3H2O
难度: 简单查看答案及解析
-
某无色溶液既可能是强酸性又可能是强碱性,在该溶液中一定能大量共存的离子是 ( )
A、H+ Na+ NO3- SO42- B、Na+ CO32- Cu2+ Cl-
C、K+ Na+ Cl- SO42- D、K+ Cl- Ba2+ HCO3-
难度: 简单查看答案及解析
-
一定温度和压强下,2体积AB2气体和1体积B2气体化合生成2体积气态化合物,则该化合物的化学式为( )
A、AB3 B、AB2 C、A3B D、A2B3
难度: 简单查看答案及解析
-
在相同体积、相同物质的量浓度的一元酸溶液中,一定相等的是( )
A、溶质的质量 B、溶质的质量分数
C、溶质的物质的量 D、氢离子的物质的量浓度
难度: 简单查看答案及解析