-
用氯化钠固体配制一定质量分数的氯化钠溶液,必须使用的一组仪器是
A.天平、烧杯、量筒、玻璃棒、药匙
B.天平、烧杯、漏斗、蒸发皿、玻璃棒
C.天平、烧杯、量筒、铁架台、药匙
D.天平、集气瓶、漏斗、蒸发皿、玻璃棒
难度: 简单查看答案及解析
-
高钙奶粉中的“钙”一般是指
A.原子 B.分子 C.离子 D.元素
难度: 简单查看答案及解析
-
微观解释不正确的是
A.酒精挥发﹣﹣分子不断运动
B.二氧化碳气体制成干冰﹣﹣分子体积变小
C.18g水中大约有6.02×1023个水分子﹣﹣分子质量很小
D.50mL酒精和50mL水混合后总体积小于100mL﹣﹣分子间有间隔
难度: 简单查看答案及解析
-
以下变化中属于化学变化的是
A.玉石刻章
B.食物腐烂
C.充有氖气的霓虹灯发出红光
D.高压锅压力过大而爆炸
难度: 简单查看答案及解析
-
属于混合物的是
A.蒸馏水 B.氧气 C.石灰水 D.氯酸钾
难度: 简单查看答案及解析
-
下列化学实验基本操作正确的是




A.点燃酒精灯 B.取用液体 C.读取体积 D.过滤
难度: 简单查看答案及解析
-
下列物质中,属于溶液的是
A.牛奶 B.豆浆 C.冰水 D.糖水
难度: 简单查看答案及解析
-
规范的操作是化学实验成功的保障.下列实验操作正确的是
A.测定溶液的pH时,将试纸直接放入待测液中
B.固体药品都可以直接放在天平的托盘上称量
C.配制稀硫酸时,将浓硫酸沿烧杯壁慢慢加入量筒中,并不断搅拌
D.点燃可燃性气体之前先检验气体的纯度
难度: 简单查看答案及解析
-
Bi4Ge3012是我国研制的一种闪烁晶体材料,曾用于诺贝尔获得者丁肇中的实验.闪烁晶体中的锗(Ge)化合价为+4价,闪烁晶体中铋(Bi)的化合价为
A.+2 B.+3 C.+4 D.+5
难度: 简单查看答案及解析
-
下列化学用语表示正确的是
A.2个氢分子﹣2H
B.3个氧原子﹣O3
C.水分子﹣H2O2
D.+1价钠元素﹣
难度: 简单查看答案及解析
-
关于空气的说法正确的是
A.空气是由空气分子构成的
B.空气中的氮气、氧气经混合,它们的化学性质都已改变
C.分离液态空气法制氧气属于分解反应
D.空气是由氮气、氧气等组成的混合物
难度: 简单查看答案及解析
-
如图所示是生活中一些常见物质的pH,根据图示判断,下列说法正确的是

A.酱油呈碱性
B.牙膏呈酸性
C.胃酸过多的人可多喝玉米粥
D.西瓜汁的酸性要比苹果汁的酸性强
难度: 简单查看答案及解析
-
下列现象可用同一化学原理解释的是
①久置的石灰水,液面上出现一层硬壳状薄膜;
②向澄清石灰水中,通过吸管不断吹气,石灰水变浑浊;
③为了使石灰浆刷过的墙壁快点晾干,在室内生起一个火盆,开始时墙壁反而更潮湿;
④向紫色石蕊试液中通入二氧化碳气体,试液变红.
A.①②③ B.①②④ C.①③④ D.②③④
难度: 简单查看答案及解析
-
下列现象不能用质量守恒定律解释的是
A.将2g氢气在20g氧气中燃烧,生成18g水
B.将20mL酒精与20mL水混合,总体积小于40mL
C.将3克的木炭在10克氧气中充分燃烧,生成二氧化碳的质量为11克
D.铁丝在氧气中燃烧后质量增加
难度: 简单查看答案及解析
-
某同学过滤含有泥沙的水,滤液仍然浑浊,其原因可能是
A.滤纸与漏斗之间有气泡
B.倾倒液体时液面高于滤纸边缘
C.过滤时玻璃棒靠在三层滤纸的一边
D.漏斗的下端未靠在烧杯壁上
难度: 简单查看答案及解析
-
当前,世界己经迈向了“低碳”时代,选择“低碳”既是一种生活方式也是一种生存责任.适应形势发展,多市推广使用节能减排的双燃料公交车.如图为公交车燃料主要成分完全燃烧的化学反应的微观示意图.则下列说法中正确的是
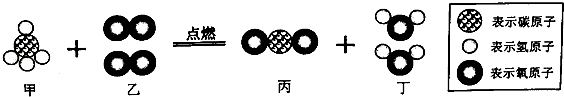
A.该反应中分子和原子的种类都发生了改变
B.物质甲的化学式是CH4
C.甲、乙两物质参加反应的质量比为1:2
D.图示反应属于化合反应
难度: 中等查看答案及解析
-
酒精灯的火焰太小时,将灯芯拨得松散一些,可能火焰更旺,其原理是
A.降低可燃物的着火点
B.提高可燃物的着火点
C.增加空气中氧气含量
D.增大可燃物与空气的接触面积
难度: 简单查看答案及解析
-
粗盐提纯实验中,经分析发现测得的纯度偏低,不可能的原因是
A.食盐没有全部溶解即过滤
B.蒸发过程中晶体飞溅
C.蒸发后所得精盐很潮湿
D.蒸发皿上沾有精盐没有全部转移到称量纸上
难度: 中等查看答案及解析
-
以下是 KCl的部分溶解度数据,下列说法中正确的是
温度(℃)
0
20
40
60
溶解度(g/100g水)
27.6
34.0
40.0
45.5
A.KCl饱和溶液中不能再溶解其他物质
B.20℃时,100g KCl饱和溶液中含KCl 34.0 g
C.20℃的KCl溶液的浓度一定小于 40℃的KCl饱和溶液的浓度
D.60℃时,将一定质量分数KCl溶液降温到40℃,一定有晶体析出
难度: 简单查看答案及解析
-
金属插入溶液中,溶液质量会增加的是
A.铜片插入硫酸铝溶液中 B.铁片插入硫酸铜溶液中
C.铜片插入硝酸银溶液中 D.锌片插入硫酸铜溶液中
难度: 中等查看答案及解析