-
下列关于空气的说法正确的是
A.空气的主要成分是氮气和氧气
B.空气中氮气体积分数约为21%
C.空气中PM2.5含量高说明空气质量好
D.洁净的空气是纯净物
难度: 简单查看答案及解析
-
下列过程中涉及化学变化的是
A. 用聚乙烯塑料制得食品袋 B. 用食盐制得纯碱
C. 将液态空气分离制得氧气 D. 将石油分离制得汽油
难度: 中等查看答案及解析
-
“促进可持续的生活方式”,核心是倡导良好的生活习惯。小明的下列做法符合这一主题的是( )
A. 去超市用布袋购物
B. 网上购买大量闲置物品
C. 节假日随父母出游,经常开私家车
D. 外出就餐,超量点菜
难度: 简单查看答案及解析
-
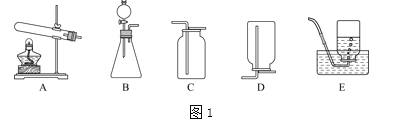
下列实验操作符合安全要求的是( )

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
化学与生活密切相关,下列叙述中正确的是( )
A.胃酸过多的人应少饮葡萄汁(葡萄汁的PH为3.5~4.5)
B.为了个人卫生,应全部使用一次性的木筷和餐盒
C.人体缺锌会引起生长发育缓慢,因此锌元素摄入得越多越好
D.铵态氮肥与草木灰混合使用可以明显提高肥效
难度: 中等查看答案及解析
-
材料在人类生产、生活中有着重要的作用。下列有关材料的说法中正确的是
A. 塑料是最常见的有机合成材料,具有密度小、耐腐蚀、易加工等优点
B. 棉花和羊毛的主要成分都是蛋白质
C. 日常生活中使用的有机玻璃、腈纶、蚕丝等都属于合成纤维
D. 钛合金、玻璃钢、碳纤维复合材料等都属于新型有机合成材料
难度: 中等查看答案及解析
-
下列叙述中正确的是( )
①化学变化不但生成其他物质,而且还伴随着能量的变化
②人类利用的能量都是通过化学反应获得的
③燃料作为重要的能源,对人类社会的发展非常重要
④可燃物在任何条件下燃烧都会发生爆炸
⑤化学反应过程中都会发生放热现象
A. ①③ B. ②③ C. ④⑤ D. ②⑤
难度: 中等查看答案及解析
-
物质的用途与性质密切相关。下列说法正确的是
A. 小苏打能作发酵粉,是因为小苏打能与面粉反应
B. 洗洁精能洗去碗筷上的油污,是因为油污能溶于洗洁精
C. 浓硫酸可用作干燥剂,是因为浓硫酸具有吸水性
D. 液氧可用于火箭发射,是因为氧气具有可燃性
难度: 中等查看答案及解析
-
钒被誉为“合金中的维生素”,钒元素的部分信息如下图。下列有关钒的说法正确的是
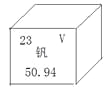
A. 属于非金属元素 B. 原子序数为23
C. 原子核外电子数为28 D. 相对原子质量为50.94g
难度: 中等查看答案及解析
-
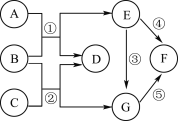
下图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合。下列说法中不正确的是
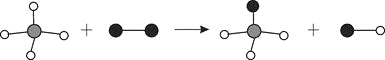
A. 图示有4种分子 B. 图示反应前后原子个数不变
C. 图示发生了复分解反应 D. 图示产物为混合物
难度: 中等查看答案及解析
-
下列各组物质的溶液不用其他试剂无法鉴别的是( )
A. H2SO4 NaCl Na2CO3 CaCl2 B. HCl NaOH CuSO4 MgSO4
C. Na2CO3 K2SO4 BaCl2 HCl D. NaNO3 HCl CaCl2 KOH
难度: 困难查看答案及解析
-
下列图像有关量的化趋势不能正确反映其对应操作的是
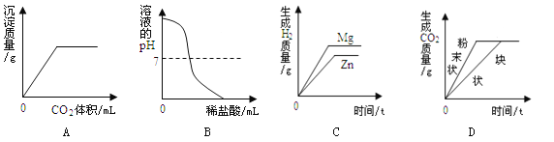
A. 在一定量的CaCl2溶液中通入CO2气体
B. 向NaOH溶液中逐滴加入稀盐酸
C. 等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应
D. 等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应
难度: 困难查看答案及解析
-
某混合气体可能含有CO、CO2、CH4和HCl中的一种或几种,为了确定其成分,将混合气体按如图所示装置进行实验(假设各步均充分反应或吸收),结果装置A中澄清的石灰水不变浑浊,但混合气体的体积明显减小;装置D增重1.8 g;装置E增重2.2 g。下列关于该混合气体成分的分析中,错误的是

A. 一定不含CO2,一定含HCl B. 一定含CH4,一定不含CO
C. 可能只含CH4和HCl D. 可能含CO2
难度: 中等查看答案及解析