-
下列说法正确的是
A.非金属氧化物一定为酸性氧化物
B.化合反应一定是有单质参加反应
C.向煮沸的 1 mol·L-1 NaOH 溶液中滴加 FeCl3 饱和溶液制备 Fe(OH)3 胶体
D.医疗上的血液透析利用了胶体的性质
难度: 中等查看答案及解析
-
化学与生产、生活密切相关。下列说法错误的是
A.Cl2、ClO2、漂白粉都可用于自来水的杀菌消毒
B.CO2、CH4 气体的大量排放会造成温室效应的加剧
C.化石燃料的直接利用,促进了“低碳”经济的发展
D.市售的加钙盐、加碘盐,这里的“钙”、“碘”指的是元素
难度: 中等查看答案及解析
-
下列化工生产过程中所发生的反应不属于氧化还原反应的是
A.用氯气和消石灰制漂白粉
B.用氢气和氮气合成氨
C.用铁矿石炼铁
D.用石灰石生成生石灰
难度: 中等查看答案及解析
-
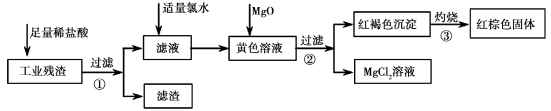
制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制得。用以上两种方法都可制得的氯化物是
A.AlCl3 B.FeCl3 C.FeCl2 D.CuCl2
难度: 中等查看答案及解析
-
下列物质的分类正确的是
A.CaO、H2O、C2H5OH均为氧化物
B.H2SO4、H3PO4、HNO3均为酸
C.Ca(OH)2、Cu2(OH)2CO3均为碱
D.空气、CuSO4·5H2O、碘酒均为混合物
难度: 简单查看答案及解析
-
下列物质的水溶液能导电,但属于非电解质的是
A.H2SO4 B.Cl2 C.NaAlO2 D.SO2
难度: 简单查看答案及解析
-
下列变化中,需加氧化剂才能实现的是
A.NaClO →NaCl B.C → CO2
C.Fe2O3→Fe D.CaO→Ca(OH)2
难度: 简单查看答案及解析
-
下列物质不能通过化合反应生成的是
A.NaOH B.NaHCO3 C.FeCl2 D.Al(OH)3
难度: 简单查看答案及解析
-
下列物质中既能跟氢氧化钠溶液反应, 又能跟稀盐酸反应的是
①Al2O3 ②Al(OH)3 ③(NH4)2CO3 ④NaHCO3 ⑤BaCl2
A.③④⑤ B.②③④⑤ C.①②③④ D.全部
难度: 中等查看答案及解析
-
用 NA 表示阿伏加德罗常数的值,下列叙述正确的是
A.1molCl2 与足量 Fe 反应,转移的电子数为 3NA
B.在常温常压下,1.7g NH3 含有的原子数为 0.4NA
C.标准状况下,11.2 L 水中含有的原子数是 1.5NA
D.0.2 mol∙L-1 的 Na2SO4 溶液中含 Na+数目为 0.4NA
难度: 中等查看答案及解析
-
能证明 SO2 具有漂白性的是
A.品红溶液中通入 SO2 气体,溶液红色消失
B.溴水中通入 SO2 气体后,溶液褪色
C.滴入酚酞的 NaOH 溶液中通入 SO2 气体,红色消失
D.酸性 KMnO4 溶液中通入 SO2 气体后,溶液褪色
难度: 中等查看答案及解析
-
下列说法中正确的是
A.标准状况下,11.2 L N2和17 g NH3中所含有的N原子数相同
B.9 g H2O和0.5 mol O2中含的原子数相同
C.20℃时,相同体积的N2、O2一定含有相同的分子数
D.在常温常压下,20 mL CH4与60 mL O2所含的原子个数比为1∶3
难度: 中等查看答案及解析
-
下列叙述不正确的是
A.含金属元素的离子一定是阳离子
B.应用蒸馏的方法,可以分离沸点相差较大的液体混合物
C.氯水和过氧化钠都具有漂白作用,其漂白原理相似
D.高炉炼铁时,还原铁矿石的还原剂为一氧化碳
难度: 中等查看答案及解析
-
足量的两份铝粉分别与等体积的盐酸和NaOH溶液反应,同温同压下产生的气体体积比为1:1,则盐酸和NaOH溶液的物质的量浓度之比为
A.2:3 B.3:1 C.1:2 D.1:1
难度: 中等查看答案及解析
-
常温下,某无色透明的溶液中,下列各组离子能够大量共存的是
A.H+、Na+、Cl-、CO32- B.Ba2+、Na+、SO42-、Cl-
C.MnO4- 、K+ 、I- 、H+ D.Mg2+ 、Cl-、NO3- 、H+
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
B.硫酸氢钠溶液中加入足量的烧碱溶液:HSO4-+OH- = SO42-+H2O
C.过氧化钠与水反应:2O22-+2H2O = 4OH-+O2↑
D.澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2 ===CaCO3↓+H2O
难度: 中等查看答案及解析
-
下列叙述正确的是
A.将40 g NaOH溶于1L水中,所得NaOH溶液的浓度为1 mol·L-1
B.将 2.3 g Na 投入到 97.7 g 水中充分反应,所得溶液中溶质的质量分数为 4.0%
C.在t℃时,将a g NH3完全溶于水,得到VmL溶液。该溶液的物质的量浓度为1000a/17V mol·L-1
D.1 mol·L-1的硫酸溶液中c(H+)=1 mol·L-1
难度: 中等查看答案及解析
-
下列有关物质检验的实验结论正确的是
选项
实 验 操 作 及 现 象
实 验 结 论
A
向某溶液中加入盐酸酸化的氯化钡溶液,有白色
沉淀生成
该溶液中一定含有 SO42-
B
向某溶液中加入 2 滴 KSCN 溶液,溶液不显红色
再向溶液中加入几滴新制的氯水,溶液变为红色
,该溶液中一定含有 Fe2+
C
将某气体通入品红溶液中,品红溶液褪色
该气体一定是 SO2
D
将某物质的溶液滴加酚酞试液中,溶液呈红色
该物质一定是碱
难度: 困难查看答案及解析
-
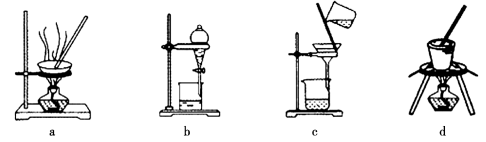
实验是化学研究的基础,下列各图所示的实验方法、装置或操作正确的是
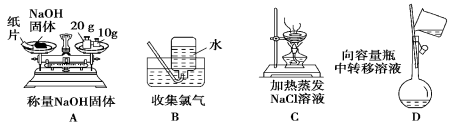
难度: 中等查看答案及解析
-
向 FeI2 溶液中滴加适量氯水,将反应后溶液分 3 份,甲试管中滴加淀粉溶液, 乙试管滴加 KSCN 溶 液,丙试管中滴加酸性高锰酸钾溶液,下列说法正确的是
A.若甲试管溶液呈蓝色,则乙试管溶液一定呈血红色
B.若甲试管溶液呈蓝色,则乙试管溶液可能无明显现象
C.乙试管溶液呈血红色,则甲试管溶液不可能呈蓝色
D.甲试管溶液呈蓝色,丙试管中紫红色褪去,说明滴加氯水后的溶液中一定存在 Fe3+和 Fe2+
难度: 困难查看答案及解析
-
下列混合物的除杂方法与发生反应的类型均正确的是
混合物
加入试剂或方法
反应类型
A
除去O2中的CO
通入炽热的CuO中
化合反应
B
除去CO2中的HCl
通入饱和NaHCO3溶液中
中和反应
C
除去CaCO3中的Na2CO3
溶解、加入BaCl2溶液
复分解反应
D
除去NaCl中的Na2CO3
加入适量盐酸、蒸发
复分解反应
难度: 中等查看答案及解析
-
Na、Mg、Al 三种金属各 2 mol 分别跟 1L 1mol∙L-1的盐酸反应时,相同条件下放出氢气体积最大的是
A.Al B.Mg
C.Na D.三者产生的氢气一样多
难度: 困难查看答案及解析
-
含氯化镁和氯化铝的混合溶液200mL,其中c(Mg2+)为0.2mol·L-1,c(Cl-)为1.3mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol·L-1NaOH溶液的体积为
A.40 mL B.72 mL C.80 mL D.128 mL
难度: 中等查看答案及解析
-
在含有 FeCl3、FeCl2、AlCl3、NaCl 的溶液中,加入足量的 NaOH 溶液,在空气中充分搅拌,反应后再加入过量的稀盐酸,溶液中离子数目减少的是
A.Na+ B.Fe3+ C.Al3+ D.Fe2+
难度: 中等查看答案及解析
-
下列对有关实验事实的解释正确的是
A.向某溶液中滴加氯水后,再加入 KSCN 溶液,溶液呈红色,说明原溶液中含有 Fe2+
B.浓硫酸和浓盐酸长期暴露在空气中浓度均降低,原理不相同
C.向某溶液中加入氯化钡溶液,生成白色沉淀,再加入稀盐酸,沉淀不溶解,则原溶液一定含有 SO42-
D.常温下,浓硫酸可以用铁制容器储运,说明铁与冷的浓硫酸不反应
难度: 中等查看答案及解析