-
化学与人类生产、生活密切相关,下列说法正确的是
A. 高纯度的硅单质广泛用于制作光导纤维
B. Na2SiO3水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料
C. 金属可分为“黑色金属”和“有色金属”,铁及其合金都属于“有色金属”
D. 食品包装里常有硅胶、石灰、还原铁粉三类小包,其作用相同
难度: 简单查看答案及解析
-
下列有关物质分类或归类正确的一组是
①液氨、液氯、干冰、碘化银均为化合物
②漂粉精、合金、氨水均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质
④碘酒、牛奶、豆浆均为胶体
⑤Na2O2、Na2CO3、NaHCO3、Na2SiO3均为钠盐
A. ①和② B. ②和③ C. ③和④ D. ②③⑤
难度: 中等查看答案及解析
-
下列关于氯水的叙述不正确的是
A. 新制氯水长期放置后颜色会逐渐褪为无色
B. 长期放置的氯水也能使有色布条褪色
C. 长期放置的氯水中含有的H+多于新制氯水
D. 新制氯水中含有的阳离子只有 H+
难度: 中等查看答案及解析
-
下列叙述正确的是
①标准状况下,0.2mol任何物质的体积均为4.48L
②若1mol气体的体积为22.4L,则它一定处于标准状况下
③标准状况下,1LHCl和1LH2O的物质的量相同
④标准状况下,1gH2和14gN2的体积相同
⑤28gCO的体积为22.4L
⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑦在同温同体积时,气体物质的物质的量越大,则压强越大
⑧同温同压下,气体的密度与气体的相对分子质量成正比
A. ①②③④ B. ②③⑥⑦⑧
C. ⑤⑥⑦⑧ D. ④⑦⑧
难度: 困难查看答案及解析
-
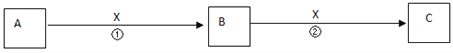
用下图表示的一些物质或概念间的从属关系中不正确的是
X
Y
Z
A
氧化物
化合物
纯净物
B
胶体
分散系
混合物
C
电解质
酸、碱、盐
化合物
D
碱性氧化物
金属氧化物
氧化物
难度: 中等查看答案及解析
-
利用实验器材(规格和数量不限),能完成相应实验的一项是
实验器材(省略夹持装置)
相应实验
A
烧杯、玻璃棒、蒸发皿
硫酸铜溶液的浓缩结晶
B
烧杯、玻璃棒、胶头滴管、滤纸
用盐酸除去硫酸钡中的少量碳酸钡
C
烧杯、玻璃棒、胶头滴管、容量瓶
用固体氯化钠配制0.5mol/L的溶液
D
烧杯、分液漏斗
用溴水和CCl4除去NaBr溶液中的少量NaI
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
实验室欲配制一种仅含四种离子的溶液(不考虑水电离),且溶液中四种离子的物质的量浓度均为1mol•L-1,能达到此目的的是
A. Al3+、K+、SO42-、NO3- B. ClO-、K+、I-、H+
C. Ba2+、OH-、CO32-、K+ D. Mg2+、Na+、Cl-、SO42-
难度: 中等查看答案及解析
-
下列实验不能达到目的的是
A. 用过量NaOH溶液除去镁粉中的铝粉 B. AlCl3溶液和氨水制备Al(OH)3沉淀
C. 用盐酸和AgNO3溶液鉴定Cl- D. 用加热的方法鉴别Na2CO3和NaHCO3
难度: 中等查看答案及解析
-
下列关于焰色反应的说法不正确的是
A. 金属单质无焰色反应
B. 只有某些金属或其化合物才有焰色反应
C. 透过蓝色钴玻璃观察钾元素焰色反应的颜色为紫色
D. 每次焰色反应实验后都要将铂丝用稀盐酸洗净并灼烧
难度: 简单查看答案及解析
-
有关NaHCO3和Na2CO3的性质,以下叙述正确的是
A. 等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下Na2CO3产生的CO2体积大
B. 等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3的两倍
C. 将石灰水加入NaHCO3溶液中不产生沉淀,加入Na2CO3 溶液中产生白色沉淀
D. 同物质的量浓度的两种溶液,Na2CO3溶液的碱性弱于NaHCO3溶液
难度: 中等查看答案及解析
-
有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可以将它们鉴别出来,这种试剂是
A. NaOH B. H2SO4 C. BaCl2 D. KSCN
难度: 中等查看答案及解析
-
二氧化硅又称硅石,是制备硅及其化合物的重要原料.下列说法正确的是
A. SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物
B. 在高温条件下SiO2能与过量的碳反应生成SiC,体现了二氧化硅的氧化性
C. 高温下SiO2能与Na2CO3反应放出CO2,不能说明H2SiO3的酸性强于H2CO3
D. 二氧化硅溶于水显酸性
难度: 中等查看答案及解析
-
若mgNa在足量氯气中燃烧,生成固体的质量为(m+3.55)g,则mgNa与氧气反应,生成固体的质量可能为
①(m+0.8)g ②(m+1.0)g ③(m+1.2)g④(m+1.6)g ⑤(m+1.4)g
A. ①④ B. ①⑤ C. ③④ D. ①②③④⑤
难度: 中等查看答案及解析
-
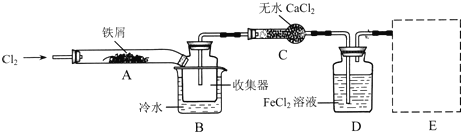
某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体的装置(夹持装置略,气密性已检验)如图所示。下列推断不合理的是
A. B中收集到的气体是氢气
B. 烧杯中双氧水溶液的作用是将Fe2+ 氧化为Fe3+
C. A中存在氧化铁与盐酸反应生成氯化铁的反应
D. 向反应后的烧杯中通入少量SO2,溶液颜色将立即由棕黄色变为浅绿色
难度: 中等查看答案及解析
-
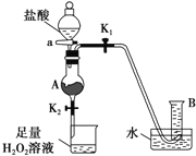
如图装置,试管中盛有水,气球a中盛有干燥的Na2O2颗粒,U形管中注有浅红色的水,将气球用橡皮筋紧缚在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是

A. U形管内红色褪去
B. 试管内溶液变红
C. 气球a变瘪
D. U形管水位d>c
难度: 中等查看答案及解析
-
向含有amolFeBr2的溶液中通入Cl2xmol ,下列各项为通Cl2的过程中溶液内发生反应的离子方程式,其中不正确的是(已知2Fe2++ Br2 = 2Fe3++ 2Br-)
A. x = 0.1a,2Fe2++Cl2 = 2Fe3++2Cl-
B. x = 0.6a,10Fe2++2Br-+6Cl2 =10Fe3++ Br2+12Cl-
C. x = a,2Br-+Cl2 = Br2+2Cl-
D. x = 1.5a,2Fe2++4Br-+3Cl2 = 2Br2+2Fe3++6Cl-
难度: 中等查看答案及解析
-
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
A. 取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
B. 取a克混合物与足量稀硫酸充分反应,逸出气体未经干燥用碱石灰吸收,增重b克
C. 取a克混合物充分加热至恒重,减重b克
D. 取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
难度: 中等查看答案及解析
-
标准状况下有22.4L氯气和氢气的混合气体,在一密闭容器中使其反应,冷却后将此气体通入足量的氢氧化钠溶液中,共消耗1.5molNaOH,则原混合气体中氯气和氢气的体积比为
A. 2:1 B. 1:1 C. 1:2 D. 3:1
难度: 中等查看答案及解析
-
在200 mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是

A. X与Y的差值为0.01 mol
B. 原溶液中c(Cl-)=0.66mol·L-1
C. 原溶液的c(H+)=0.8 mol·L-1
D. 原溶液中n(Mg2+)∶n(Al3+)=10∶1
难度: 中等查看答案及解析