-
下列说法正确的是( )
A.根据是否产生丁达尔效应,将分散系分为溶液、浊液和胶体
B.电解质溶液的导电过程就是其电解过程
C.催化剂能改变化学反应速率,但不参加化学反应
D.NO2、纯碱、CaO分别属于酸性氧化物、盐、碱性氧化物难度: 中等查看答案及解析
-
已知一定条件下断裂1mol下列化学键需要吸收的能量分别为:H-H 436kJ;Cl-Cl 243kJ;H-Cl 431kJ.对于反应 H2(g)+Cl2(g)=2HCl (g),下列说法正确的是( )
A.该反应的反应热△H>0
B.氢气分子中的化学键比氯气分子中的化学键更稳定
C.相同条件下,该反应在光照和点燃条件下的△H不同
D.H2与Cl2反应的热化学方程式为 H2(g)+Cl2(g)=2HCl(g)△H=-180.3kJ难度: 中等查看答案及解析
-
下列有关有机物的说法正确的是( )
A.石油的分馏和煤的干馏都是物理变化
B.甲烷、苯、乙酸乙酯都可以发生取代反应
C.油脂、蛋白质和纤维素都是高分子化合物
D.在加热、甲醛、饱和(NH4)2SO4溶液、X射线作用下,蛋白质都会发生变性难度: 中等查看答案及解析
-
下列有关实验操作正确的是( )
A.为了将苯和乙醇分开可用蒸馏的方法
B.用98%的浓硫酸配制100g10%的稀硫酸溶液时,除使用量筒外还需用到容量瓶
C.用瓷坩埚高温熔融NaOH和Na2CO3的固体混合物
D.浓硫酸和浓硝酸混合时,应将浓硝酸沿器壁慢慢加入到浓硫酸中,并不断搅拌难度: 中等查看答案及解析
-
含有一个苯环且分子式为C7H7Cl的同分异构体共有(不考虑立体异构)( )
A.2种
B.3种
C.4种
D.6种难度: 中等查看答案及解析
-
下列各项表达或表述中正确的是( )
A.IA族元素的金属性一定比ⅡA族元素的金属性强
B.常温常压下为气态的纯净物,分子内一定含有共价键
C.14C失去两个电子后得到12C
D.氕、氘、氚是氢元素的三种核素,具有相同的核外电子排布难度: 中等查看答案及解析
-
下列有关反应的离子方程式或电极反应式书写正确的是( )
A.钢铁的电化学腐蚀中正极反应式:Fe-2e-=Fe2+
B.金属钠与水反应:Na+2H2O=H2↑+2OH-+Na+
C.将铁加入过量的稀硝酸中 Fe+4H++NO3-=Fe3++2H2O+NO↑
D.用铜做阳极电解氯化铜溶液Cu2++2Cl-Cu+Cl2↑
难度: 中等查看答案及解析
-
关于下列各装置图的叙述中,正确的是( )
A.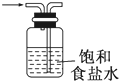
洗气装置,可以除去氯气中的氯化氢
B.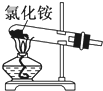
实验室可以用装置制取氨气
C.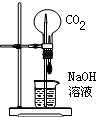
实验室用装置做“喷泉”实验不能成功
D.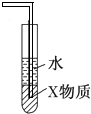
装置中X若为四氯化碳,可用于吸收氨气,并防止倒吸难度: 中等查看答案及解析
-
已知氧元素有16O、18O两种核素,按中学化学知识要求,下列说法正确的是( )
A.Na2O2与H218O反应时生成产生18O2气体
B.向2SO2(g)+O2(g)⇌2SO3(g)的平衡体系中加入18O2,结果18O2只出现在产物中
C.CH3COOH和CH3CH218OH发生酯化反应时,产物中分子式为H218O
D.用惰性电极电解含有H218O的普通水时,阳极可能产生三种相对分子质量不同的氧分子难度: 中等查看答案及解析
-
元素的原子结构决定其性质和周期表中的位置,下列有关结构和性质的说法中,正确的是( )
A.形成离子键的阴阳离子间只存在静电吸引力
B.元素周期表中,第三周期最右端的元素得电子能力最强
C.最易失去的电子能量最高
D.目前使用的元素周期表中最长的周期含有36种元素难度: 中等查看答案及解析
-
将一浅绿色溶液,置于空气中,变黄色.将此黄色溶液逐滴滴入沸水中,形成一种红褐色胶体,下列说法中错误的是( )
A.该浅绿色溶液中含有Fe2+在空气中被氧化为Fe3+
B.欲检验该黄色溶液中,是否含有未被氧化的Fe2+,向其中滴加KSCN溶液
C.配制该浅绿色溶液,要向其中加少量酸与铁粉,目的是为了防止Fe2+的水解与氧化
D.欲检验浅绿色溶液中是否含有Fe3+,滴入KSCN溶液,看是否变红色难度: 中等查看答案及解析
-
硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料、印泥等.某温度时,HgS在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
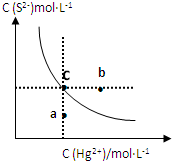
A.向硫化汞的浊液中加入硫化钠溶液,硫化汞的Ksp减小
B.图中a点对应的是饱和溶液
C.向c点的溶液中加入0.1 mol•L-1Hg(NO3)2,则c(S2-)减小
D.升高温度可以实现c点到b点的转化难度: 中等查看答案及解析
-
室温下氨水中存在平衡关系:NH3+H2O═NH3•H2O═NH4++OH-,下列有关判断正确的是( )
A.溶液中,c>c(OH-)>c(NH4+)
B.向溶液中通入氨气,增大
C.向溶液中加入少量盐酸,c(OH-)和c(NH4+)都减小
D.加水稀释平衡向右移动,c(NH4+)增大难度: 中等查看答案及解析
-
“天宫一号”与“神舟九号”载人交会对接任务的圆满成功,标志着我国载人航天工程取得重要进展.载人航天器的生态系统中,要求分离人呼出的CO2并同时提供O2.某电化学装置利用太阳能转化的电能可以实现上述要求,同时还有燃料CO生成,该装置中失电子的电极发生的反应是4OH--4e-=2H2O+O2↑.下列判断不正确的是( )
A.该装置进行的总反应为2CO2=2CO+O2
B.上述电化学装置相当于燃料电池
C.反应结束后该电化学装置中的电解质溶液pH不变
D.得电子的电极发生的反应是CO2+2e-+H2O=CO+2OH-难度: 中等查看答案及解析
-
在一定温度下,向2L体积固定的密闭容器中加入1molHI,2HI⇌H2(g)+I2(g)△H>0,H2的物质的量随时间的变化如图示,下列说法正确的是( )
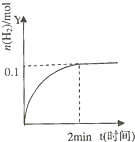
A.该温度下,反应的平衡常数是
B.0~2min内的HI的平均反应速率为0.05mol•L-1•min-1
C.恒压下向该体系中加入N2,平衡不移动,反应速率不变
D.升高温度,平衡向正反应方向移动,只有正反应速率加快难度: 中等查看答案及解析
-
化学与生产、生活息息相关,下列说法不正确的是( )
A.误食重金属盐可立即喝鲜牛奶或鸡蛋清解毒
B.高温结构陶瓷及压电陶瓷都属于新型无机非金属材料
C.服用Al(OH)3胶囊可用来治疗胃酸过多,无任何副作用
D.高铁酸钾(K2FeO4)是新型高效多功能水处理剂,既能消毒杀菌又能净水难度: 中等查看答案及解析



 (R、R′可以是烃基或H原子)
(R、R′可以是烃基或H原子)