-
变质的油脂有难闻的哈喇味,这是因为发生了
A.氧化反应 B.加成反应 C.取代反应 D.水解反应
难度: 简单查看答案及解析
-
要制取相同质量的Cu(NO3)2,下列反应中消耗HNO3最少的反应是
A.Cu和浓HNO3 B.Cu和稀HNO3
C.CuO和HNO3 D.Cu2O 和HNO3
难度: 中等查看答案及解析
-
能使淀粉碘化钾试纸变蓝的物质是
A.氯水 B.碘水 C.碘化钠溶液 D.溴化钠溶液
难度: 简单查看答案及解析
-
下列热化学方程式中的反应热为可燃物的燃烧热的是
A.H2(g)+1/2O2(g)=H2O(g) △ H =-241.8kJ·mol—1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △ H =-846.3kJ·mol—1
C.C(s)+O2(g)=CO2(g) △ H =-393. 5kJ·mol—1
D.C3H8(g)+5O2(g)=3CO(g)+4H2O(l) △ H = -2044.0kJ·mol—1
难度: 中等查看答案及解析
-
下列有机物的命名,正确的是

A.2,3,3,8,8——五甲基壬烷 B.2,2,7,7,8——五甲基壬烷
C.2,3,3,5,5——五甲基戊烷 D.2,2,4,4,5——五甲基戊烷
难度: 中等查看答案及解析
-
牙齿洁白,人人喜欢。将漂白剂沾在牙套上,牙齿咬住牙套可使牙齿变得洁白。下列物质溶于水后所得溶液可作为牙齿漂白剂的是
A.Cl2 B.HNO3 C.Na2O2 D.H2O2
难度: 简单查看答案及解析
-
在一密闭容器中充入1 mol CO和1 mol H2O(g),一定条件下反应:
达到平衡时生成0.67mol CO2,若在相同条件下将H2O(g)改为4mol,反应达到平衡时生成CO2的物质的量为
A、1.34mol B、1.0mol C、0.94mol D、0.52mol
难度: 中等查看答案及解析
-
根据反应(1)→(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是
⑴Cl2+2KI=2KCl+I2; ⑵2FeCl2+Cl2=2FeCl3;
⑶2FeCl3+2HI=2FeCl2+2HCl+I2,⑷H2S+I2=S+2HI;
A.S>I2>Fe3+>Cl2 B.Cl2>Fe3+>I2>S
C.Fe3+>Cl2>S>I2 D.Cl2>I2>Fe3+>S
难度: 中等查看答案及解析
-
对下列化学用语的理解正确的是
A.离子结构示意图
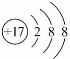 既可以表示35Cl-,也可以表示37Cl-
既可以表示35Cl-,也可以表示37Cl-B.电子式
既可以表示羟基,也可以表示氢氧根离子
C.比例模型
 既可以表示甲烷分子,也可以表示四氯化碳分子
既可以表示甲烷分子,也可以表示四氯化碳分子D.结构简式(CH3)2CHCH3既可以表示正丁烷,也可以表示异丁烷
难度: 简单查看答案及解析
-
在K2CO3样品中含Na2CO3、KNO3、Ba(NO3)2中的一或二种杂质.将13.8 g该样品溶于足量水中得到澄清溶液,再加入过量CaCl2溶液,可得9.0 g沉淀,则原样品中含有的杂质会是
A.肯定有Na2CO3,没有Ba(NO3)2
B.肯定有KNO3,没有Ba(NO3)2,可能还有Na2CO3
C.肯定没有Na2CO3,Ba(NO3)2
D.无法判断何种为肯定或否定的杂质
难度: 困难查看答案及解析
-
一个容积固定密闭容器中进行反应N2 + 3H2
2NH3,一定达到平衡状态的是
①1个N≡N键断裂的同时,有3个H — H键形成;②1个N≡N键断裂的同时,有6个N — H键形成;③N2的体积分数不再改变;④容器的压强不再改变;⑤容器内气体的密度不再改变;
A.①③④ B.①②④ C.①③⑤ D.②③④
难度: 中等查看答案及解析
-
下列说法正确的是
A.用乙醇或CCl4可提取碘水中的碘单质
B.NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同
C.24Mg32S晶体中电子总数与中子总数之比为1∶1
D.H2S和SiF4分子中各原子最外层都满足8电子结构
难度: 中等查看答案及解析
-
下列说法正确的是
A.3,3-二甲基-1-丁烯在一定条件下与氢气充分反应后得到3,3-二甲基丁烷。
B.工业生产中用乙醇与氢氧化钠作用生成乙醇钠,故乙醇可以与氢氧化钠溶液反应。
C.地球上最基本的能源是太阳能,植物通过光合作用吸收太阳能,被吸收的太阳能通过各种形式的化学反应转化为化学能,物质中的化学能又可以通过各种形式的化学反应转化为热能、光能或电能。
D.道尔顿、汤姆生、卢瑟福、波尔、阿伏伽德罗和门捷列夫等科学家对原子结构模型的建立均作出了卓越的贡献
难度: 中等查看答案及解析
-
已知反应A(g)+B(g)
nC(g) △H=x kJ·mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如图。

下列有关叙述一定正确的是
A.a条件下的反应速率小于b条件下的反应速率
B.其他条件相同时,a表示有催化剂,b表示无催化剂
C.其他条件相同,若a、b表示不同压强下的反应,则n>2
D.其他条件相同,若a、b表示不同温度下的反应,则x>0
难度: 中等查看答案及解析
-
温度为T时,向2.0L恒容密闭容器中充入1.0 molPCl5,反应PCl5(g)
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s
0
50
150
250
350
n(PCl3)/ mol
0
0.16
0.19
0.20
0.20
下列说法正确的是
A.反应在前50 s的平均速率为v(PCl3)=0.0032 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,达到平衡时,PCl3的转化率大于80%
难度: 困难查看答案及解析
-
下列溶液与100 mL 0.5 mol/L NaCl溶液中所含的Cl-物质的量浓度相同的是
A.100 mL 0.5 mol/L MgCl2溶液
B.200 mL 0.25 mol/L AlCl3溶液
C.50 mL 1 mol/L NaCl溶液
D.25 mL 0.5 mol/L HCl溶液
难度: 简单查看答案及解析




