-
化学科学对提高人类生活质量和促进社会发展具有重要作用,下列说法不正确的是
A.将地沟油回收加工为燃料油,提高资源的利用率
B.燃煤进行脱硫脱硝处理,减少硫的氧化物和氮的氧化物的排放
C.推广城市生活垃圾处理减量化、资源化、无害化技术,有利于环保和资源充分利用
D.大量生产超薄塑料袋,方便人们的日常生活
难度: 简单查看答案及解析
-
下列有关化学用语使用正确的是
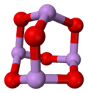
A.CO2的电子式:
B.中子数为20的氯原子:
C.乙烯的比例模型:
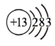
D.铝离子结构示意图:
难度: 简单查看答案及解析
-
下列溶液中,离子一定能大量共存的是
A.pH=l的溶液中:Na+、Mg2+、SO42-、HCO3-
B.滴入KSCN溶液显红色的溶液中:Al3+、Cu2+、Cl-、SO42-
C.c(I-)=0.1mol/L的溶液,Na+、Fe3+、ClO-、SO
D.水电离产生的c(H+) =10-12mol/L-1的溶液中:K+、Ba2+、NO3-、OH-
难度: 简单查看答案及解析
-
下列有关物质性质的叙述正确的是
A.浓硫酸能干燥氢气、氯气、一氧化碳等气体,说明浓硫酸具有吸水性
B.SiO2既能溶于NaOH溶液又能溶于HF,说明SiO2是两性氧化物
C.乙炔能使溴水、酸性高锰酸钾溶液褪色,说明乙炔具有漂白性
D.纤维素的水解产物能够发生银镜反应,说明纤维素是一种还原性糖
难度: 简单查看答案及解析
-
据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是
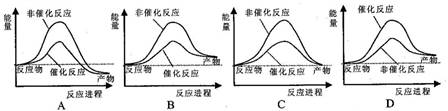
难度: 简单查看答案及解析
-
关于下列各实验装置图的叙述中,正确的是
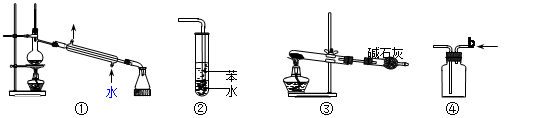
A.装置①可用于分离苯和溴苯的混合物
B.装置②可用于吸收HCl或NH3气体
C.装置③可用于分解NH4Cl制备NH3
D.装置④b口进气可收集CO2或NO气体
难度: 简单查看答案及解析
-
三种不同物质有如图所示转化关系:甲
乙
丙
甲,则甲不可能是
A.Al2O3 B.SiO2 C.CO2 D.NH4Cl
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,11.2 L乙醇所含的羟基数为0.5NA
B.常温下,1L 0.1 mol·L-1的Na2CO3溶液中含有的离子总数为0.3NA
C.常温常压下,5.6g乙烯和环丙烷的混合气体中含有的碳原子数为0.4NA
D.电解硫酸铜溶液时,阳极每生成标准状况下3.36L气体,电路中转移电子数为0.3NA
难度: 简单查看答案及解析
-
下列离子方程式表达不正确的是
A.用SO2水溶液吸收Br2:SO2 + Br2+2H2O =4H+ + SO
+2Br-
B.用稀硫酸除去铜绿:4H++Cu2(OH)2CO3===2Cu2++CO2↑+3H2O
C.酸性高锰酸钾和过氧化氢制取少量氧气:4MnO
+4H2O2+12H+=4Mn2++7O2↑+10H2O
D.用惰性电极电解硫酸铜溶液:2Cu2++ 2H2O
2Cu↓ +O2↑ +4H+
难度: 简单查看答案及解析
-
下列说法正确的是
A.反应:2CO(g)+2NO(g) N2(g)+2CO2(g)在温度为298K时能自发进行,则它的△H>0, △S>0
B.0.1mol/L NH4C1溶液加蒸馏水稀释,溶液的pH不断减小
C.为保护浸入海水中的钢闸门,可在闸门表面镶上铜锭
D.反应:2A(g)
B(g)+2C(g),增大压强反应速率加快,A的转化率减小
难度: 简单查看答案及解析
-
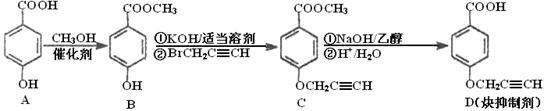
CPAE是蜂胶的主要活性成分,也可由咖啡酸合成,下列说法不正确的是
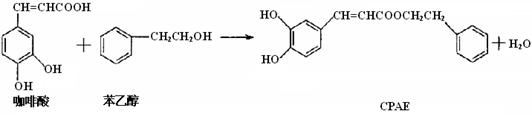
A.咖啡酸分子中所有原子可能处在同一个平面上
B.可用金属Na检测上述反应是否残留苯乙醇
C.1 mol 苯乙醇在O2中完全燃烧,需消耗10 mol O2
D.1 mol CPAE与足量的NaOH溶液反应,最多消耗3 mol NaOH
难度: 简单查看答案及解析
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,B、C同周期,D、E
也同周期, D原子最外层电子数与最内层电子数相等,A、B、C、D的原子序数之和是E
的两倍,D与C形成的化合物是一种耐高温材料,A、B形成的气态化合物的水溶液呈碱性。
下列说法正确的是
A.原子半径:D>E>B>C>A B.热稳定性:EA4>A2C
C.单质D可用海水作原料获得 D.化合物DC与化合物EC2中化学键类型相同
难度: 简单查看答案及解析
-
下列实验操作与预期目的或所得结论一致的是
选项
实验操作
实验目的或结论
A
某钠盐溶液中加入盐酸酸化的硝酸钡溶液有白色沉淀
说明该钠盐是硫酸钠或硫酸氢钠
B
向混有乙酸和乙醇的乙酸乙酯的混合物中,加入饱和Na2CO3溶液洗涤、分液
得到较纯净的乙酸乙酯
C
向裂化汽油中加入酸性高锰酸钾溶液,振荡,紫色褪去
说明汽油中含有甲苯等苯的同系物
D
向含有少量的FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取分液
除去FeCl2溶液中的FeBr2
难度: 简单查看答案及解析
-
在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
Ni(s)+4CO(g)
Ni(CO)4(g),已知该反应平衡常数与温度的关系如下表:
温度/℃
25
80
230
平衡常数
5×104
2
1.9×10-5
下列说法不正确的是
A.上述生成Ni(CO)4(g)的反应为吸热反应
B.25°C时反应Ni(CO)4(g)
Ni(s)+4CO(g)的平衡常数为2×10-5
C.80°C达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2mol/L
D.80°C时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)>v(逆)
难度: 简单查看答案及解析
-
下列有关溶液中粒子浓度的关系式中,正确的是
A.pH相同的①CH3COONa、②NaHCO3、③C6H5ONa三份溶液中的c(Na+):③>②>①
B.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C.下图中pH=7时: c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
D.下图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
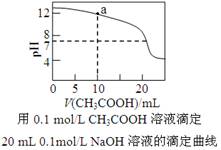
难度: 简单查看答案及解析
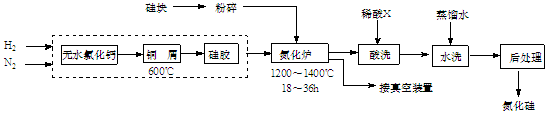
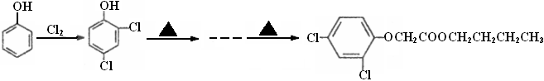
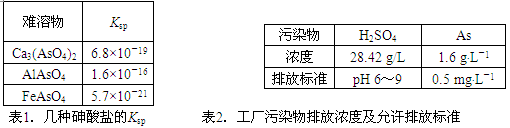 回答以下问题:
回答以下问题: