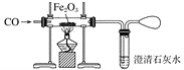
-
我国十分重视海水资源的综合利用,下列物质不需经化学变化就能从海水中获得的是
A. 氯、溴、碘 B. 钠、镁、铝 C. 烧碱、氢气 D. 食盐、淡水
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 碱性:LiOH>NaOH>KOH>RbOH
B. 金属性:Rb>K>Na>Li
C. 铷比钾活泼,铷能从氯化钾溶液中置换出钾
D. 铷不易与水反应放出氢气
难度: 简单查看答案及解析
-
海水中提取溴的过程发生反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与该反应原理最相似的是( )
A. 2NaBr+Cl2=2NaCl+Br2 B. 2KI+Br2=2KBr+I2
C. 2H2S+SO2=3S+2H2O D. Cl2+H2O=HCl+HClO
难度: 简单查看答案及解析
-
根据化学反应的实质是旧键断裂和新键形成这一事实,下列变化不属于化学变化的是( )
A. 钠投入水中 B. 石墨在高温高压下转化为金刚石
C. 干冰汽化 D. 五氧化二磷吸水
难度: 中等查看答案及解析
-
关于元素周期表,下列叙述中不正确的是( )
A. 元素周期表中共有18列, 16族
B. 周期表中的族分为主族、副族、0族和Ⅷ族
C. 过渡元素全部是副族元素
D. 主族都是由短周期元素和长周期元素共同组成
难度: 简单查看答案及解析
-
恒温恒容密闭容器中发生反应2A(g)+B(g)
2C(g),若反应物A的浓度由0.1 mol·L-1降到0.06 mol·L-1需20 s,那么由0.06 mol·L-1降到0.036 mol·L-1所需的时间为( )
A. 等于10 s B. 等于12 s
C. 大于12 s D. 小于12 s
难度: 简单查看答案及解析
-
分子式为C16H28的链状烃,其分子中只含有C=C双键,而无其他不饱和键,则含有C=C双键的数目是( )
A. 1个 B. 2个 C. 3个 D. 4个
难度: 简单查看答案及解析
-
下列哪一组元素的原子间反应容易形成离子键( )
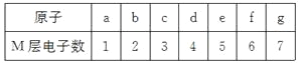
A. a和c B. a和f C. d和g D. c和g
难度: 简单查看答案及解析
-
在下图的装置中,属于原电池且有电流产生的是( )
A.
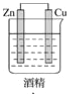 B.
B. 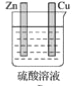 C.
C. 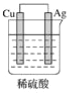 D.
D. 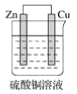
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A. 碱金属元素中,金属活动性最强的是锂
B. 碱金属单质都可保存在煤油中
C. 过氧化钠在某些呼吸面具中用于制备氧气
D. 钠长时间放置在空气中最终将转化为氧化钠
难度: 简单查看答案及解析
-
原子序数为x的元素E在周期表中位于A、B、C、D四种元素中间(如图所示),则A、B、C、D四种元素的原子序数之和不可能是(镧系、锕系、0族元素除外)( )

A. 4x B. 4x+6 C. 4x+10 D. 4x+14
难度: 中等查看答案及解析
-
下图为铜锌原电池示意图,下列说法正确的是( )
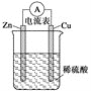
A. 锌片逐渐溶解
B. 烧杯中溶液逐渐呈蓝色
C. 电子由铜片通过导线流向锌片
D. 锌为正极,铜为负极
难度: 简单查看答案及解析
-
不能使碘化钾淀粉溶液显蓝色的物质是( )
A. I2 B. KI C. NO2 D. Cl2
难度: 简单查看答案及解析
-
在下列元素中,与氢气反应最剧烈的是( )
A. 氟 B. 氯 C. 溴 D. 碘
难度: 简单查看答案及解析
-
2SO2(g)+O2(g)
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
A. 催化剂V2O5不改变该反应的逆反应速率 B. 增大反应体系的压强,反应速率一定增大 C. 该反应是放热反应,降低温度将缩短反应达到平衡的时间 D. 在t1、l2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为
难度: 中等查看答案及解析
-
将溴水和苯混合振荡,静置后分液分离,把分离出来的苯层置于一试管中,加入某些物质后可以在试管口产生白雾,这种物质是( )
①亚硫酸钠 ②溴化铁 ③锌粉 ④铁粉
A. ①③ B. ②④ C. ①④ D. ②③
难度: 简单查看答案及解析
-
下列有关化学反应速率和限度的说法中,不正确的是( )
A. 实验室用过氧化氢分解制氧气,加入二氧化锰,反应速率明显加快
B. 在金属钠与足量水反应中,增加水的量能加快反应速率
C. 2SO2+O2
2SO3反应中,增加二氧化硫的量可加快反应速率
D. 实验室用碳酸钙和盐酸反应制取二氧化碳,用碳酸钙粉末比块状反应要快
难度: 简单查看答案及解析
-
城市大气中铅污染的主要来源是( )
A. 铅笔的随意丢弃 B. 使用含铅汽油的汽车尾气
C. 蓄电池的使用 D. 化妆品的大量使用
难度: 简单查看答案及解析
-
已知①2C+O2=2CO和②2CO+O2=2CO2都是放热反应,下列说法中不正确的是(其它条件相同)( )
A. 12 g碳所具有的能量一定高于28 g一氧化碳所具有的能量
B. 28 g一氧化碳和16 g氧气所具有的总能量一定高于44 g二氧化碳所具有的总能量
C. 12 g碳和32 g氧气所具有的总能量一定高于44 g二氧化碳所具有的总能量
D. 将一定质量的碳燃烧,生成二氧化碳比生成一氧化碳时放出的热量多
难度: 简单查看答案及解析
-
下列说法中正确的是( )
A. 乙醇分子中的氢原子均可被钠置换
B. 乙醇能与钠反应放出氢气,说明乙醇能电离产生H+而表现酸性
C. 乙醇分子中的羟基(—OH)氢比乙烷分子中的氢原子活泼
D. 乙醇分子中的羟基氢与其分子中其他的氢一样活泼
难度: 简单查看答案及解析
-
下列有关说法不正确的是( )
A. 乙烯的化学性质比乙烷活泼是因为乙烯分子中含有碳碳双键
B. 乙烯分子的碳碳双键中有一个键容易断裂,能与溴水发生加成反应
C. 1 mol乙烯与氯气完全加成后,产物再与氯气彻底取代,两个过程中共消耗氯气6 mol
D. 乙烯在空气中的燃烧现象与甲烷燃烧现象不同的原因是乙烯中含碳量高
难度: 简单查看答案及解析
-
某主族元素的原子最外层只有一个电子,下列说法正确的是( )
A. 该元素与卤素化合时一定形成离子键
B. 该元素与卤素化合时一定不能形成离子键
C. 该元素与氯元素形成的化合物一定是离子化合物
D. 该元素与氯元素形成的化合物的水溶液能导电
难度: 简单查看答案及解析
-
下列各组物质中,互称为同分异构体的是( )。
A. 冰和水 B. 白磷和红磷
C. 纯碱和烧碱 D. 新戊烷和异戊烷
难度: 简单查看答案及解析
-
下列说法能够说明氮的非金属性比磷强的是( )
A. 硝酸比磷酸更稳定
B. 硝酸的氧化性比磷酸强
C. 硝酸的酸性比磷酸强
D. 硝酸比磷酸容易挥发
难度: 简单查看答案及解析
-
下列关于试剂保存正确的是( )
A. 氢氧化钠固体保存在带有橡胶胶塞的细口瓶中
B. 碳酸钠溶液保存在带有橡胶塞的广口瓶中
C. 金属钾保存在煤油中
D. 过氧化钠密封在带玻璃塞的广口瓶中
难度: 简单查看答案及解析