-
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是( )
A.加热
B.不用稀硫酸,改用98%的浓硫酸
C.滴加少量CuSO4溶液
D.不用铁片,改用铁粉难度: 中等查看答案及解析
-
把a、b、c、d四块金属片浸入稀酸中,用导线两两相连组成原电池.若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时,c极上产生大量气泡;b、d相连时,b极上有大量气泡产生.则四种金属的活动性顺序由强到弱为( )
A.a>b>c>d
B.c>a>b>d
C.a>c>d>b
D.b>d>c>a难度: 中等查看答案及解析
-
A、B为同主族的两元素,A在B的上一周期,若A的原子序数为n,则B的原子序数不可能为( )
A.n+8
B.n+18
C.n+32
D.n+20难度: 中等查看答案及解析
-
已知汽车尾气无害化处理反应为2NO(g)+2CO(g)⇌N2(g)+2CO2(g),下列说法不正确的是( )
A.升高温度可使该反应的逆反应速率降低
B.使用高效催化剂可有效提高正反应速率
C.反应达到平衡后,NO的反应速率保持恒定
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡难度: 中等查看答案及解析
-
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4═Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是( )
实验 反应温度/℃ Na2S2O3溶液 稀H2SO4 H2O V/mL c/ V/mL c/ V/mL A 25 5 0.1 10 0.1 5 B 25 5 0.2 5 0.2 10 C 35 5 0.1 10 0.1 5 D 35 5 0.2 5 0.2 10
A.A
B.B
C.C
D.D难度: 中等查看答案及解析
-
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构.下列关于X、Y、Z、W四种元素的描述,不正确的是( )
A.原子半径:X>Y>Z>W
B.原子序数:Y>X>Z>W
C.原子最外层电子数:Z>W>Y>X
D.金属性:X>Y难度: 中等查看答案及解析
-
Se是人体必需的微量元素,下列关于
Se和
Se的说法正确的是( )
A.Se和
Se互为同素异形体
B.Se和
Se互为同位素
C.Se和
Se分别含有44和46个质子
D.Se和
Se都含有34个中子
难度: 中等查看答案及解析
-
一种比黄金贵百倍的818O2气体,不久前在兰州近代物理研究所制备成功.1mol 818O2气体中所含中子的物质的量为( )
A.16mol
B.18mol
C.20mol
D.24mol难度: 中等查看答案及解析
-
下列叙述能说明X的非金属性比Y强的是( )
A.X原子的电子层数比Y原子的电子层数多
B.达到稳定结构时,X比Y得电子数多
C.X的氢化物比Y的氢化物稳定
D.Y单质可以将X从NaX的溶液中置换出来难度: 中等查看答案及解析
-
现有xMm-和yNn+两种简单离子,它们的电子层结构相同.则表示M元素质子数的正确表达式是( )
A.x=y-n-m
B.x=y+n+m
C.x=y+n-m
D.x=y-n+m难度: 中等查看答案及解析
-
下列排列顺序错误的是( )
A.酸性:H4SiO4<H3PO4<H2SO4<HClO4
B.沸点:HF>HI>HBr>HCl
C.氢化物的稳定性:SiH4>H2S>H2O>HF
D.原子半径:F<O<S<Na难度: 中等查看答案及解析
-
下列说法正确的是( )
A.化学键断裂放出能量
B.离子化合物中可能含有共价键
C.单质中可能含离子键
D.由分子组成的物质中一定存在共价键难度: 中等查看答案及解析
-
某元素的原子最外层只有一个电子,它跟氯元素结合时( )
A.一定形成共价键
B.一定形成离子键
C.可能形成共价键,也可能形成离子键
D.以上说法都不对难度: 中等查看答案及解析
-
决定化学反应速率的主要因素是( )
A.反应物的性质
B.反应物的浓度
C.反应温度
D.使用催化剂难度: 中等查看答案及解析
-
理论上不能设计为原电池的化学反应是( )
A.CH4+2O2CO2+2H2O
B.AgNO3+NaCl=NaNO3+AgCl
C.2H2+O22H2O
D.2FeCl3+Fe═3FeCl2难度: 中等查看答案及解析
-
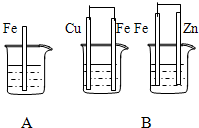
下列装置中有电流产生的是( )
A.
B.
C.
D.难度: 中等查看答案及解析
-
物质的下列性质能肯定该物质为离子化合物的是( )
A.水溶液能导电的化合物
B.由金属元素和非金属元素组成的化合物
C.在熔化状态下能导电的化合物
D.熔点高的物质难度: 中等查看答案及解析
-
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物对应水化物呈碱性,且碱性b>a;c和d的气态氢化物的还原性d>c;五种元素的原子得失电子后所形成的简单离子中e的离子半径最小,则它们的原子序数由小到大的顺序是( )
A.b、a、d、c、e
B.e、b、a、d、c
C.b、a、e、d、c
D.c、d、e、a、b难度: 中等查看答案及解析
-
已知SO2和O2反应生成4mol SO3时放出的热量为Q kJ,那么相同条件下2mol SO2和1mol O2在一有催化剂的密闭容器中发生反应时,放出的热量为( )
A.大于0.5QkJ
B.等于0.5QkJ
C.小于0.5QkJ
D.无法确定难度: 中等查看答案及解析
-
下列关于原电池的叙述中正确的是( )
A.正极和负极必须是两种不同的金属
B.原电池是把化学能转化成电能的装置
C.原电池工作时,正极和负极上发生的都是氧化还原反应
D.锌、铜和盐酸构成的原电池,锌片上有6.5g锌溶解,正极上就有0.1g氢气难度: 中等查看答案及解析
 且X、Y 均为不大于20的正整数,据此回答下列问题:
且X、Y 均为不大于20的正整数,据此回答下列问题: