-
分析下面的能量变化图,判断下列选项中正确的是
A. 2A(g)+B(g) === 2C(g) △H<0 B. 2A(g)+B(g) === 2C(g) △H>0
C. 2A+B=== 2C △H<0 D. 2C=== 2A+B △H<0
难度: 中等查看答案及解析
-
下列热化学方程式中△H的绝对值表示可燃物燃烧热的是
A. CO(g)+
O2(g) ===CO2(g) △H=-283.0 kJ•mol-1
B. CH4(g)+ 2O2(g) ===CO2(g)+2H2O(g) △H=-802.3 kJ•mol-1
C. 2H2(g)+ O2(g) ===2H2O(l) △H=-571.6kJ•mol-1
D. C(s)+
O2(g) ===CO(g) △H=-110.5kJ•mol-1
难度: 中等查看答案及解析
-
100gC不完全燃烧所得产物中,CO所占体积为
,CO2为
,且:
C(s)+
O2(g) ===CO(g) ΔH=-110.35 kJ•mol-1
CO(g)+
O2(g) ===CO2(g) ΔH=-282.57 kJ•mol-1
与这些碳完全燃烧相比,损失的热量为
A.39.292kJ B.3274.3kJ C.784.92kJ D.2489.44kJ
难度: 中等查看答案及解析
-
设C+CO2
2CO-Q1,反应速率V1;N2+ 3 H2
2NH3+Q2反应速率V2 。对于上述反应,当温度升高时,V1和V2的变化情况为
A. 同时增大 B. 同时减小
C. V1增大,V2减小 D. V1减小,V2增大
难度: 中等查看答案及解析
-
在2L密闭容器中,发生3A(气)+B(气) ==2C(气)的反应,若最初加入A和B都是4mol,A的平均反应速率为0.12mol/(L·s),则10秒钟后容器中B的物质的量为
A. 2.8mol B. 1.6mol C. 3.2mol D. 3.6mol
难度: 中等查看答案及解析
-
下图是关于反应A2(g)+3B2(g)
2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是
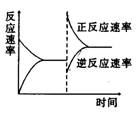
A.升高温度,同时加压
B.降低温度,同时减压
C.增大反应物浓度,同时减小生成物浓度
D.增大反应物浓度,同时使用催化剂
难度: 中等查看答案及解析
-
在一定温度下,容器内某一反应中M、N的物质的量随反应时间的变化曲线如图,下列表述中正确的是
?
A. 反应的化学方程式为:2M
N B. t2时,正逆反应速率相等,达到平衡
C. t3时,正反应速率大于逆反应速率 D. t1时,N的浓度是M浓度的2倍
难度: 中等查看答案及解析
-
把下列四种 X 溶液分别加入四个盛有 10mL2 mol•L-1盐酸的烧杯中,均匀加水稀释到50mL。此时X 和盐酸缓缓地进行反应。其中反应速率最大的是
A. 20mL 3 mol•L-1的 X 溶液 B. 20mL 2 mol•L-1的 X 溶液
C. 10mL 4 mol•L-1的 X 溶液 D. l0mL 2 mol•L-1的 X 溶液
难度: 中等查看答案及解析
-
在恒温恒容的密闭容器中,对于可逆反应A(g)+B(g)
2C(g),可以判断达到化学平衡状态的是
A. 体系压强不变 B. 单位时间消耗n molA,同时生成2nmolC
C. A的转化率不变 D. 容器内气体密度不变
难度: 中等查看答案及解析
-
在某温度下,H2和I2各0.10mol的气态混合物充入10L的密闭容器中,发生反应:H2(g)+I2(g)
2HI(g),充分反应后达到平衡,测得c(H2)=0.008 mol•L-1,则该反应的平衡常数为
A. 40 B. 62.5 C. 0.25 D. 4
难度: 中等查看答案及解析
-
能说明溶液呈中性的可靠依据是
A. pH=7 B. c(H+)=c(OH-)
C. pH试纸不变色 D. 石蕊试液不变色
难度: 中等查看答案及解析
-
下列说法正确的是
A. 强电解质溶液的导电能力一定比弱电解质溶液的强
B. 氨气是弱电解质,铜是强电解质
C. 氧化钠是强电解质,醋酸是弱电解质
D. 硫酸钠是强电解质,硫酸钡是弱电解质
难度: 中等查看答案及解析
-
25℃时,水的电离可达到平衡:H2O
H++OH- △H>0,下列叙述正确的是
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C. 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D. 将水加热,Kw增大,pH不变
难度: 中等查看答案及解析
-
实验室在配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释至所需浓度,如此操作的目的是
A. 防止硫酸铁分解 B. 抑制硫酸铁水解
C. 提高硫酸铁的溶解度 D. 提高溶液的pH
难度: 中等查看答案及解析
-
25℃时,将稀氨水逐滴加入到稀
硫酸中,当溶液的pH=7时,下列关系正确的是
A. c(NH4+) = c(SO42-) B. c(NH4+)=2c(SO42-)
C. 2c(NH4+)=c(SO42-) D. c(OH-)+c(SO42-) = c(H+)+c(NH4+)
难度: 中等查看答案及解析
-
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
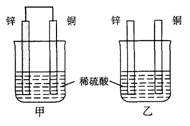
A. 两烧杯中铜片表面均无气泡产生 B. 甲中铜片是正极,乙中铜片是负极
C. 两烧杯中溶液的pH均增大 D. 产生气泡的速度甲比乙慢
难度: 中等查看答案及解析
