-
已知铋元素(Bi)的化合价可表现为+3或+5.锗酸铋(简称BGO)是一种性能优良的闪烁晶体材料,其中锗(Ge)元素为+4价.BGO可看成由锗和铋两种元素的氧化物所形成的化合物.已知在BGO中,两种氧化物所含氧的质量相同,则BGO的化学式可能是( )
A.Bi3Ge3O15
B.Bi3Ge3O12
C.Bi4Ge3O16
D.Bi4Ge3O12难度: 中等查看答案及解析
-
水的污染主要来自:①天然水与空气、岩石与土壤长期接触;②工业生产中废气、废液、废渣的任意排放;③水生动物的繁殖;④城市生活污水的大量排放;⑤农业生产中农药、化肥使用不当.( )
A.④、⑤
B.②、④、⑤
C.①、②、③
D.②、③、④、⑤难度: 中等查看答案及解析
-
下列说法正确的是( )
A.消化过程是一种不消耗能量的过程
B.近年常发生工业用盐当作食盐用而引起食物中毒的现象,该工业用盐对人有致癌作用,它的化学成分是NaNO2
C.新陈代谢过程是生物体自我更新的过程,因此,只存在物质变化,不涉及能量的转化
D.磁悬浮列车在运行时会“浮”在轨道上方,从而减少了地球对列车的引力,故可高速运行难度: 中等查看答案及解析
-
为防止水源污染,最近,政府部门决定对市售洗衣粉的销售和使用加以限制,严禁销售和使用的洗衣粉中主要是因为含有
( )
A.蛋白酶
B.碱性物质
C.磷的化合物
D.香料难度: 中等查看答案及解析
-
己知一个R原子的质量是一个氧原子质量的2倍,假设以一个氧原子质量的1/n作为国际相对原子质量标准,则R的氧化物RO2的相对分子质量为( )
A.3n
B.2n
C.n
D.4n难度: 中等查看答案及解析
-
在不同光照强度(单位LX)下,CO2浓度对菜豆叶片光合速率的影响如图所示,下列哪项说法不合理( )
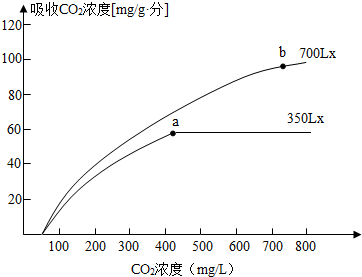
A.a点以前影响光合速率的主要因素是CO2浓度
B.a点以后影响光合速率的主要因素是光照速度
C.菜豆较适宜的光照强度为700LX
D.菜豆最适宜的CO2浓度为450mg/L难度: 中等查看答案及解析
-
将稀盐酸分别慢慢滴入装有Na2CO3溶液和NaHCO3溶液的两试管中,会发现:装有NaHCO3溶液的试管中很快产生气泡,而装有Na2CO3溶液的试管中开始没有气泡产生,但随着滴入稀盐酸的量增加,才会产生气泡.在Na2CO3溶液试管中发生这种现象的主要原因是( )
A.Na2CO3溶液开始与稀盐酸不反应
B.与CaCO3和过量CO2水溶液反应类似,Na2CO3溶液与稀盐酸反应先生成了NaHCO3
C.NaHCO3溶液碱性比Na2CO3溶液强,与盐酸反应快
D.Na2CO3溶液呈酸性难度: 中等查看答案及解析
-
人体正常的血红蛋白中应含有Fe2+,若误食亚硝酸盐,则导致血红蛋白中的Fe2+转化为Fe3+,产生高价铁血红蛋白而中毒.服用维生素C可解除亚硝酸盐中毒.在维生素C解毒的反应中( )
A.亚硝酸盐是还原剂
B.维生素C是氧化剂
C.亚硝酸盐被氧化
D.维生素C将Fe3+还原为Fe2+难度: 中等查看答案及解析