-
提出元素周期律并绘制了第一张元素周期表的化学家是( )
A. 戴维 B. 侯德榜 C. 道尔顿 D. 门捷列夫
难度: 简单查看答案及解析
-
在下列过程中,需要加快反应速率的是( )
A. 食物变质 B. 合成氨 C. 钢铁腐蚀 D. 塑料老化
难度: 简单查看答案及解析
-
下列不属于高分子化合物的是( )
A. 纤维素 B. 聚氯乙烯 C. 淀粉 D. 油脂
难度: 简单查看答案及解析
-
下列变化属于物理变化的是( )
A. 石油分馏 B. 煤的液化 C. 蛋白质变性 D. 石油裂化
难度: 简单查看答案及解析
-
金刚石与C60互称( )
A. 同一种物质 B. 同位素 C. 同素异形体 D. 同分异构体
难度: 简单查看答案及解析
-
干冰所属晶体类型为( )
A. 原子晶体 B. 分子晶体 C. 金属晶体 D. 离子晶体
难度: 简单查看答案及解析
-
下列各物质的分子中所有原子处于同一平面的是( )
A. 甲烷 B. 丙烷 C. 苯 D. 乙醇
难度: 简单查看答案及解析
-
下列反应中,生成物的总能量高于反应物的总能量的是( )
A. 煅烧石灰石 B. 锌与稀硫酸反应 C. NaOH溶液和稀盐酸反应 D. 铝热反应
难度: 简单查看答案及解析
-
下列各组有机物中,使用溴水不能鉴別出的是
A. 苯、四氯化碳 B. 乙炔、乙烯 C. 乙烷、乙烯 D. 苯、酒精
难度: 简单查看答案及解析
-
下列化学用语不正确的是( )
A. NH3分子的结构式:
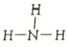 B. 乙烯的球棍模型:
B. 乙烯的球棍模型:
C. NaCl的电子式:
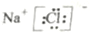 D. 中子数为7的碳原子
D. 中子数为7的碳原子难度: 简单查看答案及解析
-
下列元素中,属于第二周期且原子半径较大的是( )
A. N B. F C. Na D. Al
难度: 简单查看答案及解析
-
钠与水的反应属于( )
①氧化还原反应;②离子反应;③放热反应
A. ①②③ B. ①② C. ②③ D. ①③
难度: 简单查看答案及解析
-
下列关于能量转化的说法中正确的是( )
A. 给手机充电时:化学能转化为电能
B. 铅蓄电池的放电过程:电能转化为化学能
C. 氢气在氧气中燃烧:化学能转化为热能和光能
D. 植物的光合作用:生物质能(化学能)转化为光能(太阳能)
难度: 简单查看答案及解析
-
下列反应或事实不能说明碳元素的非金属性比硅元素的非金属性强的是( )
A. 热稳定性:CH4>SiH4 B. SiO2+2C
Si+2CO↑
C. 碳酸酸性比硅酸酸性强 D. 碳与硅属于同一主族元素,且碳原子序数小于硅
难度: 简单查看答案及解析
-
下列各组比较正确的是( )
A. 酸性:H2SO4<H2SO3 B. 碱性:NaOH>Mg(OH)2
C. 最外层电子数:Ne=He D. 电子层数:P>Si
难度: 简单查看答案及解析
-
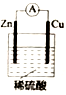
如右图所示,用石墨电极电解CuCl2溶液。下列分析正确的是( )

A. b为阳极、a为阴极 B. 通电一段时间后,d极附近观察到黄绿色气体
C. 阳极上发生的反应:Cu2++2e-=Cu D. 若电路中转移0.2mole-,则d极增重6.4g
难度: 中等查看答案及解析
-
下列物质中只含有一种分子的是( )
A. 二氯甲烷(CH2Cl2) B. 分子组成为C2H6O的有机物
C. 分子组成为C4H10的有机物 D. 聚乙烯
难度: 简单查看答案及解析
-
在一定条件下,对于密闭容器中进行的可逆反应:H2(g)+I2(g)
2HI(g),达到化学平衡状态的标志是( )
A. 正、逆反应速率都等于零 B. H2、I2的浓度相等
C. HI、H2、I2在容器中共存 D. HI、H2、I2的浓度均不再变化
难度: 中等查看答案及解析
-
下列实验能达到预期目的的是( )
A. 用分液漏斗分离溴和苯
B. 分馏石油时,将温度计插入石油液面下
C. 取样灼烧,可以鉴别白色纺织品是棉织品还是羊毛制品
D. 直接往淀粉水解液中加入新制氢氧化铜悬浊液并且加热,可检验淀粉水解产物
难度: 简单查看答案及解析
-
锌与过量的稀盐酸反应,为了加快反应速率,又不影响生成氢气的总量,可以采取的措施是( )
A. 加入浓盐酸 B. 加入一定量CuSO4固体 C. 加入适量的水 D. 降低温度
难度: 简单查看答案及解析
-
已知4NH3+5O2=4NO+6H2O ,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A. 2/3v(NH3)=v(H2O) B. 5v(O2)=6v(H2O) C. v(NH3)∶v(O2)=4∶5 D. 5/4v(O2)=v(NO)
难度: 简单查看答案及解析
-
1gH2燃烧生成液态水放出142.9kJ的热量,下列热化学方程式书写正确的是( )
A. 2H2(g)+O2(g)=2H2O(1)△H=-142.9 kJ/mol
B. 2H2(g)+O2(g)=2H2O(1)△H=-571.6kJ/mol
C. 2H2(g)+O2(g)=2H2O △H=-571.6 kJ/mol
D. H2(g)+l/2O2(g)=H2O(g) △H=-285.8 kJ/mol
难度: 简单查看答案及解析
-
某有机物的结构如图所示,有关该物质的描述不正确的是( )
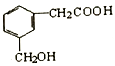
A. 能发生催化氧化反应
B. 不能发生水解反应
C. 1mol该有机物能与足量金属钠反应生成2gH2
D. 1mol该有机物能与足量碳酸氢钠反应生成2 molCO2
难度: 简单查看答案及解析
-
短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。X和Z为同主族元素,由X、Z两种元素形成的化合物是形成酸雨的主要物质。下列说法不正确的是( )
A. X的简单氢化物的热稳定性比W的强 B. Y的简单离子与X的具有相同的电子层结构
C. Z与Y属于同一周期 D. W、X、Y、Z原子的核外最外层电子数的总和为20
难度: 中等查看答案及解析