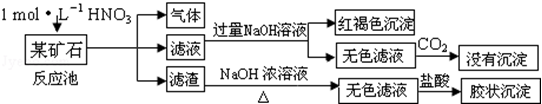
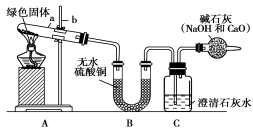
-
化学在生产和日常生活中有着重要的作用。下列有关说法正确的是( )
A. 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
B. 氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应
C. 国庆节期间燃放的焰火是某些金属元素焰色反应所呈现出来的色彩
D. 浓硫酸可刻蚀石英制艺术品
难度: 简单查看答案及解析
-
下列化学用语描述正确的是( )
A.NH4I的电子式:
B.漂白粉、石英都属于纯净物
C.烧碱、冰醋酸、干冰、胆矾均为电解质
D.C60、C70、金刚石、石墨均为碳的同素异形体
难度: 简单查看答案及解析
-
以NA表示阿伏加德罗常数的值,
下列说法正确的是( )
A.0.1 mol Fe与足量盐酸反应,转移的电子数为0.3 NA
B.0.1 mol/L氢氧化钠溶液中所含Na+数为0.1NA
C.1 mol Na2O2与水完全反应时转移电子数为2NA
D.46g NO
2和N2O4的混合气体中含有的原子个数为3NA
难度: 简单查看答案及解析
-
下列离子组在一定条件下能共存,当加入相应试剂后会发生化学变化,且所给离子方程式正确的是( )
选项
离子组
加入试剂
加入试剂后发生反应的
离子方程式
A
Fe2+、NO
、K+
稀硫酸
3Fe 2++NO
+4H+= 3Fe3++NO↑+2H2O
B
Fe3+、I-、ClO-
氢氧化钠溶液
Fe3++3OH-= Fe(OH)3↓
C
Ba2+、HCO
、Cl-
氢氧化钠溶液
H
CO
+OH-= CO
+H2O
D
Al3+、Cl-、NO
过量氢氧化钠溶液
Al3++3OH-= Al(OH)3↓
难度: 简单查看答案及解析
-
下列各组物质相互混合反应后,最
终有白色沉淀生成的是( )
①金属钠投入到FeCl2溶液中
②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过
量CO2
⑤向饱和Na2CO3溶液中通入过量CO2
A.①③④⑤ B.只有①④ C.只有②③ D.只有③④⑤
难度: 中等查看答案及解析
-
下列图示能达到实验目的的是( )
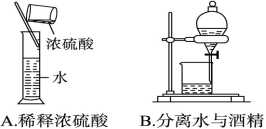
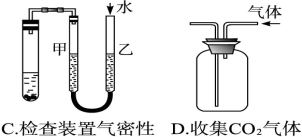
难度: 中等查看答案及解析
-
下列实验操作不正确的是的是( )
A. NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热
B. 除去Fe(OH)3胶体中混有的Cl- 离子,可用渗析的方法
C. 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗上口倒出
D. 实验中需2mol/L的Na2CO3溶液950mL,配制时应选用500mL容量瓶配制两次
难度: 简单查看答案及解析
-
下列除杂方案错误的是( )
选项
被提纯的物质
杂质
除杂试剂
除杂方法
A.
CO(g)
CO2(g)
NaOH溶液、浓H2SO4
洗气
B.
NH4Cl(aq)
Fe3+(aq)
NaOH溶液
过滤
C.
Cl2(g)
HCl(g)
饱和食盐水、浓H2SO4
洗气
D.
Na2CO3(s)
NaHCO3(s)
—
灼烧
难度: 简单查看答案及解析
-
①Na2CO3—制玻璃
②SiO2—太阳能电池
③干冰—人工降雨
④NaCl—制纯碱
⑤Al2O3—焊接钢轨
⑥NaClO—消毒剂
⑦Fe2O3—红色油漆或涂料
⑧MgO—耐火材料
A. 4 B. 5 C. 6 D. 7
难度: 简单查看答案及解析
-
下列关于同温同压下的两种气体12C18O和14N2的判断正确的是( )
A.体积相等时密度相等
B.原子数相等时具有的中子数相等
C.体积相等时具有的电子数相等
D.质量相等时具有的质子数相等
难度: 简单查看答案及解析
-
常温下,在溶液中可发生以下反应:
①H++Z-+XO
=X2++Z2+H2O(未配平),
②2M2++R2=2M3++2R-,
③2R-+Z2=R2+2Z-。由此判断下列说法正确的是
A.常温下反应2M2++Z2 = 2M3++2Z-不可以自发进行
B.R元素在反应②中被氧化,在③中被还原
C.反应①配平后,H2O的化学计量数为8
D.还原性强弱顺序为:X2+>Z->R->M2+
难度: 中等查看答案及解析
-
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O=2NO+HNO3+9HF,下列有关该反应的说法正确的是( )
A.NF3是氧化剂,H2O是还原剂
B.还原剂和氧化剂的物质的量之比是2∶
1
C.若生成0.2 mol HNO3,则转移0.2 mol电子
D.NF3在潮湿的空气中泄漏会产生红棕色气体
难度: 中等查看答案及解析
-
X、Y均为短周期元素,X位于IA族,X、Y能形成X2Y化合物,下列说法正确的是( )
A. X与Y形成的化合物中原子个数比可能为1 :1
B. X2Y不可能是共价化合物
C. X和Y分别形成的简单离子不可能具有相同电子层结构
D. 根据周期表递变规律判断X原子半径一定大于Y原子半径
难度: 中等查看答案及解析
-
一定质量的铜分别与足量的稀硝酸或浓硝酸完全反应,在相同条件下,用排水集气法收集产生的气体(假设产物气体只可能是NO或NO2).下列叙述一定正确的是( )
①硝酸浓度越大,消耗的硝酸越少
②硝酸浓度不同,生成的Cu(NO3)2的物质的量相同
③硝酸浓度越大,产生的气体越少
④用排水集气法收集到的气体在相同状况下体积相同.
A.只有② B.②④ C.③④ D.①②③
难度: 困难查看答案及解析
-
把一块镁铝合金投入到20 mL 1 mol/L的HCl溶液里,待合金完全溶解后,往溶液里加入1 mol/L的NaO
H溶液,生成沉淀的物质的量随加入NaOH溶液体积(mL)变化的
关系如图所示。下列说法中正确的是( )

A.镁铝合金具有很强的抗腐蚀能力,它不溶解在任何酸、碱或盐中
B.c值越大,合金中Al的含量越高
C.b值越大,合金中Mg的含量越高
D.假设c=25,整个实验过程中,只发生了4个离子反应
难度: 困难查看答案及解析
-
a molNa2O2和b molNaHCO3固体混合后,在密闭容器中加热到250℃,使其充分反应,当排出气体为两种气体时, a:b不可能为( )
A.3:4 B.4:5 C.2:3 D.3:2
难度: 困难查看答案及解析