-
空气中体积分数约为21%的气体是
A.氮气 B.氧气 C.二氧化碳 D.水蒸气
难度: 简单查看答案及解析
-
地壳中含量最多的金属元素是
A.铝 B.铁 C.氧 D.硅
难度: 中等查看答案及解析
-
决定元素种类的是
A.质子数 B.电子数 C.中子数 D.最外层电子数
难度: 中等查看答案及解析
-
下列物质中,属于氧化物的是
A.O2 B.KCl C.SO3 D.K2CO3
难度: 中等查看答案及解析
-
豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指
A.原子 B.分子 C.元素 D.单质
难度: 简单查看答案及解析
-
走进水果店就能闻到水果香味,人们能够闻到香味的原因是
A.分子在不断运动 B.分子间有间隔
C.分子由原子构成 D.分子的质量和体积都很小
难度: 中等查看答案及解析
-
碳酸氢钠是治疗胃酸过多的一种药剂,其俗称是
A.火碱 B.纯碱 C.熟石灰 D.小苏打
难度: 简单查看答案及解析
-
下列物质中,属于纯净物的是
A.食用醋 B.干冰 C.清洁空气 D.加碘食盐
难度: 中等查看答案及解析
-
下列金属中,活动性最强的是
A.镁 B.铜 C.锌 D.银
难度: 简单查看答案及解析
-
已知一种铁原子,原子核内有26个质子和30个中子,则该铁原子的核外电子数为
A.4 B.26 C.30 D.56
难度: 中等查看答案及解析
-
下列是人体中几种体液的正常pH,其中酸性最强的是
A.胆汁(6.8~7.4) B.唾液(6.6~7.1)
C.血浆(7.35~7.45) D.胃液(0.8~1.5)
难度: 简单查看答案及解析
-
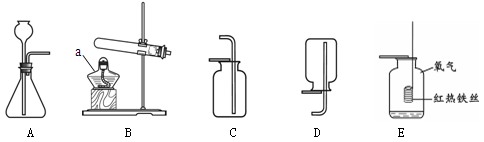
下列实验操作中,不正确的是
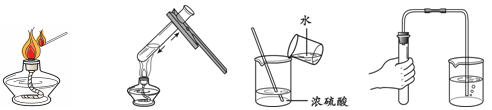
A.点燃酒精灯 B.加热液体 C.稀释浓硫酸 D.检查气密性
难度: 简单查看答案及解析
-
将下列固体分别放入水中,能形成溶液的是
A.冰 B.蔗糖 C.植物油 D.碳酸钙
难度: 中等查看答案及解析
-
鉴别一瓶气体是否为氧气,下列操作正确的是
A.闻气体的气味 B.倒入澄清石灰水
C.观察气体的颜色 D.插入带火星的木条
难度: 中等查看答案及解析
-
下列物质的用途中,只利用其物理性质的是
A.氧气用于气焊 B.二氧化碳用于制作碳酸饮料
C.干冰用于人工降雨 D.熟石灰用于改良酸性土壤
难度: 中等查看答案及解析
-
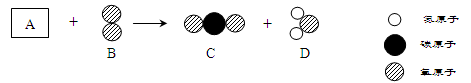
氨气(NH3)燃烧反应的化学方程式为4NH3 + 3O2 点燃 6H2O + 2N2。该反应属于
A.置换反应 B.化合反应 C.分解反应 D.复分解反应
难度: 中等查看答案及解析
-
在工作、生活中,为了防止事故,常采用一些安全措施,下列措施不安全的是
A.厨房煤气泄漏要关闭阀门、开窗通风 B.霉变的大米,要煮熟后食用
C.燃放烟花爆竹时,远离人群和可燃物 D.电器失火后首先要切断电源
难度: 简单查看答案及解析
-
氯酸钾(KClO3)中氯元素的化合价为
A.﹣1 B.﹢3 C.﹢5 D.﹢7
难度: 中等查看答案及解析
-
下列物质久置敞口容器中,质量会增加但不会变质的是
A.浓硫酸 B.氢氧化钠 C.食盐 D.浓盐酸
难度: 中等查看答案及解析
-
下列物质分别在氧气中燃烧,都可生成无色气体(常温下)的一组是
A.细铁丝和红磷 B.甲烷和红磷
C.氢气和木炭粉 D.木炭粉和一氧化碳
难度: 中等查看答案及解析
-
下列对教材中相关实验的分析不正确的是
A.电解水实验说明水由氢、氧两种元素组成
B.用黄铜片在铜片上刻划实验说明合金一般比纯金属硬度大
C.NaOH溶于水实验说明化学反应在生成新物质的同时还放出热量
D.向镁、锌、铁、铜中分别加入盐酸的实验得出镁、锌、铁的金属活动性比铜强
难度: 中等查看答案及解析
-
某同学对下列四个实验都设计了两种方案,两种方案均合理的是
选项
A
B
C
D
实验
目的
除去NaCl中的NaOH
鉴别盐酸、氢氧化钙、氯化钠三种溶液
检验CO中是否有少量CO2
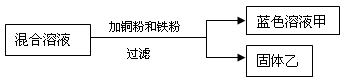
分离铜粉和碳粉
方案1
滴加适量稀硫酸
滴加紫色石蕊溶液
点燃
滴加稀硫酸
方案2
滴加适量稀盐酸
滴加碳酸钠溶液
通入紫色石蕊溶液
氧气中加热
难度: 中等查看答案及解析
-
氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂。
已知:① 氢化钙通常用氢气与钙加热制得。
② 氢化钙要密封保存,遇水反应生成氢氧化钙和氢气。
下列判断中正确的是
A.氢化钙的化学性质稳定
B.①中发生化合反应,②中发生复分解反应
C.氢化钙作为能源提供剂是因为与水反应能生成氢气
D.氢化钙可用于干燥潮湿的二氧化碳、氯化氢等气体
难度: 中等查看答案及解析
-
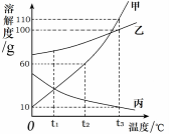
20 ℃时,取甲、乙、丙、丁四种纯净物各40 g,分别加入到四个各盛有100 g水的烧杯中,充分溶解,其溶解情况如下表:
物质
甲
乙
丙
丁
未溶解固体的质量 /g
8.4
4
0
18.4
下列说法正确的是
A.所得四杯溶液都是饱和溶液
B.丁溶液的溶质质量分数最大
C.20℃时四种物质溶解度的关系为:丁>甲>乙>丙
D.四杯溶液中各加入20 ℃的100 g水后,溶液质量相等,且均为不饱和溶液
难度: 中等查看答案及解析
-
现有两种金属单质组成的混合物。向100 g稀盐酸中加入该混合物,加入混合物的质量与生成氢气的质量关系如图所示。下列说法正确的是
A.若混合物为Zn和Cu,则m大于0.2 g
B.若混合物为Zn和Fe,则m可能是0.2 g
C.若混合物为Fe和Cu,稀盐酸中溶质质量分数为7.3%
D.若混合物为Fe和Cu,m为0.1 g,则混合物中Fe和Cu的质量比为1:1
难度: 中等查看答案及解析
-
(3分)氢气是最清洁的燃料,计算200 g氢气完全燃烧生成水的质量。
难度: 困难查看答案及解析





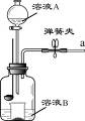 (1)检查装置气密性后,燃烧匙中放入少量的白磷,小烧杯内放入适量的碳酸钠粉末,组装好装置。打开弹簧夹,将溶液A缓慢加入到小烧杯内,溶液A是______,一段时间后,______(填写后续实验步骤和现象),关闭分液漏斗的活塞、弹簧夹,然后用凸透镜加热白磷,观察到白磷不燃烧,该实验过程的目的是______。
(1)检查装置气密性后,燃烧匙中放入少量的白磷,小烧杯内放入适量的碳酸钠粉末,组装好装置。打开弹簧夹,将溶液A缓慢加入到小烧杯内,溶液A是______,一段时间后,______(填写后续实验步骤和现象),关闭分液漏斗的活塞、弹簧夹,然后用凸透镜加热白磷,观察到白磷不燃烧,该实验过程的目的是______。