-
“金银花”一名出自《本草纲目》,其既能宣散风热,还善清解血毒。天然植物金银花提取物的主要成份为绿原酸(简称CA,分子式为C16H18O9)。绿原酸属于
A. 氧化物 B. 盐 C. 无机物 D. 有机物
难度: 简单查看答案及解析
-
下列关于乙烯的说法不正确的是
A. 密度比空气大 B. 是无色气体
C. 分子式为C2H4 D. 分子中含有碳碳双键
难度: 简单查看答案及解析
-
下列物质属于电解质的是
A. Fe B. KNO3 C. C2H5OH D. NaCl溶液
难度: 简单查看答案及解析
-
当光束通过下列分散系时,能观察到丁达尔效应的是
A. 白酒 B. 蒸馏水 C. 食盐水 D. 稀豆浆
难度: 简单查看答案及解析
-
在周期表中,下列各组元素位于同一主族的是
A. H、Na B. Mg、Al C. N、Si D. S、Cl
难度: 简单查看答案及解析
-
运输汽油的车上,贴有的危险化学品标志是
A.
 B.
B.  C.
C.  D.
D. 
难度: 简单查看答案及解析
-
糖类、油脂和蛋白质是生命活动所必需的营养物质。下列物质中不能发生水解反应的是
A. 淀粉 B. 植物油 C. 葡萄糖 D. 蛋白质
难度: 简单查看答案及解析
-
合金的应用极大地促进了人类社会的发展。下列不属于合金的是
A.狗头兽首铜像
B.柔性显示屏(基础材料:石墨烯)
C.流通硬币
D.潜水器外壳(钛、铝等)




A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列元素中,原子半径最大的是
A. F B. Cl C. Na D. Mg
难度: 简单查看答案及解析
-
钯(
)是航天、航空、航海、兵器和核能等高科技领域以及汽车制造业不可缺少的关键材料。钯原子核内中子数与核外电子数之差是
A. 106 B. 60 C. 46 D. 14
难度: 简单查看答案及解析
-
某粒子的结构示意图为
,关于该粒子的说法不正确的是
A. 核电荷数为17 B. 核外有3个电子层
C. 属于非金属元素 D. 在化学反应中容易得1个电子
难度: 简单查看答案及解析
-
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。一定条件下,恒容密闭容器中,发生反应:CO(g)+2H2(g)
CH3OH(g) 。下列能充分说明该反应已经达到化学平衡状态的是
A. 正、逆反应速率都等于零 B. CO、H2、CH3OH的浓度不再变化
C. CO、H2、CH3OH的浓度相等 D. CO、H2、CH3OH在密闭容器中共存
难度: 简单查看答案及解析
-
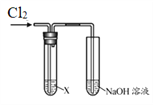
原电池是将化学能转变为电能的装置。关于下图所示原电池的说法不正确的是
A. Cu为正极,Zn为负极 B. 电子由铜片通过导线流向锌片
C. 正极反应式为2H+ + 2e-
H2↑ D. 原电池的反应本质是氧化还原反应
难度: 简单查看答案及解析
-
下列属于取代反应的是
A. 甲烷与氯气反应生成一氯甲烷 B. 乙烯与水反应生成乙醇
C. 乙醇与氧气反应生成乙醛 D. 乙烯与高锰酸钾溶液反应生成CO2
难度: 简单查看答案及解析
-
控制变量是科学研究的重要方法。已知反应:Na2S2O3 + H2SO4
S↓+ SO2↑+ H2O + Na2SO4,相同体积和浓度的Na2S2O3溶液与相同体积的稀硫酸分别在下列条件下发生反应,其中反应速率最快的是
A
B
C
D
t / ℃
20
20
40
40
c(H2SO4) / (mol·L−1)
0.1
0.5
0.1
0.5
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列物质的电子式书写正确的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
自然界的硫循环如下图所示,下列说法不正确的是
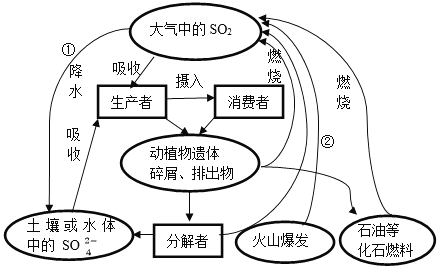
A. ①和②中硫元素均被氧化
B. ①是自然界形成酸雨的唯一原因
C. 含硫有机物和含硫无机物可相互转化
D. 控制化石燃料的使用可以减少SO2排放
难度: 简单查看答案及解析
-
下列行为不符合安全要求的是
A. 点燃CH4前,必须检验气体的纯度
B. 做实验剩余的金属钠不得直接丢弃在废液缸中
C. 大量氯气泄漏时,迅速离开现场并尽量往低处去
D. 配制稀硫酸时,将浓硫酸缓慢倒入水中并不断搅拌
难度: 简单查看答案及解析
-
下列物质用途与物质性质的对应关系中,不正确的是
选项
性质
用途
A
氧化铁呈红棕色
红色涂料
B
金属的焰色反应
制烟花
C
浓硫酸具有脱水性
干燥剂
D
液氨汽化时要吸收大量的热
制冷剂
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列说法中,正确的是
A. 33.6 L CO2的物质的量为1.5 mol
B. 34 g NH3物质的量为0.5 mol
C. 500 mL 0.1 mol·L−1 NaOH溶液中含有0.05 mol Na+
D. 1 mol NO2中含有的氧原子数约为6.02×1023
难度: 简单查看答案及解析
-
下列反应的离子方程式书写不正确的是
A. 氯化铁与铁粉:Fe 3+ +Fe === 2Fe2+
B. 金属钠与水:2Na + 2H2O === 2Na+ + 2OH- + H2↑
C. 稀盐酸与碳酸钙:CaCO3 + 2H+ === Ca2+ + CO2 ↑ + H2O
D. 铜与浓硝酸:Cu + 4H++ 2NO3-
Cu2++ 2NO2↑ + 2H2O
难度: 简单查看答案及解析
-
下列实验装置或操作与实验目的不相符的是
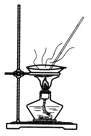


A.除去水中的泥沙
B.用Ca(OH)2和NH4Cl制取NH3
C.用自来水制取蒸馏水
D.配制100 mL0.1 mol·L−1 NaCl溶液
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列“推理或结论”与“实验操作及现象”不相符的一组是
选项
实验操作及现象
推理或结论
A
将蘸有浓盐酸的玻璃棒与蘸有浓氨水的玻璃棒靠近,产生大量白烟
NH3遇到HCl时反应生成NH4Cl晶体
B
向碘水中加入CC14,振荡,溶液分层,下层为紫红色
碘在CC14中的溶解度大于在水中的溶解度
C
将打磨后的镁条放入盛有稀盐酸的试管中,用手触摸试管外壁感觉变热
镁条与稀盐酸反应是放热反应
D
将某气体通入品红溶液,品红溶液褪色
该气体一定是SO2
A. A B. B C. C D. D
难度: 中等查看答案及解析