-
关于元素周期表的说法正确的是( )
A.元素周期表中有8个主族 B.ⅠA族的元素全部是金属元素
C.元素周期表有7个周期 D.短周期是指第一、二周期
难度: 中等查看答案及解析
-
化学与生活、社会密切相关。下列说法不正确的是( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
难度: 中等查看答案及解析
-
-NMR(核磁共振)可用于含碳化合物的结构分析,
表示的是( )
A.核外有13个电子,其中6个能参与成键
B.核内有6个质子,核外有7个电子
C.质量数是13,原子序数是6,核内有7个质子
D.质量数是13,原子序数是6,核内有7个中子
难度: 简单查看答案及解析
-
下列各组粒子中属于同位素的是 ( )
A.16O和18O B.H2O和D2O C.H2和D2 D.24Mg和24Na
难度: 简单查看答案及解析
-
下列物质中既有离子键,又有共价键的是( )
A.H2O B.CaCl2 C.KOH D.Cl2
难度: 中等查看答案及解析
-
下列化学电池不易造成环境污染的是( )
A.氢氧燃料电池 B.干电池 C.铅蓄电池 D.锌锰电池
难度: 简单查看答案及解析
-
下列反应的能量变化属于吸热反应的是( )
A.氯化铵与消石灰的反应 B.氢氧化钠溶液与盐酸反应
C.锌片与稀硫酸反应 D.钠与冷水反应
难度: 中等查看答案及解析
-
用铁片与稀硫酸反应制氢气时,下列措施不能使反应速率加快的是( )
A.加热 B.不用稀硫酸,改用98%的浓硫酸
C.滴加少量CuSO4溶液 D.不用铁片,改用铁粉
难度: 中等查看答案及解析
-
下列说法正确的是:( )
A.Na,Mg,Al还原性依次减弱 B.HCl,PH3,H2S稳定性依次减弱
C.NaOH,KOH,CsOH碱性依次减弱 D.S2-,Cl-,Ca2+半径依次增大
难度: 中等查看答案及解析
-
对于反应A2+3B2=2C来说,以下化学反应速率的表示中,反应速率最快的是( )
A.v(B2)=0.8 mol/ (L·s) B.v(A2)=0.4 mol/ (L·s)
C.v(C)=0.6 mol/ (L·s) D.v(B2)= 4.2 mol/ (L·s)
难度: 中等查看答案及解析
-
对于可逆反应2SO2+O2
2SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子 ( )
A.只存在于O2中 B.只存在于O2和SO3中
C.只存在于SO2和O2中 D.存在于SO2、O2和SO3
难度: 中等查看答案及解析
-
下列物质的电子式书写正确的是( )
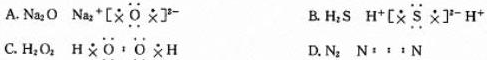
难度: 中等查看答案及解析
-
一定温度下,对反应2A(g)+B(s)
2C(g)能说明其达到平衡状态的是( )
A.容积中A、B、C三者共存
B.单位时间内反应的A与生成的C的物质的量之比为1:1
C.c(A):c(B):c(C)=2:1:2
D.气体的总质量不再发生变化
难度: 中等查看答案及解析
-
对已达化学平衡的下列反应 2X(g)+Y(g)
2Z(g),减小压强时,对反应产生的影响是( )。
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
难度: 中等查看答案及解析
-
反应4NH3(g)+5O2(g)===4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率(X)(反应物的消耗速率或产物的生成速率)可表示为( )
A.(NH3)=0.010 mol·L-1·s-1 B.(O2)=0.001 0 mol·L-1·s-1
C.(NO)=0.001 0 mol·L-1·s-1 D.(H2O)=0.045 mol·L-1·s-1
难度: 中等查看答案及解析
-
将4mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) === 2C(g)。若经2 s后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol·L-1·s-1 ②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1 ③2 s时物质A的转化率为50% ④2 s时物质B的浓度为0.7 mol·L-1 其中正确的是( )
A.①③ B.①④ C.②③ D.③④
难度: 中等查看答案及解析
-
在如右图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )
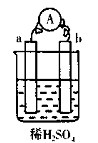
A.碳棒上有气体放出,溶液酸性变弱
B.a是正极,b是负极
C.导线中有电子流动,电子流向从a极到b极
D.a极上发生了氧化反应
难度: 中等查看答案及解析
-
在一定温度和压强下,合成氨反应达到平衡时,下列操作平衡不发生移动的是( )
A.恒温、恒压时充入氨气 B.恒温、恒容时充入氮气
C.恒温、恒容时充入氦气 D.恒温、恒压时充入氦气
难度: 中等查看答案及解析