-
下列叙述正确的是
A.1.00mol NaCl中含有6.02×1023个NaCl分子
B. 1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023
C.欲配置1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中
D.电解58.5g 熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠
难度: 中等查看答案及解析
-
X、Y、Z、W是原子序数依次增大的短周期元素,元素R为长周期元素,是日本地震造成核电站爆炸产生的污染物,且X、Z和R同主族。X 最外层电子数和其电子层数相同,Y最外层电子是其电子层数的3倍。Z、W是金属元素,最外层电子数之和为4,工业上一般通过电解氧化物的方法获得W的单质。则下列说法不正确的是
A.W、Z、R元素对应碱的碱性逐渐增强
B.R是一种柔软的金属,它的熔沸点高于金属钠
C.X和Y可形成原子个数比为1:1和2:1的化合物
D.Y、Z和W三种元素形成的化合物的水溶液呈碱性
难度: 中等查看答案及解析
-
“化学,让生活更美好”,下列叙述不能直接体现这一主旨的是
A.风力发电,让能源更清洁 B.合成光纤,让通讯更快捷
C.合成药物,让人类更健康 D.环保涂料,让环境更宜居
难度: 中等查看答案及解析
-
2011年11月1日“神州八号”成功发射,它和“天宫一号”在中国甘肃、陕西上空实现对接,我国探月工程迈出重要一步。据科学家预测,月球的土壤中吸附着数百万吨的32He,每百吨32He核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上,氦元素主要以42He的形式存在。下列说法正确的是
A.42He原子核内含有4个质子 B.32He原子核内含有3个中子
C.32He和42He互为同位素 D. 42He具有较强的金属活动性
难度: 中等查看答案及解析
-
下列有关物质的分类或归类不正确的是
①混合物:石炭酸、福尔马林、水玻璃、水银 ②化合物:CaCl2、烧碱、苯乙烯、HD
③电解质:明矾、胆矾、冰醋酸、硫酸钡 ④纯净物:干冰、冰水混合物、浓硫酸、水晶
⑤同位素:C、C、C ⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
A.①②③④ B.①②④⑥ C.①③④⑤ D.②④⑤⑥
难度: 中等查看答案及解析
-
下列有关化学用语的描述有错误的是( )
A.-OH 与
都可以表示羟基
B. Br-与
都可以表示溴离子
C.
与
都可以表示乙醇
D.
与O=C=O 都可以表示二氧化碳
难度: 中等查看答案及解析
-
已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,下列说法正确的是
A.Z元素的原子半径可能比Y元素的原子半径小
B.Z元素的最高化合价可能比Y元素的高
C.W的气态氢化物的稳定性一定比Y的强
D.Z的最高价氧化物的水化物的酸性一定比W的强
难度: 中等查看答案及解析
-
下列实验操作或对实验事实的叙述正确的是
①用稀盐酸洗涤盛放过石灰水的试剂瓶 ②配制浓硫酸和浓硝酸的混合酸时,将浓硫酸沿器壁慢慢加入到浓硝酸中,并不断搅拌; ③用pH试纸测得氯水的pH为2; ④用稀硝酸清洗做过银镜反应实验的试管; ⑤如果皮肤上不慎沾有苯酚,应立即用大量的NaOH稀溶液冲洗; ⑥用瓷坩埚高温熔融Fe(CrO2)2和Na2CO3的固体混合物; ⑦向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体; ⑧向某溶液加入NaOH浓溶液并加热能产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中含NH4+
A、①⑤⑦ B、③④⑦⑧ C、②③⑤⑥ D、①②④⑧
难度: 中等查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列有关NA 的叙述中正确的有
① 0.25molNa2O2中含有的阴离子数为0.5 NA
②0.05 mol熔融的KHSO4中含有阳离子数目为0.10 NA
③ 1 mol α-氨基乙酸(甘氨酸)分子中存在10 NA 对共用电子
④ 1mol/L的Na2CO3溶液中含有CO32-一定小于NA
⑤ 标准状况下,2.24L CHCl3含有的分子数为0.1 NA
⑥电解精炼铜时,当阳极溶解32 g铜时,转移的电子数为NA个
⑦ 2mol的Zn与足量的浓硫酸反应转移的电子数为4NA
A.2个 B.3个 C.4个 D.5个
难度: 中等查看答案及解析
-
下列离子方程式书写不正确的是
A.向KI与稀硫酸的混合溶液中通入氧气:4H++O2+4I-=2I2+2H2O
B.硫化钠的水解反应:S2-+H2O
HS-+OH-
C.4mol/L的KAl(SO4)2溶液与7mol/L的Ba(OH)2溶液等体积混合: 4Al3++7SO42—+7Ba2++14OH—=2Al(OH)3↓+2AlO2—+7BaSO4↓+4H2O
D.硝酸银溶液中滴加过量氨水:Ag++NH3·H2O=AgOH↓+NH4+
难度: 中等查看答案及解析
-
下列用来表示物质变化的化学反应中.正确的是
A.表示中和热的热化学方程式:H++OH— H2O △H= —57.3kJ·mol-l
B.硫酸氢铵溶液与少量氢氧化钠溶液混合共热的离子方程式:NH4++OH— NH3↑+H2O
C.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式: 3ClO— + 2Fe(OH)3 2FeO42—+3Cl—+H2O+4H+
D.高锰酸钾酸性溶液与双氧水反应的离子方程式:2MnO4—十5H2l8O2+6H+ 2Mn2++518 O2↑+8H2O
难度: 中等查看答案及解析
-
下图所示对实验仪器名称的标注或实验操作正确的是
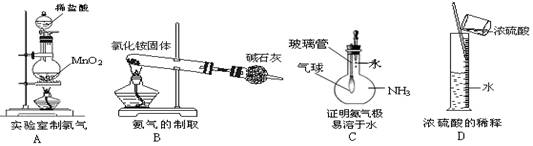
难度: 中等查看答案及解析
-
某无色溶液中可能含有Na+、K+、Fe3+、NH4+、Cu2+、SO42-、SO32-、CO32-、Cl-、
Br-这几种离子中的若干种,依次进行下列实验,观察到的现象记录如下:
①pH试纸检验,溶液的pH>7。
②取少量原溶液,向溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。
③另取少量原溶液,向溶液中滴加足量氯水,无气体产生,再加入CCl4振荡,静置后CCl4层呈橙色,用分液漏斗分液。
④向分液后的水溶液中加入Ba(NO3)2溶液和HNO3溶液,有白色沉淀产生,过滤。
⑤在滤液中加入AgNO3和HNO3的混合溶液有白色沉淀产生。
则关于原溶液的判断中不正确的是
A.肯定存在的离子是Na+、K+、SO32-、Br-
B.肯定不存在的离子是Fe3+、Cu2+、NH4+、SO42-、CO32-
C.无法确定原溶液中是否存在Cl-
D.若步骤④改用BaCl2溶液和盐酸的混合溶液,则对溶液中离子的判断无影响
难度: 中等查看答案及解析
-
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是
选项化合物
A
B
C
D
Y
CO2
Fe2O3
C2H5OH
FeCl3
W
MgO
Al2O3
C2H5ONa
CuCl2
难度: 中等查看答案及解析
-
高铁酸钾( K2FeO4)是一种新型的自来水处理剂,它的性质和作用是
A.有强氧化性,可消毒杀菌,还原产物能吸附水中杂质
B.有强还原性,可消毒杀菌,氧化产物能吸附水中杂质
C.有强氧化性,能吸附水中杂质,还原产物能消毒杀菌
D.有强还原性,能吸附水中杂质,氧化产物能消毒杀菌
难度: 中等查看答案及解析
-
有五个系列同族元素的物质,101.3 kP时测定它们的沸点(℃)如下表所示:
①
He -268.8
(a) -249.5
Ar -185.8
Kr -151.7
②
F2 -187.0
Cl2 -33.6
(b) 58.7
I2 184.0
③
(c) 19.4
HCl -84.0
HBr -67.0
HI -35.3
④
H2O 100.0
H2S -60.2
(d) -42.0
H2Te -1.8
⑤
CH4 -161.0
SiH4 -112.0
GeH4 -90.0
(e) -52.0
对应表中内容,下列各项中不正确的是( )
A.a、b、c的化学式分别为Ne、Br2、HF
B.系列②物质均有氧化性;系列③物质对应水溶液除c外其它均是强酸
C.系列④中各化合物的稳定性顺序为:H2O>H2S>H2Se>H2Te
D.上表内物质HF和H2O,由于氢键的影响,其分子特别稳定
难度: 中等查看答案及解析
-
小明做实验时不小心沾了一些KMnO4,皮肤上的黑斑很久才能消、除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:MnO4-+H2C2O4+H+→CO2↑+Mn2++□(未配平)。关于此反应的叙述正确的是
A.该反应的氧化剂是H2C2O4 B.1molMnO4-在反应中失去5mol电子
C.该反应右框内的产物是OH- D.配平该反应后,H+的计量数是6
难度: 中等查看答案及解析
-
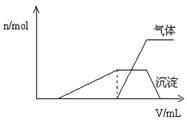
用含1 mol HCl的盐酸酸化含1 mol MgSO4的溶液,当向其中滴加1 mol/L 的Ba(OH)2 溶液时,产生沉淀的物质的量(n)与加入Ba(OH)2 溶液体积(V)间的关系图正确的是

难度: 中等查看答案及解析