-
有关下列能量转化的认识不正确的是( )
A.植物的光合作用使得太阳能转化为了化学能
B.人类使用照明设备是将电能转化为了光能
C.生物体内的化学变化过程在能量转化上比在体外发生的一些能量转化更为合理、有效
D.燃料燃烧时只是将化学能转化为了热能
难度: 简单查看答案及解析
-
下列粒子半径之比小于1的是( )。
A. r (Na+)/ r (Na) B. r (Cl-)/ r (Cl) C. r (Na)/ r (Mg) D. r (Ca)/ r (Mg)
难度: 中等查看答案及解析
-
下列说法中正确的是
A.原电池是把电能转变为化学能的装置
B.原电池中电子流出的一极是负极,发生氧化反应
C.原电池的两极发生的反应均为氧化还原反应
D.形成原电池后,原电池中的阳离子向负极方向移动
难度: 简单查看答案及解析
-
下列元素中,最高正化合价数值最大的是( )。
A. C B. F C. S D. Ne
难度: 简单查看答案及解析
-
已知某粒子
,则元素R的原子序数是( )。
A. Z B. A-Z C. Z-n D. Z+n
难度: 中等查看答案及解析
-
元素的性质随着元素原子序数的递增而呈周期性变化的原因是( )。
A. 元素原子的核外电子排布呈周期性变化
B. 元素的原子半径呈周期性变化
C. 元素的化合价呈周期性变化
D. 元素的金属性、非金属性呈周期性变化
难度: 简单查看答案及解析
-
有A、B、C、D四种金属,投入水中只有D反应放出氢气,将A投入C的盐溶液中可置换出金属C,B的最高价氧化物的水化物碱性比A的最高价氧化物的水化物碱性强,则四种金属的金属性强弱顺序正确的是( )
A. A>B>C>D B. D>B>A>C C. D>A>C>B D. C>A>B>D
难度: 中等查看答案及解析
-
下列事实不能说明非金属性Cl>I的是( )。
A. Cl2+2I-==2Cl-+I2 B. 稳定性:HCl>HI
C. 酸性:HClO4>HIO4 D. 酸性:HClO3>HIO3
难度: 中等查看答案及解析
-
下列说法错误的是( )。
A. 原子半径:F<Mg<K B. 稳定性:PH3>H2S>NH3
C. 酸性:H3PO4<H2SO4<HClO4 D. 碱性:Al(OH)3<Mg(OH)2<KOH
难度: 中等查看答案及解析
-
运用元素周期律分析下面的推断,其中不正确的是
A.锂(Li)与水反应比钠与水反应剧烈
B.砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸
C.在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂
D.HBrO4的酸性比HIO4的酸性强
难度: 中等查看答案及解析
-
某种元素R原子的核外电子数等于核内中子数,该元素单质2.8 g与氧气充分反应,可得到6 g化合物RO2,则该种元素R在周期表中的位置是( )
A. 第二周期第ⅣA族 B. 第三周期第ⅣA族
C. 第三周期第ⅥA族 D. 第二周期第ⅥA族
难度: 中等查看答案及解析
-
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
A. 质子数:c>d B. 离子的还原性:Y2->Z-
C. 氢化物的稳定性:H2Y>HZ D. 原子半径:X<W
难度: 中等查看答案及解析
-
主族元素R的原子的电子式可表示为 ::
· 。 该元素组成的以下物质,其化学式肯定错误的是 ( )
A. 含氧酸化学式可能为H3RO4 B. 含氧酸化学式可能为HRO3
C. 气态氢化物化学式为RH5 D. 最高价氧化物化学式为R2O5
难度: 中等查看答案及解析
-
下列含有共价键的化合物是( )
A.HI B. NaOH C. Br2 D. NaCl
难度: 中等查看答案及解析
-
下列电子式书写正确的是:

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A.O2分子间存在着非极性共价键
B.CO2分子内存在着极性共价键
C.SO2与H2O反应的产物是离子化合物
D.盐酸中含有H+和Cl-,故HCl为离子化合物
难度: 中等查看答案及解析
-
下列用电子式表示物质的形成过程正确的是 ( )
A.
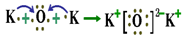 B.
B. 
C.
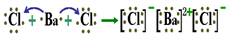 D.
D. 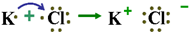
难度: 中等查看答案及解析
-
“摇摇冰”是一种即用即冷的饮料。吸食时将饮料罐隔离层中的化学物质和水混合后摇动即会制冷。该化学物质可能是
A.氯化钠 B.固体硝酸铵 C.生石灰 D.蔗糖
难度: 中等查看答案及解析
-
对于放热反应
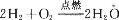 ,下列说法正确的是
,下列说法正确的是A.产物H20所具有的总能量高于反应物H2和O2所具有的总能量
B.反应物H2和O2所具有的总能量高于产物H2O所具有的总能量
C.反应物H2和O2所具有的总能量等于产物H2O所具有的总能量
D.反应物H2和02具有的能量相等
难度: 中等查看答案及解析
-
下列图示变化为吸热反应的是

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X和Y组成原电池时,Y为电池的负极。X、Y、Z三种金属的活动性顺序为( )
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Y>Z>X
难度: 中等查看答案及解析
-
某原电池的离子方程式是 Zn + Cu2+ = Zn2+ + Cu,该原电池正确的组成是 ( )
正极
负极
电解质溶液
A.
Cu
Zn
HCl
B.
Zn
Cu
CuSO4
C.
Cu
Zn
CuSO4
D.
Cu
Zn
ZnCl2
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列各装置不能构成原电池的是(电解质溶液均为稀硫酸)( )

A. A B. B C. C D. D
难度: 中等查看答案及解析
-
人造地球卫星用到的一种高能电池——银锌蓄电池,其电池的电极反应式为Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是
A.负极,并被氧化
B.正极,并被还原
C.负极,并被还原
D.正极,并被氧化
难度: 中等查看答案及解析
-
下右图是氢氧燃料电池构造示意图。关于该电池的说法不正确的是

A.a极是负极
B.正极的电极反应是:O2+2H2O+4e-=4OH-
C.电流由b通过灯泡流向a
D.氢氧燃料电池是环保电池
难度: 中等查看答案及解析
