-
是γ射线放射源,可用于农作物诱变育种,我国用该方法培育出了许多农作物新品种,下列叙述正确的是
A.60是Co元素的相对原子质量
B.由Co的不同种同位素组成的单质,其化学性质与物理性质均不同
C.60是
这种核素的质量数
D.
原子中,中子数是27,电子数是33
难度: 中等查看答案及解析
-
有机化学知识在生活中应用广泛,下列说法错误的是
A.利用天然气做燃料可以有效地减少“温室效应”的气体产生
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
C.可以用浸泡过高锰酸钾溶液的硅土来吸收水果或花朵产生的乙烯,达到保鲜目的
D.从石油中可以获得乙烯,乙烯是一种重要的基本化工原料
难度: 中等查看答案及解析
-
有关化学用语正确的是
① 羟基的电子式
② 乙烯的结构简式:CH2CH2
③硫化氢的电子式 H+
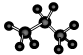
2-H+ ④丙烷分子的球棍模型:
⑤ 苯分子的比例模型
⑥甲烷的结构式
A.①④ B.②③④ C.④⑤⑥ D.②③⑤
难度: 中等查看答案及解析
-
下列有关物质结构和元素周期律的表述正确的是
A.ⅦA族元素是同周期中非金属性最强的元素
B.第二周期ⅣA族元素的原子核电荷数和中子数分别为6
C.主族元素的最高正价均等于其族序数
D.非金属元素的气态氢化物溶于水后,水溶液均为酸性
难度: 中等查看答案及解析
-
下列关于实验现象的描述错误的是
A.铜锌原电池中铜是正极
B.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D.把锌粒放入盛有盐酸的试管中,加几滴氯化铜溶液,气泡放出速率加快
难度: 中等查看答案及解析
-
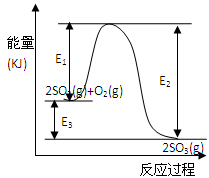
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是
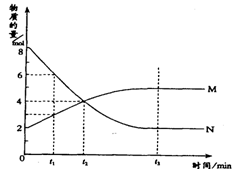
A.反应的化学方程式为2 M
N
B.t2时,正逆反应速率相等达到平衡状态
C.t1时,N的浓度是M浓度的2倍
D.t3时,正反应速率大于逆反应速率
难度: 中等查看答案及解析
-
下列说法中正确的一组是
A.H2和D2互为同位素;
B.
互为同分异构体
C.正丁烷和异丁烷是同系物
D.
是同一种物质
难度: 中等查看答案及解析
-
科学家对土星的最大卫星——土卫六的探测数据分析发现,土卫六的大气层中含有95%的氮气,剩余的气体为甲烷和其它碳氢化合物。关于甲烷和碳氢化合物的叙述错误的是
A.甲烷是含碳量最低的碳氢化合物
B.所有的碳氢化合物分子组成均符合Cn H2n+2的通式
C.碳氢化合物均不溶于水
D.碳氢化合物分子中的化学键一定有极性键,也可能有非极性键
难度: 中等查看答案及解析
-
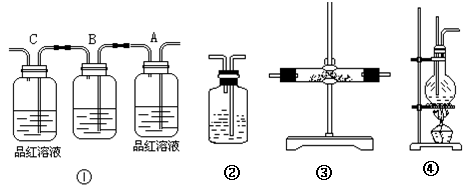
下列各组混合物,能用分液漏斗分开的是
①四氯化碳和水 ②苯和溴苯 ③乙醇和水 ④苯和水 ⑤硝基苯和水 ⑥苯和四氯化碳
A.①②③ B.②④⑥ C.①④⑤ D.④⑤⑥
难度: 中等查看答案及解析
-
下列文字表述与反应方程式对应且正确的是
A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br- + Ag+==AgBr↓
B.用醋酸除去水垢:CaCO3 + 2H+==Ca2+ + H2O + CO2↑
C.利用腐蚀法制作印刷线路板:Fe3+ + Cu == Fe2+ + Cu2+
D.实验室用液溴和苯在催化剂作用下制溴苯:
难度: 中等查看答案及解析
-
如图为短周期的一部分,推断关于Y、Z、M的说法正确的是
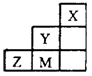
A.非金属性:Y>Z>M
B.ZM2分子各原子均满足8e-稳定结构
C.原子半径:M>Z>Y
D.Y离子的结构示意图可表示为:
难度: 中等查看答案及解析
-
主族元素X、Y、Z的离子为aX+、bY2—、cZ—,半径大小关系是aX+< cZ—< bY2—下列说法错误的是
A.b一定小于c B.单质的还原性X>Z
C.Y2—的还原性大于Z ¯ D.X可位于Y的上一周期、下一周期或同周期
难度: 中等查看答案及解析
-
A、B两元素的原子分别失去2个电子形成稳定结构时,A吸收的能量大于B吸收的能量;C、D两元素的原子分别得到一个电子形成稳定结构时,D放出的能量大于C放出的能量。若A、B、C、D间分别形成化合物时,属于离子化合物可能性最大的是
A.AD2 B.BC2 C.AC2 D.BD2
难度: 中等查看答案及解析
-
如下图,先向B中充入2molX、2molY,关闭活塞K,再向A充入1molX、1molY,使起始时A、B的体积相等都等于a L,在相同温度和催化剂存在的条件下,两容器中各自发生下述反应,X(g)+ Y(g)
2 Z(g)+W(g); A保持恒压,B保持恒容,达平衡时,A的体积为1.4a L 。下列说法错误的是
A.反应速率:v(B)
>v(A)
B.A容器中X的转化率为 80%
C.A中混合气体密度不再变化能够证明 A中反应达到平衡状态
D.B中混合气体密度不再变化能够证明 B中反应达到平衡状态
难度: 中等查看答案及解析
-
Li-Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li+ + FeS + 2e- == Li2S + Fe ,有关该电池的下列叙述中正确的是
A.该电池的电池反应式为:2Li + FeS == Li2S + Fe
B.Li-Al合金在电池中作为正极材料
C.负极的电极反应式为:Al — 3e- == Al3+
D.Li-Al/FeS电池中,电子经外电路流入Li-Al极
难度: 中等查看答案及解析
-
利用下列反应制备括号中的物质,不合理的是
A.乙烯与氯气加成(1,2-二氯乙烷)
B.乙烯与水加成(乙醇)
C.等物质的量的氯气与乙烷在光照条件下反应(氯乙烷)
D.氯气与苯用氯化铁做催化剂反应(氯苯)
难度: 中等查看答案及解析
-
某化合物的分式为C5H11Cl,分析数据表明:分子中有两个—CH3、两个—CH2—、一个
和一个—Cl,则它的可能结构有几种
A.2种 B.3种 C.4种 D.5种
难度: 中等查看答案及解析
-
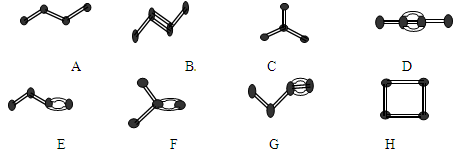
下列物质中所有原子都有可能在同一平面上的是

难度: 中等查看答案及解析
-
某烃的结构简式为
,它可能具有的性质是
A.它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色
B.它既能使溴水褪色,也能使酸性高锰酸钾溶液褪色
C.易溶于水,也易溶于有机溶剂
D.能发生加成反应,一定条件下1mol该有机物最多可与4mol氢气加成
难度: 中等查看答案及解析
-
a mL三种气态烃的混合物和足量的氧气混合点燃爆炸后,恢复到原来的状态(常温常压),气体体积共缩小2a mL(不考虑二氧化碳的溶解)。则三种烃可能的组合是
A.CH4、C2H4、C3H4任意体积比
B.CH4、C3H6、C2H2保持C3H6∶C2H2=1∶ 2(物质的量之比)
C.C2H6、C4H6、C2H2同条件下体积比为2∶1∶1
D.C3H8、C4H8、C2H2质量比为11∶14∶26
难度: 中等查看答案及解析