-
证明某溶液只含有Fe2+而不含有Fe3+的实验方法最好是 ( )
A. 先滴加氯水,再滴加KSCN溶液后显红色
B. 先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C. 滴加NaOH溶液,先产生白色沉淀,后变灰绿,最后呈红褐色
D. 只需滴加KSCN溶液
难度: 简单查看答案及解析
-
“世界地球日”即每年的4月22日,是一项世界性的环境保护活动。下列行为中不利于环境保护的是( )
A. 严格履行《京都议定书》,控制温室气体的排放
B. 大量开采煤、石油及天然气以满足工业发展的需要
C. 加强新能源研究,使用压缩天然气、氢气作汽车燃料
D. 研发可降解塑料或代用品,控制白色污染
难度: 中等查看答案及解析
-
下列物质中,属于混合物的是
A. 水玻璃 B. 液氯 C. 小苏打 D. 明矾
难度: 中等查看答案及解析
-
下列物质的变化,能通过一步化学反应完成的是( )
A. Al→Al(OH)3 B. N2→NO2
C. SiO2→Na2SiO3 D. SiO2→H2SiO3
难度: 中等查看答案及解析
-
材料与化学密切相关。下列物质与材料对应关系不正确的是
A. 晶体硅——光导纤维 B. 氧化铝——耐火材料
C. 铁碳合金——碳素钢 D. 硅酸盐——普通玻璃
难度: 中等查看答案及解析
-
下列药品的保存方法中,不正确的是( )
A. 钠和钾保存在煤油中
B. 盛放氢氧化钠溶液的瓶子不能用磨口玻璃塞
C. 氢氟酸要盛放在玻璃瓶中
D. 漂白粉保存在密闭容器中
难度: 中等查看答案及解析
-
已知水和苯不互相溶,苯不与钠反应,在烧杯中加水和苯(密度:0.88 g/mL)各50 mL。将一小粒金属钠(密度:0.97 g/mL)投入烧杯中,观察到的现象可能是
A. 钠在水层中反应并四处游动
B. 钠停留在苯层中不发生反应
C. 钠在苯的液面上反应并四处游动
D. 钠在苯与水的界面处反应,可能做上下跳动
难度: 中等查看答案及解析
-
已知甲、乙、丙、X是四种中学化学中常见的物质,其转化关系如图所示.则甲和X不可能是( )

A. 甲为C,X为O2 B. 甲为SO2,X为NaOH溶液
C. 甲为Fe,X为Cl2 D. 甲为AlCl3,X为NaOH溶液
难度: 中等查看答案及解析
-
在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象和结论一致且正确的是( )
A. 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在
B. 溶液呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在
C. 用盐酸酸化后,滴入AgNO3溶液产生白色沉淀,说明氯水中有Cl-存在
D. 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 在常温常压下,11.2L H2含有的分子数为0.5NA
B. Na2O2和Na2O中阳离子和阴离子个数比分别为1:1和2:1
C. 在标准状况下,22.4L SO3含有的原子数为4NA
D. 7.1g Cl2与足量的氢氧化钠溶液反应转移电子数为0.1NA
难度: 中等查看答案及解析
-
25 ℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A. 在强酸性溶液中:Na+、Cl-、K+、SiO32-
B. 与铝反应产生氢气的溶液中:HCO3-、NH4+、NO3-、Ca2+
C. 无色溶液中:Cu2+、NO3-、Cl-、H+
D. 在强碱性溶液中:Na+、K+、AlO2-、Cl-
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是( )
A. 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑
B. 铁粉与氯化铁溶液反应:
C. 氯气与水的反应:Cl2+ H2O ═ 2H+ + Cl- + ClO-
D. 漂白粉溶液中通入过量的CO2:ClO- + CO2 + H2O ═ HClO + HCO3-
难度: 中等查看答案及解析
-
下列离子在溶液中因发生氧化还原反应而不能大量共存的是( )
A. HCO3-、NH4+、H+、Cl- B. Al3+、OH-、Na+、Cl-
C. Na+、 H+ 、Fe2+、NO3- D. Mg2+、Fe3+、NO3-、SCN-
难度: 中等查看答案及解析
-
检验SO2气体中是否混有CO2气体,可采用的方法是( )
A. 通过品红溶液
B. 通过澄清石灰水
C. 先通过氢氧化钠溶液,再通过澄清石灰水
D. 先通过酸性高锰酸钾溶液,再通过澄清石灰水
难度: 中等查看答案及解析
-
下列有关焰色反应及其操作的说法正确的是
A. 焰色反应是化学变化
B. Na与NaCl在灼烧时火焰颜色相同
C. 铂丝在做完氯化钠溶液的焰色反应后,用稀硫酸洗净,再蘸取少量的K2SO4溶液,重复以上实验
D. 用洁净的铂丝蘸取某溶液,放在火焰上灼烧,观察到黄色火焰,则证明该溶液中一定有Na+,没有K+
难度: 中等查看答案及解析
-
下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的物质是( )
① NaHCO3; ② Al2O3; ③ Al(OH)3; ④ Al
A. ③④ B. ②③ C. ①③④ D. 全部
难度: 中等查看答案及解析
-
两种金属混合粉末15g,与足量的盐酸反应时生成11.2L H2(标况下),符合上述情况的金属混合物是( )
A. Mg、Fe B. Zn、Ag C. Fe、Zn D. Mg、Al
难度: 中等查看答案及解析
-
下列四种有色溶液与SO2 作用,均能褪色,其实质相同的是( )
①品红溶液 ②酸性KMnO4溶液 ③溴水 ④滴有酚酞的NaOH溶液
A. ①④ B. ②③ C. ②③④ D. ①②③
难度: 中等查看答案及解析
-
甲、乙、丙、丁分别是Al2(SO4)3、FeSO4、NaOH、BaCl2四种物质中的一种,若将丁溶液滴入乙溶液中,有白色沉淀生成,继续滴加则沉淀消失;丁溶液滴入甲溶液中,无明显现象,据此可推断丙物质是
A. Al2(SO4)3 B. NaOH C. BaCl2 D. FeSO4
难度: 中等查看答案及解析
-
向100mL12mol/L的浓盐酸中加入足量的二氧化锰并加热,被还原的盐酸的物质的量是( )
A. 等于1.2mol B. 大于0.6mol,小于1.2mol
C. 等于0.60mol D. 小于0.60mol
难度: 中等查看答案及解析
-
下列除杂试剂的选择或除杂操作不正确的是( )
选项
括号内为杂质
除杂试剂
除杂操作
A
Fe(Al)固体
NaOH
充分反应后过滤
B
Na2CO3(NaHCO3)溶液
CO2
通入过量的CO2
C
FeCl3(FeCl2)溶液
Cl2
通入过量的Cl2
D
CO2(HCl)气体
饱和NaHCO3溶液
洗气
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
将某些化学知识用图像表示,可以收到直观、简明的效果。下列图象所表示的化学知识中,明显不正确的是( )

A. A B. B C. C D. D
难度: 困难查看答案及解析
-
某同学用下图所示的装置及药品进行比较酸性强弱的实验,一段时间后试管②中有胶冻状物质生成。下列说法正确的是( )

A. 用带有玻璃塞的试剂瓶盛装Na2SiO3溶液
B. 试管①中反应的离子方程式是:Na2CO3+ 2H+ = 2Na+ + CO2↑+ H2O
C. 该实验可以证明酸性:盐酸>碳酸>硅酸
D. 若将盐酸换成硫酸,能证明酸性:硫酸>碳酸>硅酸
难度: 中等查看答案及解析
-
把盛有NO2和N2的混合气体的试管倒立在盛水的水槽中,最终液面上升到距试管底部2/3处,则原混合气体中NO2和N2的体积比是
A.1∶1 B.1∶2 C.2∶1 D.3∶1
难度: 中等查看答案及解析
-
某溶液中可能含有H+,Na+,Ba2+,Mg2+,Fe3+,Al3+,SO42﹣,CO32﹣等离子,当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示,下列判断正确的是( )
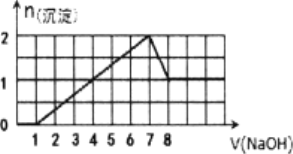
A. 原溶液中一定含有H+、Fe3+、Al3+,可能含Ba2+
B. 原溶液中含Fe3+和Al3+,物质的量之比为l:l
C. 原溶液中可能含有CO32﹣
D. 反应最后形成的溶液中含有的溶质只有NaAlO2
难度: 中等查看答案及解析



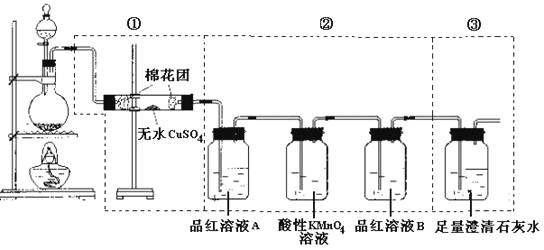
 ,产生的所有气体产物,选用了下图所示实验装置。
,产生的所有气体产物,选用了下图所示实验装置。