-
下列做法不能体现低碳生活的是
A. 注意节约用水 B. 减少食品加工过程
C. 发展氢能和太阳能 D. 大量使用化石燃料
难度: 简单查看答案及解析
-
有一种气体的质量是14.2g,体积是4.48升(标况下),该气体的摩尔质量是 ( )
A. 28.4 B. 28.4g·mol-1
C. 71 D. 71g·mol-1
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 32gO2占有的体积约为22.4L
B. 22.4LN2含有阿伏加德罗常数个氮气分子
C. 在标准状况下,22.4L水的质量约为18g
D. 22g二氧化碳与标准状况下11.2LHCl含有相同的分子数
难度: 简单查看答案及解析
-
A. 蒸发结晶操作时,当有大量晶体析出时停止加热,用余热蒸干
B. 蒸馏操作时,应使温度计水银球插入液态混合物中
C. 分液操作时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
D. 萃取操作时,萃取剂要和原溶剂互不相溶,且不能与溶质和溶剂反应
难度: 简单查看答案及解析
-
下列溶液中Cl--浓度由大到小的顺序是( )
①200 mL 2 mol/L MgCl2溶液 ②1000 mL 2.5mol/L NaCl溶液 ③300 mL 5 mol/L KCl溶液 ④250 mL 1 mol/LFeCl3溶液
A. ②③①④ B. ④①②③ C. ①④②③ D. ③①④②
难度: 简单查看答案及解析
-
将10.6
溶于水配制成1000
溶液,从中取出20
,该溶液中
的物质的量浓度为( )
A. 0.1
B. 0.2
C. 0.05
D. 0.025
难度: 简单查看答案及解析
-
分类是学习化学的方法之一,下列各组物质是按氧化物、酸、碱、盐顺序排列的一组是
A.氢氧化铁、硝酸、火碱、氯化钠 B.干冰、碳酸、纯碱、硫酸钾
C.水、硫酸、熟石灰、氯化钾 D.氨水、醋酸、氢氧化铁、食盐
难度: 简单查看答案及解析
-
下列物质在一定条件下能够导电,但属于非电解质的是
A. 食盐 B. 氨气 C. 硫酸 D. 蔗糖
难度: 简单查看答案及解析
-
下列关于胶体的叙述不正确的是
A. 胶体区别于其他分散系的本质特征是分散质的微粒直径在10-7 ~10-9m之间
B. 用平行光照射NaCl溶液和Fe(OH)3胶体,可以加以区分
C. 把FeCl3饱和溶液与NaOH溶液混合,以制取Fe(OH)3胶体
D. 除去Fe(OH)3胶体中的H+、Cl-,可用渗析的实验方法
难度: 简单查看答案及解析
-
某溶液中存在大量的Ba2+、Ag+、NH4+,该溶液中还可能大量存在的离子是
A.OH- B.Cl- C.SO42- D.NO3-
难度: 中等查看答案及解析
-
能用H++OH-=H2O来表示的化学反应是
A. 氢氧化镁和稀盐酸反应 B. Ba(OH)2溶液滴入稀硫酸中
C. 澄清石灰水和稀硝酸反应 D. 二氧化碳通入澄清石灰水中
难度: 简单查看答案及解析
-
下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A.
B.
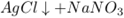
C.
D.
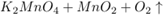
难度: 中等查看答案及解析
-
苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色(Fe2+)变为棕黄色(Fe3+)。若榨汁时加入维生素C,可有效防止这种现象发生。这说明维生素C具有( )
A. 氧化性 B. 还原性 C. 碱性 D. 酸性
难度: 简单查看答案及解析
-
对于反应3Cl2+6NaOH
5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A. Cl2是氧化剂,NaOH是还原剂
B. 被氧化的氯原子和被还原的氯原子的物质的量之比为5∶1
C. Cl2既做氧化剂又做还原剂
D. 氧化剂得电子数与还原剂失电子数之比为5∶1
难度: 简单查看答案及解析
-
下列化学反应既属于氧化还原反应,且水做氧化剂的是( )
A. 2F2+2H2O=4HF+O2 B. 2Na+2H2O=2NaOH+H2↑
C. CaO+H2O=Ca(OH)2 D. H2+CuO = Cu+H2O
难度: 中等查看答案及解析
-
取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是:①金属先熔化;②在空气中燃烧,放出黄色火花;③燃烧后得白色固体;④燃烧时火焰为黄色;⑤燃烧后生成浅黄色固体物质 ( )
A.①② B.①②③ C.①④⑤ D.④⑤
难度: 中等查看答案及解析
-
氢氧化铝可作为治疗某种胃病的内服药,这是利用了氢氧化铝的( )
A. 酸性 B. 碱性 C. 两性 D. 氧化性
难度: 简单查看答案及解析
-
下列离子的检验方法合理的是( )
A. 向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B. 向某溶液中通入Cl2,然后再加入KSCN溶液变红色,则原溶液中含有Fe2+
C. 向某溶液中加入NaOH溶液,得到红褐色沉淀,说明溶液中含有Fe3+
D. 向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明溶液中含有Fe2+,不含有Mg2+
难度: 简单查看答案及解析
-
为了除去铁粉中的少量铝粉,可以选取下列哪种溶液( )
A. 浓盐酸 B. 浓硝酸 C. 浓硫酸 D. 浓氢氧化钠溶液
难度: 中等查看答案及解析
-
下列说法错误的是:
A.钠在空气燃烧时先熔化,再燃烧,最后所得的产物是Na2O2
B.铝因在空气中形成了一薄层致密的氧化膜,保护内层金属,故铝不需特殊保护
C.铝制品在生活中非常普通,是因为铝非常不活泼
D.铁因在潮湿的空气中形成的氧化物疏松,不能保护内层金属
难度: 简单查看答案及解析