-
将某铁铝合金样品均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,同温同压下产生的气体体积比为3∶2,则样品中铁、铝的物质的量之比为( )
A. 3∶2 B. 2∶1 C. 3∶4 D. 4∶3
难度: 中等查看答案及解析
-
某无色溶液含有下列离子中的若干种:H+、NH4+、Fe3+、Ba2+、Al3+、CO32–、Cl–、OH–、NO3–。向该溶液中加入铝粉,只放出H2,则溶液中能大量存在的离子最多有
A. 3种 B. 4种 C. 5种 D. 6种
难度: 中等查看答案及解析
-
某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
A. K+、Na+、HCO3-、NO3- B. Na+、SO42-、Cl-、ClO-
C. H+、Mg2+、SO42-、NO3- D. Ag+、K+、NO3-、Na+
难度: 困难查看答案及解析
-
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
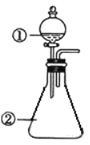
①中物质
②中物质
预测②中的现象
A
稀盐酸
碳酸钠与氢氧化钠的混合溶液
立即产生气泡
B
浓硝酸
用砂纸打磨过的铝条
剧烈反应
C
氯化铝溶液
浓氢氧化钠溶液
立即产生大量白色沉淀
D
亚硫酸钠溶液
高锰酸钾酸性溶液
溶液逐渐褪色
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
现象或事实
解释
A
二氧化硅是生产光纤的原料
二氧化硅熔点高、硬度大、具有半导性
B
氧化铝是一种较好的耐火材料
氧化铝是一种难熔物质
C
食品的包装盒内常有小袋包装的硅胶或生石灰
其作用为防止富脂食品被氧化
D
铜制器皿表面生成铜绿
Cu与CO2、H2O反应生成碱式碳酸铜
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
有五种化合物:①Mg(HSO3)2,②Al(OH)3 ③Na[Al(OH)4], ④(NH4)2CO3,⑤Al2O3。跟盐酸和NaOH溶液都反应的是
A. ②④ B. ①②③ C. ①②④⑤ D. ③④⑤
难度: 简单查看答案及解析
-
下列物质间的每步转化只需通过一步反应就能实现的是
A. S→SO3→H2SO4→Na2SO3 B. Al→Al (OH)3→Al2O3→Na[Al(OH)4]
C. Na→Na2O2→Na2CO3→NaOH D. Si→SiO2→H2SiO3→Na2SiO3
难度: 简单查看答案及解析
-
如图表示AlCl3溶液与NaOH溶液相互滴加过程中微粒的量的关系曲线,下列判断错误的是
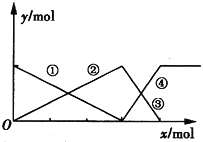
A. ①线表示Al3+的物质的量的变化 B. x表示AlCl3的物质的量
C. ②③线均表示Al(OH)3的物质的量的变化 D. ④线表示[Al(OH)4]-的物质的量的变化
难度: 中等查看答案及解析
-
下列各组物质的无色溶液,不用其他试剂即可鉴别的是
①KOHNa2SO4AlCl3②Na2CO3Ba(OH)2H2SO4③HClNa[Al(OH)4]NaHSO4④Ca(OH)2Na2CO3BaCl2
A.①②
B.②③
C.①③④
D.①②④
难度: 中等查看答案及解析
-
两种微粒含有相同的质子数和电子数,这两种微粒可能是
①两种不同的原子;②两种不同元素的原子;③一种原子和一种分子;④一种原子和一种离子;⑤两种不同分子;⑥一种分子和一种离子;⑦两种不同阳离子;⑧两种不同阴离子;⑨一种阴离子和一种阳离子
A. ①③⑤⑥⑦⑧ B. ①③⑤⑦⑧
C. ①③④⑤⑦ D. 全部都是
难度: 中等查看答案及解析
-
硫酸铝、硫酸钾、明矾三种物质组成的混合物中,当SO42-的浓度为0.20 mol·L-1时,加入等体积的0.20 mol·L-1的KOH溶液(混合后溶液体积变化忽略不计),使生成的白色沉淀恰好溶解,那么最后混合物中K+的浓度是( )
A.0.20 mol·L-1 B.0.25 mol·L-1 C.0.225 mol·L-1 D.0.45 mol·L-1
难度: 困难查看答案及解析
-
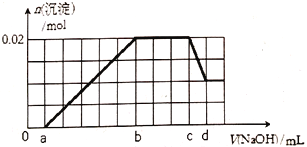
将一定量的A12O3固体加入100mLNaOH溶液中,固体全部溶解,向所得溶液中逐滴加入1.0 mol•L-1盐酸,所得沉淀的物质的量与加入盐酸体积的关系如图所示(不考虑溶液体积的变化),则下列说法正确的是

A. 原NaOH溶液的浓度为1.0mol/L B. 原A12O3的质量为0.51g
C. V0的数值为35 D. 沉淀量达到最大时,溶液的溶质有两种
难度: 中等查看答案及解析