-
下列实验现象的描述错误的是
A.红磷在空气中燃烧,产生大量白烟 B.氢气在空气中燃烧,产生淡蓝色火焰
C.碳在氧气中燃烧发出白光,生成黑色固体 D.硫在氧气中燃烧,发出蓝紫色火焰
难度: 中等查看答案及解析
-
用分子的知识解释下列现象,其中合理的是
A. 水结成冰,是因为水分子停止了运动
B. 变瘪了的乒乓球放在热水中鼓起,是由于分子的体积变大
C. 加入糖的水变甜,是由于分子永不停息的做无规则运动
D. 1L大豆与1L水混合后总体积小于2L,是由于分子间有间隙
难度: 简单查看答案及解析
-
薯片放置于空气中一段时间,变得不再松脆,说明空气中含有( )
A. 氮气 B. 氧气 C. 水蒸气 D. 二氧化碳
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 相对原子质量就是原子的实际质量
B. 湿衣服在阳光下比阴凉处干得快,原因是水分子受热后运动速率加快
C. 气体比液体容易被压缩,原因是物质的气态分子小而液态分子大
D. 过氧化氢分子能分解成水分子和氧分子,说明分子是化学变化中的最小微粒
难度: 简单查看答案及解析
-
化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数与质子数之和,如136C表示核内有6个质子和7个中子的碳原子。下列关于13153I和12753I的说法错误的是
A.各一个原子相比较,质子数相同 B.各一个原子相比较,中子数相同
C.各一个原子相比较,核外电子数相同 D.属于同种元素
难度: 中等查看答案及解析
-
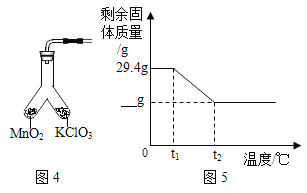
下图是用来测定空气中氧气含量的装置,下列有关该实验的说法正确的是
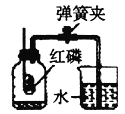
A. 红磷燃烧时产生大量白色烟雾 B. 由此实验可推测氮气难溶于水
C. 燃烧匙中的红磷可换成细铁丝 D. 红磷量不足导致测定结果偏大
难度: 中等查看答案及解析
-
下列化学方程式正确的是( )
A. S+O2
SO2↑ B. 4Al+3O2
2Al2O3
C. P+O2
PO2 D. Mg+O2
MgO2
难度: 简单查看答案及解析
-
正确的实验操作对实验结果、人身安全都非常重要。下列实验操作正确的是

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
甲、乙是两种粒子的结构示意图,下列说法正确的是( )

A. 甲是阳离子 B. 乙是阴离子
C. 甲、乙属于不同种元素 D. 甲、乙都属于金属元素
难度: 中等查看答案及解析
-
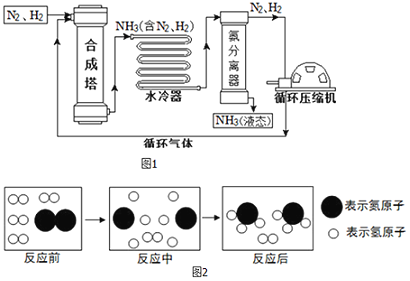
如图是某种化学反应的微观示意图,从中获得的信息不正确的是( )

A. 该反应是化合反应
B. 反应前后原子的种类、个数都不变
C. 甲和乙两种物质的相对分子质量比为11∶4
D. 甲、乙、丙三种物质的分子数比为1∶1∶1
难度: 中等查看答案及解析
-
在“2A+3B
2C+4D”的反应中,已知8g物质A完全反应生成11g物质C和9g物质D。若A的相对分子质量为32,则物质B的相对分子质量是( )
A. 16 B. 32 C. 48 D. 64
难度: 简单查看答案及解析
-
三甲基一氯硅[(CH3)3SiCl]是一种生产有机硅化合物的原料,遇火能燃烧甚至会发生爆炸,与水接触可产生盐酸.则下列说法错误的是( )
A. 保存三甲基一氯硅时应密封防水
B. 三甲基一氯硅中碳氢元素质量比为4:1
C. 三甲基一氯硅属于有机化合物
D. 三甲基一氯硅由碳、氢、硅、氯四个原子构成
难度: 简单查看答案及解析
-
根据图示信息和已学知识判断,下列说法正确的是( )

A. 镁元素位于元素周期表的第三周期,镁原子核内有12个质子
B. 氯的相对原子质量为35.45g,在化学变化中,氯原子易得电子
C. 当X=8时,该微粒属于稀有气体元素的原子
D. 镁离子与氯离子的电子层数相等
难度: 简单查看答案及解析
-
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表
物 质
甲
乙
丙
丁
反应前质量(g)
4
18
10
1
反应后质量(g)
待测
2
21
10
关于此反应,下列认识正确的是()
A. 该变化的基本反应类型是化合反应 B. 参加反应的甲、丙的质量比为2:11
C. 丙、丁的相对分子质量比一定为11: 9 D. 甲反应后的质量为0g
难度: 简单查看答案及解析